120-94 french - Cardiologie actualités

Présenté et commenté par:
JUAN CARLOS MONGE, M.D.
La thrombose athéroscléreuse est la conséquence de
la rupture d’une plaque athéromateuse et d’une throm-
bose surajoutée. Elle est à l’origine des signes cliniques
de la maladie cérébro-vasculaire ischémique, de la car-
diopathie ischémique et de la maladie vasculaire
périphérique. Les plaquettes déclenchent le processus
de thrombose aiguë et contribuent à la formation d’une
plaque stable. Le clopidogrel entrave l’activation pla-
quettaire ADP-dépendante et inhibe également d’autres
mécanismes qui ne sont pas touchés par des agents tels
que l’AAS. Comme les auteurs de l’essai CAPRIE2l’ont
démontré, le clopidogrel est plus efficace que l’AAS
pour prévenir les événements athérothrombotiques et
offre un excellent profil d’innocuité et d’efficacité.
Thrombose athéroscléreuse
Le terme thrombose athéroscléreuse se réfère à une
séquence d’événements entraînant la production d’une
plaque athéromateuse à laquelle se surajoute une thrombose.
C’est un mécanisme à deux stades: premièrement, la forma-
tion d’une plaque athéromateuse, un processus qui prend de
nombreuses années, voire des décennies; deuxièmement,
l’occlusion thrombotique du vaisseau, un processus qui
survient en quelques minutes et qui est dû habituellement à
la rupture d’une plaque athéromateuse instable. Ensemble,
ces processus sont à l’origine des signes cliniques de la
maladie cérébro-vasculaire ischémique, de la cardiopathie
ischémique et de la maladie vasculaire périphérique.
Activation plaquettaire
Les plaquettes jouent un rôle important dans le proces-
sus d’occlusion vasculaire thrombotique. Elles contribuent
au déclenchement du processus et à la formation d’une
plaque stable. L’occlusion vasculaire thrombotique survient
habituellement après la rupture d’une plaque instable qui
entraîne ultérieurement la libération de nombreux com-
posants, tels que le facteur tissulaire, qui sont à l’origine de la
formation de thrombine. La thrombine peut non seulement
transformer le fibrinogène en fibrine, mais c’est un activateur
plaquettaire puissant.
Un autre aspect du rôle des plaquettes dans la thrombose
athéroscléreuse, à savoir leur contribution à la formation et à
la croissance de la plaque athéromateuse, est moins certain.
Cependant, la recherche immunohistochimique a conduit à
l’identification de composants dérivés des plaquettes à l’in-
térieur des plaques athéromateuses. Ceux-ci comprennent,
entre autres, le facteur plaquettaire 4 et le facteur de crois-
sance dérivé des plaquettes. Ainsi, la formation de thrombi à
l’intérieur des plaques pourrait jouer un rôle dans le
développement de lésions athéroscléreuses à long terme.
Il est également possible que les plaquettes ne soient
pas identiques chez tous les individus et que chez certains
patients atteints de thrombose athéroscléreuse grave, les
plaquettes soient hyperréactives et réagissent plus facile-
ment au processus d’activation. Par exemple, on a signalé
que des anomalies au niveau du récepteur glycoprotéinique
Nouvelles tendances dans le traitement
de la thrombose athéroscléreuse
Présenté par: K. SCHRÖR, M.D., C. PRENTICE, M.D., J.R. HAMPTON, M.D., R.L. HABERL, M.D.
Symposium satellite du XIXe Congrès de la Société européenne de cardiologie
Stockholm, Suède, le 27 août 1997
Actualités scientifiquesMC
Cardiologie
UNIVERSITY
OF TORONTO
ST. MICHAEL’S HOSPITAL
RAPPORT DE LA DIVISION DE CARDIOLOGIE
ST. MICHAEL’S HOSPITAL, UNIVERSITÉ DE TORONTO
Division de cardiologie St. Michael’s Hospital
30 Bond St., suite 701A
Toronto, Ontario M5B 1W8
Télécopieur: (416) 864-5330
Les opinions exprimées sont exclusivement
celles des membres de la division.
Publié grâce à des subventions sans restrictions.
Luigi Casella, M.D.
Robert J. Chisholm, M.D.
Paul Dorian, M.D.
David H. Fitchett, M.D.
Michael R. Freeman, M.D.
Shaun Goodman, M.D.
Robert J. Howard, M.D.
Stuart Hutchison, M.D.
Anatoly Langer, M.D. (rédacteur)
Gordon W. Moe, M.D.
Juan Carlos Monge, M.D.
David Newman, M.D.
Trevor I. Robinson, M.D.
Duncan J. Stewart, M.D. (chef)
Bradley H. Strauss, M.D.
Kenneth R. Watson, M.D.

(Gp) IIb/IIIa, un récepteur qui se lie au fibrinogène activé
par l’ADP et la thromboxane A2, sont associées à un risque
accru de coronaropathie. Il est possible que le polymor-
phisme des plaquettes soit lié au risque de thrombose
athéroscléreuse.
La relation existant entre les plaquettes et l’endothélium
vasculaire joue probablement un rôle important dans la for-
mation des plaques athéromateuses ainsi que dans la throm-
bose vasculaire aiguë. Par conséquent, la validation clinique
d’inhibiteurs plaquettaires plus nouveaux et plus efficaces est
une démarche importante dans l’évolution du traitement de
la thrombose athéroscléreuse en particulier en raison des
effets antiplaquettaires relativement faibles de l’acide acétyl-
salicylique (AAS) (voir la figure 1).
Rôle de l’inhibition de l’ADP
La surface normale de l’endothélium est antithrombo-
tique. Cependant, après la rupture d’une plaque, il se produit
une stimulation des plaquettes par des forces de cisaillement
sous l’influence d’activateurs sécrétés tels que l’ADP, la
thromboxane A2, la thrombine, la sérotonine et d’autres
médiateurs entraînant l’activation et l’agrégation plaquet-
taires. De nombreuses substances interviennent dans cette
voie. L’AAS entrave spécifiquement la production de throm-
boxane et toutes les voies d’activation thromboxane-dépen-
dantes. Des composés comme la ticlopidine ou le clopidogrel
ont pour fonction principale d’inhiber l’ADP.
Le clopidogrel entrave l’activation plaquettaire ADP-
dépendante et inhibe également d’autres mécanismes sur
lesquels l’AAS n’a aucun effet. Le clopidogrel a une action
plus marquée dans toutes les situations où l’ADP est un
agoniste important. Il a un large spectre d’activité et est
potentiellement plus efficace que l’AAS. Le clopidogrel
inhibe également l’activation du récepteur glycopro-
téinique IIb/IIIa, bien qu’il ne soit pas un antagoniste du
récepteur lui-même dans le sens traditionnel du terme. Le
clopidogrel est qualitativement différent des inhibiteurs
des récepteurs glycoprotéiniques IIb/IIIa car il n’entrave
pas directement la formation de complexes avec les récep-
teurs du fibrinogène.
Il existe deux types de récepteurs de l’ADP. Le P2X1 est
couplé au calcium et a peu d’importance dans le cadre de
cette discussion. Le second récepteur, le P2Y1, est un récep-
teur couplé à la protéine G qui entraîne l’activation de la gly-
coprotéine IIb/IIIa et l’agrégation plaquettaire.
Un autre mode d’action intéressant de l’ADP est qu’il
stimule la synthèse d’une protéine G qui inhibe l’adénylcy-
clase. Le clopidogrel, qui agit à ce niveau, prévient la baisse
des taux d’AMP cyclique associée à la liaison à l’ADP et à l’ac-
tivation plaquettaire. Les trois principaux objectifs pharma-
cologiques du clopidogrel sont donc les suivants:
•le récepteur de l’ADP lui-même,
•les voies régulatrices principales entraînant l’activation de
la glycoprotéine IIb/IIIa,
•le maintien de taux accrus d’AMP cyclique après la stimu-
lation des récepteurs de l’ADP.
Chez les patients traités à l’aide des doses standard de
clopidogrel, on a noté une diminution de 60 à 70% des sites
de liaison à l’ADP. Cela entraîne un effet irréversible sur la
durée de vie de la plaquette. Les effets du clopidogrel ne se
manifestent pas avant 2 à 4 heures après son administration
et les effets cliniques complets se manifestent entre 3 et
7jours après la dose initiale. Un effet maximal précoce pour-
rait être obtenu avec une dose de charge.
Le clopidogrel n’est pas un composé actif, mais on ne
connaît pas actuellement le site de production de son
métabolite actif de même que son site d’action, étant donné
que l’on ignore s’il agit sur les plaquettes matures ou dans les
mégacaryocytes. Un autre aspect qui n’a pas été clairement
défini est la question de savoir si l’usage concomitant du
clopidogrel et de l’AAS offrirait des effets bénéfiques addi-
tionnels. En théorie, étant donné que les voies de la throm-
boxane sont indépendantes des voies de l’ADP, la
combinaison est une option intéressante, en particulier dans
les situations d’activation plaquettaire aiguë. De récentes
données sur un autre inhibiteur de l’ADP, la ticlopidine,
administrée à des patients après l’implantation de tuteurs
coronaires appuient cette hypothèse1.
Cardiologie
Actualités scientifiques
Dysfonction endothéliale
Adhésion plaquettaire
Activation plaquettaire
Sécrétion plaquettaire
Agrégation plaquettaire
GP Ib/IX, facteur de
von Willebrand,
GP IIb/IIIa
ADP
Thromboxane A2
Glycoprotéine IIb/IIIa
(Aspirin)
(abciximab,
integrelin,
tirofiban)
(clopidogrel,
tidopidine)
Figure 1: Modes d’action des inhibiteurs plaquettaires

Résultats de l’étude CAPRIE
Dans l’étude CAPRIE2(comparaison du clopidogrel et de
l’AAS chez des patients à risque d’événements ischémiques), les
effets de ces deux inhibiteurs plaquettaires chez des patients
ayant présenté auparavant un accident cérébro-vasculaire d’ori-
gine ischémique, un infarctus du myocarde ou une maladie vas-
culaire périphérique ont été comparés. Le clopidogrel est un
dérivé de la thiénopyridine qui inhibe la thrombose principale-
ment en bloquant le récepteur plaquettaire de l’ADP. Les
auteurs de l’étude CAPRIE ont pris pour hypothèse que la
thrombose athéroscléreuse est une seule maladie accompagnée
de manifestations cliniques multiples selon le territoire vascu-
laire touché. Cette hypothèse a été appuyée par les auteurs d’é-
tudes sur des inhibiteurs plaquettaires ayant travaillé en
collaboration qui ont publié en 1994 une méta-analyse sur des
inhibiteurs plaquettaires, principalement l’AAS. Une réduction
du risque d’événements de 25% a été observée, que les patients
aient souffert d’un accident cérébro-vasculaire, d’un infarctus
du myocarde ou d’une maladie vasculaire périphérique3.
Le clopidogrel a été dérivé de la ticlopidine afin d’ap-
porter une solution aux problèmes de toxicité au niveau de
la moelle osseuse associée à la ticlopidine dans des cas peu
nombreux mais difficiles. Étant donné l’existence de ce pro-
blème, il semble peu probable que la ticlopidine puisse
représenter un produit de remplacement de l’AAS utilisé
comme inhibiteur plaquettaire à long terme.
Un total de 19,885 patients ont participé à l’étude
CAPRIE. Environ un tiers des sujets de l’étude ont été
assignés au hasard à un traitement en raison d’un accident
cérébro-vasculaire antérieur, un tiers en raison d’un infarctus
du myocarde antérieur et un tiers en raison d’une maladie
vasculaire périphérique symptomatique. Le paramètre pri-
maire était la survenue d’un accident cérébro-vasculaire, d’un
infarctus du myocarde ou de la mort vasculaire. Les patients
ont été assignés au hasard à un groupe de traitement à l’aide
de clopidogrel à raison de 75 mg, une fois par jour (n =
9,599) ou à un groupe de traitement à l’aide d’AAS à raison
de 325 mg par jour (n = 9,586). Les caractéristiques initiales
des patients dans les deux groupes ont été bien appariées. On
remarquera qu’environ 17% des sujets qui ont été inclus
dans l’étude car ils présentaient des antécédents d’accident
cardio-vasculaires ou de maladie vasculaire périphérique,
avaient également subi auparavant un infarctus du myocarde.
Après la période de suivi prévue, on a noté 1,960 événe-
ments cibles primaires. Une analyse des sujets retenus au
début de l’étude a indiqué que les patients traités à l’aide du
clopidogrel présentaient un risque annuel d’événement pri-
maire de 5,32 comparativement à 5,83 pour les patients
traités à l’aide d’AAS. Ainsi, l’usage du clopidogrel entraîne
une réduction du risque relatif statistiquement significative
(p = 0,043) de 8,7% (voir la figure 2).
L’étude CAPRIE démontre que le clopidogrel est au
moins aussi sûr que l’AAS, une affirmation qui ne peut être
faite en ce qui concerne de nombreux médicaments. De fait,
la fréquence des événements indésirables était très faible
dans les groupes AAS et clopidogrel. On a noté une diminu-
tion légère mais cliniquement significative des éruptions
cutanées chez les patients traités à l’aide du clopidogrel com-
parativement à l’AAS (0,26% comparativement à 0,1%),
mais un nombre significativement moins élevé de patients
traités à l’aide du clopidogrel ont présenté des hémorragies
gastro-intestinales graves (0,49% comparativement à
0,72%). En ce qui concerne la question importante de la
toxicité hématologique, la neutropénie (<1,200/mm3) a été
extrêmement rare dans les deux groupes, celle-ci étant surve-
nue chez 16 patients recevant de l’AAS et chez seulement
10 patients recevant du clopidogrel.
Le clopidogrel n’a causé aucun effet toxique notable sur
la moelle osseuse et a été associé à un taux d’hémorragie
Cardiologie
Actualités scientifiques
0
0
5
10
15
20
369121518212427303336
Temps depuis la randomisation (mois)
p = 0.043
Aspirin
Clopidogrel
Risque cumulatif (%)
Patients A: 9586 9190 8087 6139 3979 2143 542
à risque C: 9599 9247 8131 6160 4053 2170 539
A=aspirin; C=clopidogrel
D’après CAPRIE Steering Committee. Lancet 1996; 348:1329-39.
Figure 2: Risque cumulatif d’accidents cérébro-vascu-
laires d’origine ischémique, d’infarctus du
myocarde ou de mort vasculaire
Tableau 1: Risques relatifs selon les interventions
Risque relatif d’accident Hémorragie
Médicament cardio-vasculaire intracrânienne
Coumadin -50% (à trois ans) +3%
AAS -25% +0,5%
Clopidogrel -32% +0,3%

gastro-intestinale notablement inférieur comparativement à
l’AAS. Sur la base des résultats de l’étude CAPRIE, le clopi-
dogrel, un nouvel inhibiteur plaquettaire, améliorera les
effets de l’AAS dans la prévention de cinq événements addi-
tionnels par 1000 patients pour chaque année de traitement.
Sur la base d’une méta-analyse3, on peut prévoir que l’Aspirin
préviendrait 19 événements par 1000 années-patients dans
une population comparable à celle de l’étude CAPRIE.
D’après les résultats relatifs à l’efficacité signalés par les
auteurs de l’étude Antiplatelet Trialists Collaboration3et de
l’étude CAPRIE2, l’AAS réduit le risque d’événements vascu-
laires de un quart et le clopidogrel, de un tiers.
Accident cérébro-vasculaire chez les patients
cardiaques
L’accident cérébro-vasculaire peut avoir plusieurs étiolo-
gies chez le patient cardiaque:
•embolisation directe provenant du coeur; chez les patients
présentant ce problème, le traitement anticoagulant a des
effets bénéfiques;
•atteinte des petits vaisseaux intracrâniens (artériolos-
clérose) dont le principal risque est l’hypertension; et
•atteinte des gros vaisseaux comme les carotides et la crosse
de l’aorte, chez 50 à 60% de tous les patients présentant
un accident cérébro-vasculaire.
Cependant, cette vue du processus est orientée sur la
pathologie et plutôt limitée. La vue clinique de ce processus
est beaucoup plus complexe étant donné que la plupart des
patients ayant subi un accident cérébro-vasculaire souffrent
d’atteinte multitronculaire et que le risque d’accident
cérébro-vasculaire chez les patients cardiaques est potentiali-
sé par la présence d’autres facteurs de risque, comprenant
l’âge, les antécédents d’hypertension, l’insuffisance car-
diaque, la dysfonction ventriculaire et les antécédents
d’événements athérothrombotiques.
L’extrapolation des résultats de l’étude CAPRIE et leur
comparaison avec ceux d’études précédentes indiquent que
le risque relatif d’accident cérébro-vasculaire après un infarc-
tus du myocarde varierait selon les différentes interventions,
comme l’indique le tableau 1. Comparativement à d’autres
interventions, le clopidogrel entraîne une réduction
moyenne du risque avec une faible fréquence d’hémorragie et
il est supérieur à l’AAS à cet égard.
Les résultats de l’étude CAPRIE peuvent également être
comparés à ceux d’autres mesures de prévention secondaires,
tel qu’indiqué au tableau 2.
Conclusion
Le traitement antiplaquettaire à l’aide de clopidogrel est
équivalent ou supérieur à d’autres mesures acceptées de
prévention secondaire. Comme le démontre l’étude
CAPRIE, le clopidogrel est au moins aussi sûr et plus effi-
cace que l’AAS pour prévenir les événements athérothrom-
botiques récidivants.
Références
1. Schomig A, Newman FJ, Kastrati A, Schulen H et coll. A randomized
comparison of antiplatelet and anticoagulant therapy after the place-
ment of coronary artery stents. N Engl J Med 1996; 334:1084-1089.
2. Comité directeur de l’étude CAPRIE. A randomised blinded trial of
clopidogrel versus aspirin in patients at risk of ischaemic events.
Lancet 1996; 348: 1329-39.
3. Antiplatelet Trialists Collaboration. Colaborative overview of ran-
domized trials of antiplatelet therapy. BMJ 1994; 308:81-106.
4. Sacks FM, Pfeffer MA, Moye LA, Rouleau JL, Rutherford JO, Cole
TG, Brown L, Warnica JW, Arnold JMO, Won C-C, Davis BR et
Braunwald E au nom des chercheurs de l’étude Cholesterol and
Recurrent Events Trial. N Engl J Med 1996; 335: 1001-1009.
5. MacMahon S, Peto R et coll. Blood pressure, stroke, and coronary
heart disease. Part 1. Prolonged differences in blood pressure
prospective observational studies corrected for the regression dilu-
tion bias. Lancet 1990; 335: 765-74.
©1997 Division de cardiologie, St. Michael’s Hospital, Université de Toronto, seule responsable du contenu de cette publication. Édition: Snell Communication Médicale Inc. avec la collaboration de la Division de car-
diologie, St. Michael’s Hospital, Université de Toronto. Tous droits réservés. Imprimé au Canada. Tout recours à un traitement thérapeutique, décrit ou mentionné dans Actualités scientifiques – Cardiologie, doit être con-
forme aux renseignements d’ordonnance au Canada. Snell Communication Médicale Inc. se consacre à l’avancement de l’éducation médicale continue de niveau supérieur. 120-94F
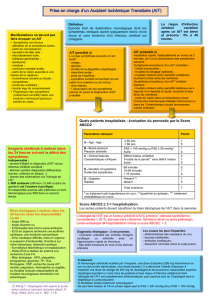
Tableau 2 : Avantages des mesures de prévention acceptées
Intervention Événements prévenus par 1 000 patients/année Source
Aspirin 19 Antiplatelet trialists3
Pravastatine 18 CARE4
Agents antihypertensifs 13 MacMahon 19905
Clopidogrel 24 CAPRIE2
La version française a été revisée par le DrGeorge Honos, Montréal.
1
/
4
100%