DS sur le chapitre dissolution/dilution - Académie de Nancy-Metz

Mercredi 21 Janvier 2015 8h00-9h00
Nom Prénom :
Classe :
Salle :
Laurence Bertolotti Laurence.Bertolotti@ac-nancy-metz.fr
Physique Chimie - Devoir commun 2nde - Sujet A
A. Dissolution
On dissout m = 5,00 g de saccharose dans l’eau. Le volume de la solution est V = 100 m L. Calculer la concentration massique cm de la solution.
B. Masse de soluté à peser
On prépare V' = 500 mL de solution de diiode de concentration massique cm' = 8,0.10 -1 g.L-1. Calculer la masse (m') de soluté à peser ?
C. Quantité de matière
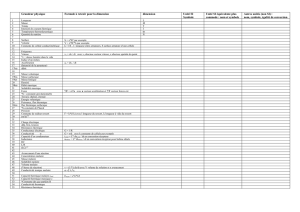
Compléter le tableau sur ce sujet.
D. Dilution
On dispose d’une solution aqueuse S0 de chlorure de sodium de concentration massique c0 = 20 g.L-1.
On souhaite préparer un volume V1 = 200 mL de solution « fille » S1 de concentration massique c1 = 2,0 g.L-1. Calculer le volume V0 de solution
« mère » S0 à prélever.
E. Liste de matériel
Dresser la liste complète du matériel à utiliser pour préparer la solution S1 de la question D.
F. Phénomènes périodiques
Définir la période T d’un phénomène périodique puis exprimer sa fréquence f en fonction de T. Préciser les unités utilisées.
G. Visite médicale
Etienne souhaite se présenter aux sélections internationales des spationautes à Cologne. Une visite médicale est obligatoire au cours de laquelle
l’électrocardiogramme suivant est réalisé (Etienne était alors en état de repos) :
Echelle horizontale :
1 gros carreau
représente 0,125 s
A l’issue de cette première phase, seuls les candidats ayant un cœur qui, au repos, bat entre 60 et 80 pulsations par minute pourront continuer la
suite des tests. Etienne sera-t-il parmi eux ?
G.1. En exploitant l’électrocardiogramme ci-dessus, déterminer la fréquence f du signal puis la fréquence cardiaque en pulsations par minute.
G.2. En utilisant le résultat de la question précédente et les informations de l’énoncé, expliquer si Etienne passera cette première phase de test.
H. Dilutions successives.
Un élève dispose de 100 mL d’une solution aqueuse de chlorure de potassium (solution S0) à la concentration molaire c = 2,0.10-1 mol.L-1. Il prélève
10,0 mL de cette solution qu’il verse dans une fiole jaugée de 200 mL et il complète avec de l’eau distillée jusqu’au trait de jauge (solution S1). Puis il
prélève 25,0 mL de la solution S1 obtenue et la transfère dans une fiole jaugée de 100,0 mL (solution S2). Enfin, il dilue 5 fois la solution S2 pour
obtenir une solution très diluée S3. Calculer la concentration molaire de la solution S3.
Niveau d’acquisition
coefficient
Question
Compétence évaluée
A B C D
G2 H
S’APPROPRIER - Rechercher, extraire et organiser l’information en lien avec une
situation
□ □ □ □
2
E
ANALYSER - Choisir, concevoir ou justifier un protocole / dispositif expérimental
□ □ □ □
1
A B C D H
REALISER - Effectuer un calcul simple
□ □ □ □
2
G1
VALIDER - Exploiter et interpréter des observations, des mesures
□ □ □ □
1
A B D F
VALIDER - Utiliser les symboles et unités adéquats
□ □ □ □
2
F
COMMUNIQUER - Utiliser les notions et le vocabulaire scientifique adaptés
□ □ □ □
1
G2
COMMUNIQUER - Présenter, formuler une proposition, une argumentation, une
synthèse ou une conclusion de manière cohérente complète et compréhensible
□ □ □ □
1
Barème : Acquis A = 2 pts Presque acquis B = 1,5 pt En cours d’acquisition C = 1 pt Non acquis D = 0 pt
Données
Elément
Na
Cl
Cu
S
O
H
Masse molaire atomique M (g.mol-1)
23,0
35,5
63,5
32,1
16,0
1,0
Espèces chimiques
Masse molaire M (g.mol-1)
Masse m (g)
Quantité de matière n (mol)
NaCl
100
CuSO4,5H2O
3,1

Mercredi 21 Janvier 2015 8h00-9h00
Nom Prénom :
Classe :
Salle :
Physique Chimie - Devoir commun 2nde - Sujet B
A. Dissolution
On dissout m = 3,00 g de saccharose dans l’eau. Le volume de la solution est V = 100 m L. Calculer la concentration massique cm de la solution.
B. Masse de soluté à peser
On prépare V' = 250 mL de solution de diiode de concentration massique cm' = 8,0.10 -1 g.L-1. Calculer la masse (m') de soluté à peser ?
C. Quantité de matière
Compléter le tableau sur ce sujet.
D. Dilution
On dispose d’une solution aqueuse S0 de chlorure de sodium de concentration massique c0 = 20 g.L-1.
On souhaite préparer un volume V1 = 250 mL de solution « fille » S1 de concentration massique c1 = 2,0 g.L-1. Calculer le volume V0 de solution
« mère » S0 à prélever.
E. Liste de matériel
Dresser la liste complète du matériel à utiliser pour préparer la solution S1 de la question D.
F. Phénomènes périodiques
Définir la période T d’un phénomène périodique puis exprimer sa fréquence f en fonction de T. Préciser les unités utilisées.
G. Visite médicale
Nathan souhaite se présenter aux sélections internationales des spationautes à Cologne. Une visite médicale est obligatoire au cours de laquelle
l’électrocardiogramme suivant est réalisé (Nathan était alors en état de repos) :
Echelle horizontale :
1 gros carreau représente 0,102 s
A l’issue de cette première phase, seuls les candidats ayant un cœur qui, au repos, bat entre 60 et 80 pulsations par minute pourront continuer la
suite des tests. Nathan sera-t-il parmi eux ?
G.1. En exploitant l’électrocardiogramme ci-dessus, déterminer la fréquence f du signal puis la fréquence cardiaque en pulsations par minute.
G.2. En utilisant le résultat de la question précédente et les informations de l’énoncé, expliquer si Nathan passera cette première phase de test.
H. Dilutions successives.
Un élève dispose de 100 mL d’une solution aqueuse de chlorure de potassium (solution S0) à la concentration molaire c = 2,0.10-1 mol.L-1. Il prélève
10,0 mL de cette solution qu’il verse dans une fiole jaugée de 200 mL et il complète avec de l’eau distillée jusqu’au trait de jauge (solution S1). Puis il
prélève 25,0 mL de la solution S1 obtenue et la transfère dans une fiole jaugée de 100,0 mL (solution S2). Enfin, il dilue 10 fois la solution S2 pour
obtenir une solution très diluée S3. Calculer la concentration molaire de la solution S3.
Niveau d’acquisition
coefficient
Question
Compétence évaluée
A B C D
G2 H
S’APPROPRIER - Rechercher, extraire et organiser l’information en lien avec une
situation
□ □ □ □
2
E
ANALYSER - Choisir, concevoir ou justifier un protocole / dispositif expérimental
□ □ □ □
1
A B C D H
REALISER - Effectuer un calcul simple
□ □ □ □
2
G1
VALIDER - Exploiter et interpréter des observations, des mesures
□ □ □ □
1
A B D F
VALIDER - Utiliser les symboles et unités adéquats
□ □ □ □
2
F
COMMUNIQUER - Utiliser les notions et le vocabulaire scientifique adaptés
□ □ □ □
1
G2
COMMUNIQUER - Présenter, formuler une proposition, une argumentation, une
synthèse ou une conclusion de manière cohérente complète et compréhensible
□ □ □ □
1
Barème : Acquis A = 2 pts Presque acquis B = 1,5 pt En cours d’acquisition C = 1 pt Non acquis D = 0 pt
Données
Elément
Na
Cl
Cu
S
O
H
Masse molaire atomique M (g.mol-1)
23,0
35,5
63,5
32,1
16,0
1,0
Espèces chimiques
Masse molaire M (g.mol-1)
Masse m (g)
Quantité de matière n (mol)
O2
32,0
2,0.10-1
NaCl
200
CuSO4,5H2O
6,2
1
/
2
100%