Exercice Un volume V = 25,0 mL de cyclohexanol C6H11—OH est

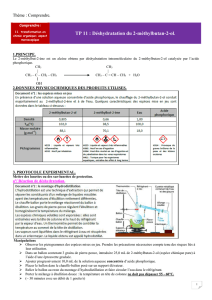
Exercice
Un volume V = 25,0 mL de cyclohexanol C6H11—OH est agité avec Vacide = 60 mL d’une solution d’acide
chlorhydrique de concentration molaire C = 11 mol.L-1. Après trente minutes d’agitation, le mélange est
introduit dans une ampoule à décanter.
La phase aqueuse est éliminée, puis la phase organique est lavée avec une solution d’hydrogénocarbonate de
sodium ( Na+(aq) + HCO3-(aq) ), et enfin traitée par du sulfate de magnésium anhydre.
La phase organique est filtrée, puis distillée ; la masse de distillat alors recueilli vaut m = 25,7g.
1. Ecrire l’équation de la réaction de synthèse
2. Faire un schéma de l’ampoule à décanter en précisant la position des deux phases.
3. Lors du lavage par la solution d’hydrogénocarbonate de sodium, un dégagement gazeux se produit ;
quelle est sa nature ? Ecrire l’équation de sa réaction de formation.
4. Comment vérifier, à l’aide d’un test simple, la nature du produit formé lors de cette réaction ? Décrire
le test correspondant.
5. Comment vérifier, lors de la manipulation, que le produit obtenu est le chlorocyclohexane ?
6. Déterminer le réactif limitant de cette synthèse et en déduire le rendement de cette syntèse.
Données :
- (cyclohexanol) = 0,962 g.mL-1 ;
- (chlorocyclohexane) = 1,00 g.mL-1 ;
- (phase aqueuse) = 1,10 g.mL-1 ;
- éb(chlorocyclohexane) = 142°C.
- éb(cyclohexanol) = 161 )C.
Exercice
Un volume V = 25,0 mL de cyclohexanol C6H11—OH est agité avec Vacide = 60 mL d’une solution d’acide
chlorhydrique de concentration molaire C = 11 mol.L-1. Après trente minutes d’agitation, le mélange est
introduit dans une ampoule à décanter.
La phase aqueuse est éliminée, puis la phase organique est lavée avec une solution d’hydrogénocarbonate de
sodium ( Na+(aq) + HCO3-(aq) ), et enfin traitée par du sulfate de magnésium anhydre.
La phase organique est filtrée, puis distillée ; la masse de distillat alors recueilli vaut m = 25,7g.
1. Ecrire l’équation de la réaction de synthèse
2. Faire un schéma de l’ampoule à décanter en précisant la position des deux phases.
3. Lors du lavage par la solution d’hydrogénocarbonate de sodium, un dégagement gazeux se produit ;
quelle est sa nature ? Ecrire l’équation de sa réaction de formation.
4. Comment vérifier, à l’aide d’un test simple, la nature du produit formé lors de cette réaction ? Décrire
le test correspondant.
5. Comment vérifier, lors de la manipulation, que le produit obtenu est le chlorocyclohexane ?
6. Déterminer le réactif limitant de cette synthèse et en déduire le rendement de cette syntèse.
Données :
- (cyclohexanol) = 0,962 g.mL-1 ;
- (chlorocyclohexane) = 1,00 g.mL-1 ;
- (phase aqueuse) = 1,10 g.mL-1 ;
- éb(chlorocyclohexane) = 142°C.
- éb(cyclohexanol) = 161 )C.

1
/
2
100%