ASA 2004 ASA 20 04

L’anatomie au service des blocs
locorégionaux
L’équipe de Chicago a présenté deux travaux dont l’objet
était de tirer profit des connaissances anatomiques pour faci-
liter la pratique clinique. On sait ainsi, depuis le travail de
Benzon et al. (Anesthesiology 1997;87:547-52),que,lors
de la réalisation d’un bloc sciatique au creux poplité en
injection unique, la réponse musculaire permettant d’obte-
nir un bloc sensitif complet dans 100 % des cas est l’inver-
sion du pied. L’hypothèse avancée pour expliquer ce résultat
était que l’inversion du pied est un mouvement résultant de
la contraction des muscles tibial postérieur et tibial antérieur,
qui sont respectivement innervés par le nerf tibial et le nerf
fibulaire commun. En d’autres termes, l’inversion du pied
témoigne du fait que l’aiguille de neurostimulation se
situe entre les deux contingents du nerf sciatique, position
idéale si l’objectif est la diffusion la plus large possible de
la solution anesthésique. Ces résultats ont été confirmés au
décours de l’approche infraglutéale (Sukhani et al., Anesth
Analg 2004;99:584-8) avec un délai d’action raccourci et
un taux de succès plus important pour l’inversion du pied par
comparaison aux autres réponses musculaires. On peut aller
encore plus loin dans la précision et décomposer la réponse
à type d’inversion en adduction (muscle tibial antérieur) et
d’inversion en supination (muscle tibial postérieur).
Nader et al. (abstract A-900) ont ainsi comparé le délai d’ins-
tallation et le taux de succès d’un bloc sciatique abordé en
infraglutéal selon que la réponse musculaire était de type
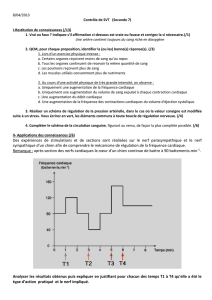
adduction, supination ou flexion des orteils. Les résultats
montrent que la réponse musculaire en supination du pied
procurait le délai d’action le plus rapide et le taux de succès
le plus élevé (figure 1). La supination résulte d’une contrac-
tion du muscle tibial postérieur, lui-même innervé par des
fascicules nerveux situés au bord latéral du nerf tibial, et
donc à proximité du nerf fibulaire commun. Toute la diffi-
culté réside dans l’analyse fine de mouvements du pied qui,
parfois, restent d’interprétation difficile !
La même équipe (Yaghmour et al., abstract A-891) pro-
pose de prédire l’installation d’un bloc sciatique à partir
du testing cutané du nerf sural. Ce dernier a en effet une
double origine dans le nerf tibial et dans le nerf fibulaire
commun. Par ailleurs, le nerf étant de petit diamètre par rap-
port aux deux composants du nerf sciatique, l’installation
de l’anesthésie sur son territoire cutané devrait être rapide.
À partir de cette hypothèse, les auteurs ont étudié l’instal-
lation d’un bloc sciatique (abord sous-glutéal) dans les ter-
ritoires cutanés des nerfs sural, fibulaire commun, fibulaire
superficiel et tibial postérieur chez 180 patients opérés de
la cheville. L’installation de l’anesthésie au bord latéral du
pied à 2 et à 4 minutes après le bloc est celle qui prédit le
mieux une installation complète du bloc sciatique à
Les techniques d’anesthésie
et d’analgésie locorégionales
5
Le Courrier de l’algologie (4), no1, janvier/février/mars 2005
ASA 2004
ASA 2004
Figure 1. Délai d’installation et succès du bloc sciatique selon la
réponse motrice obtenue.
20
0100 20
Flexion plantaire (n = 47),
8 ont reçu un bloc de complément
Inversion : adduction (n = 31),
1 a reçu un bloc de complément
Inversion : supination (n = 21),
pas de bloc de complément
30
Temps (mn)
Pourcentage de patients
avec un bloc complet
40 50 60
40
60
80
100
CHAPITRE 1

6
Le Courrier de l’algologie (4), no1, janvier/février/mars 2005
ASA 2004
ASA 2004
25 minutes. Ce test est d’autant plus intéressant que l’injec-
tion unique s’est faite sur une réponse en flexion plantaire
des orteils (Sukhani et al., Anesth Analg 2004;99:584-8)
et que le taux de succès à 25 minutes passe à plus de
96 % lorsqu’on ne retient que les patients dont le territoire
cutané sural est bloqué à 2 minutes !
La neurostimulation dans tous ses états
L’équipe de Singelyn (Bruxelles) a présenté deux commu-
nications sur ce thème. Le travail de Fuzier et al. (abstract
A-889)confirme les résultats récemment publiés par Had-
zic (Anesthesiology 2004;100:1526-30) montrant que la
position de l’électrode cutanée (sur le membre ipsilatéral ou
sur le membre opposé) n’avait aucune importance, à en juger
par le courant minimal nécessaire pour obtenir une réponse
musculaire. On remarque que les mesures ont été pratiquées
à faible intensité et donc en approche finale, là où le neuro-
stimulateur délivre les intensités demandées. Cette ques-
tion du positionnement de l’anode a plus d’intérêt en début
de recherche, au moment où l’on demande au neurosti-
mulateur de délivrer des intensités élevées. Théoriquement,
en effet, plus la distance électrode-aiguille est grande, plus
la résistance est grande, et plus il est difficile, pour des neuro-
stimulateurs de faible impédance, de maintenir un courant
constant. La distance électrode-aiguille est donc un facteur
négligeable en comparaison de la qualité des électrodes et
des caractéristiques de la peau du patient.
Dans le second travail, Richez et al. (abstract A-890) partent
de la quantité de courant en nC (nanoCoulomb) pour définir
un seuil en deçà duquel on peut considérer que l’extrémité
de l’aiguille est suffisamment proche du nerf pour injecter
la solution anesthésique. Ce courant-seuil est habituelle-
ment de 0,5 mA à 100 µs, soit 50 nC. Peut-on considérer
comme valide ce seuil de 50 nC quelle que soit la durée
de stimulation ? Pour le savoir, les auteurs ont réalisé des
blocs sciatique, fémoral et médian avec une quantité de
courant initiale de 150 nC et une durée de stimulation de
50 µs jusqu’à l’obtention d’une réponse musculaire. La
quantité de courant est ensuite progressivement diminuée
tant que la réponse musculaire est toujours présente. Sans
mobiliser l’aiguille de neurostimulation, la durée de stimu-
lation est ensuite portée à 150 et à 300 µs. Pour ces durées,
la quantité minimale de courant nécessaire au maintien de
la réponse musculaire est alors enregistrée, et les résultats
montrent qu’avec des durées courtes (50 et 150 µs), le seuil
de moins de 50 nC peut être atteint. En revanche, pour des
durées plus longues (300 µs), considérer un tel seuil mini-
mum ≤50 nC peut s’avérer dangereux, puisque les quan-
tités minimales de courant permettant d’obtenir une réponse
musculaire se situent entre 68 et 79 nC ! Au total, il n’est
pas souhaitable de parler en nC, car la durée est un facteur
clé qui doit toujours être précisé. Une durée courte est plus
discriminante, plus précise pour une approche finale. Il reste
donc de beaux jours aux mA et aux µs, malgré les nC…
Désinfection cutanée
et anesthésie péridurale : …CQFD
L’effet de trois “désinfectants” (povidone iodée/isopropa-
nol + povidone iodée/chlorhexidine alcoolisée) sur la conta-
mination de l’aiguille et du cathéter de péridurale par des
bactéries de la flore cutanée a été comparé par une équipe
japonaise (Shibata et al., abstract A-928). Pour ce faire,
282 patients bénéficiant d’un acte chirurgical avec indica-
tion d’une anesthésie/analgésie péridurale ont été répartis
en trois groupes : dans le premier (n = 98), la peau a été
préparée avec de la povidone iodée à 10 % appliquée en
deux couches ; dans le second (n = 87), l’application d’iso-
propanol à 70 % était suivie de deux applications de povi-
done iodée à 10 % ; le dernier groupe (n = 97) recevait deux
applications de chlorhexidine alcoolisée à 80 %. Immédia-
tement après la pose du cathéter de péridurale, l’extrémité
de l’aiguille était mise en culture. Le cathéter était retiré entre
J1 et J8 et son extrémité était également mise en culture.
Les résultats ont montré une incidence significativement
plus importante de colonisation bactérienne avec les deux
solutions de povidone iodée qu’avec la chlorhexidine
alcoolisée à 80 %, au niveau de l’extrémité de l’aiguille
(39,8 % vs 36,8 % vs 6,2 %) ainsi que du cathéter (40,8 % vs
33,3 % vs 14,4 %). La contamination des cathéters montés
au travers d’aiguilles, elles-mêmes contaminées, était
significativement plus importante que celle observée sur
des cathéters montés au travers d’aiguilles non contaminées
(67,5 % vs 15,1 %). Les auteurs en ont conclu que la conta-
mination de l’aiguille de péridurale est une source de con-
tamination du cathéter et que la chlorhexidine alcoolisée est
plus puissante que les solutions de povidone iodée.
La bétadine (povidone iodée) est un antiseptique fréquem-
ment utilisé pour la désinfection cutanée avant la pose
d’une péridurale. Lorsqu’on ne s’intéresse qu’à la conta-
mination cutanée par des prélèvements de surface à l’aide
d’un écouvillon, on peut observer un taux de réussite
important, avec une désinfection à plus de 95 % dans cer-

7
Le Courrier de l’algologie (4), no1, janvier/février/mars 2005
ASA 2004
ASA 2004
taines populations (Birnbach et al.,Anesthesiology 1998;
88:668-72). Chez la parturiente, les conditions du travail
et de l’accouchement diminuent considérablement l’effica-
cité de l’antiseptique, avec un taux de désinfection de 70 %
(Hebl et Horlocker. Reg Anesth Pain Med 2003;28:376-9).
Yentur et al. (Reg Anesth Pain Med 2003;28:389-93) avaient
déjà observé, sur une population non obstétricale, qu’en
dépit d’une désinfection correcte de la surface de la peau
avec de la povidone iodée (96,5 %), l’aiguille et le cathéter
de péridurale étaient contaminés avec, respectivement,
34,6 % et 45,8 % de cultures bactériennes positives. Une
explication de cette contamination a été proposée par Sato
et al. (Anesthesiology 1996;85:1276-82) qui montraient,
à partir de biopsies cutanées de patients opérés du dos, la
présence de germes au niveau des follicules pileux. Ces
derniers paraissaient “protégés” de l’action du désinfectant
par des couches lipidiques situées au-dessus de la couche
cornée. Le travail de Yentur et al., déjà cité, montrait clai-
rement que la povidone iodée pouvait être efficace en sur-
face, mais nettement moins en profondeur. L’utilisation
d’une solution alcoolisée avait été évoquée comme facteur
permettant de diminuer la colonisation à partir des couches
profondes, mais le travail présenté à l’ASA ne confirme pas
cette hypothèse puisque, dans un groupe pourtant conta-
miné, la povidone iodée était précédée d’une solution
alcoolisée (isopropanol 70 %). Bien entendu, cela ne doit
pas faire oublier que, à côté du choix de l’antiseptique, il
est tout aussi important de respecter les règles d’hygiène
et d’asepsie qui, malheureusement, font souvent défaut !
Anesthésie locorégionale de l’épaule :
une nouvelle approche supraclaviculaire
Une multitude d’approches ont déjà été publiées pour les
abords supraclaviculaires, et l’équipe de Nice (Armando et al.,
abstract A-1077) a proposé une approche fondée sur des
repères simples et accessibles à tous. Le point de ponction se
situe au bord postérieur du muscle sterno-cléido-mastoïdien,
à 4 cm au-dessus du bord supérieur de la clavicule. L’aiguille
est introduite à 45 ° par rapport au plan cutané, puis avan-
cée en direction du milieu de la clavicule (figure 2).
Les résultats rapportés chez 240 patients montrent un
temps de réalisation de 107 ± 87 secondes et une profon-
deur avant réponse motrice de 27±7mm. L’avancée de
l’aiguille en direction du milieu de la clavicule permet
d’obtenir une réponse musculaire dans 73 % des cas, tan-
dis que l’aiguille devait être réorientée dans une direction
plus caudale dans 22 % des cas, et en direction de l’épaule
homolatérale dans 5 % des cas. Les réponses musculaires
se répartissaient de la façon suivante : axillaire/musculo-
cutané/radial : 39 %, 44 % et 17 % respectivement. Le pour-
centage de succès était de 97 % et les scores de douleur
étaient significativement diminués en salle de soins post-
interventionnels (SSPI). L’expérience de l’opérateur
(195 anesthésistes confirmés vs 95 internes en première
année) ne modifiait pas les résultats obtenus, attestant ainsi
de la faisabilité de la technique.
L’intérêt principal de cette technique réside dans l’éloigne-
ment des structures périmédullaires, grâce à la direction
caudale donnée à l’aiguille ainsi qu’à la facilité de mise
en place d’un cathéter dont la progression se fait dans l’axe
du plexus. Le problème potentiel est le nerf phrénique, qui
est stimulé dans près de 15 % des cas lors de ce bloc. On
connaît également quelques cas (publiés ou non) de para-
lysie définitive du nerf phrénique au décours d’un bloc inter-
scalénique, avec des conséquences respiratoires variables.
La tendance actuelle est donc de dire qu’il ne faut pas recher-
cher cette réponse (contraction du diaphragme) de façon
intentionnelle et que, en cas d’obtention accidentelle de
celle-ci, il faut rapidement se replacer dans un autre plan.
Le bloc paravertébral
Le bloc paravertébral consiste à injecter l’anesthésique
local (AL) à proximité des vertèbres, là où les nerfs spinaux
émergent du foramen intervertébral (figures 3 et 4). Ce bloc
s’accompagne d’un bloc ipsilatéral sur plusieurs dermatomes
au-dessus et en dessous du site d’injection. Il est utile pour
le traitement des douleurs aiguës et chroniques ayant pour
Figure 2. Repères cutanés et direction de l’aiguille dans l’abord sus-
claviculaire (d’après Armando et al., abstract A-1077).

8
Le Courrier de l’algologie (4), no1, janvier/février/mars 2005
ASA 2004
ASA 2004
origine le thorax ou l’abdomen. On assiste depuis quelques
années à un regain d’intérêt pour ce bloc, au point qu’il est
proposé chez l’adulte, chez l’enfant et même chez le
nouveau-né.
Plusieurs techniques sont possibles (position assise ou laté-
rale ou en décubitus ventral). La position assise permet de
mieux identifier les repères cutanés et paraît plus confortable
pour le patient. Une aiguille de 22 G et 100 mm de long
est introduite 2,5 à 3 cm en dehors de la partie la plus ros-
trale de l’apophyse épineuse et est avancée perpendiculai-
rement à la peau jusqu’au contact de l’apophyse transverse
sous-jacente, le plus souvent située à une distance de 2 à
4cm. Le contact osseux est impératif au point que, s’il n’est
pas perçu à cette profondeur, il faut ressortir l’aiguille en
position sous-cutanée pour la rediriger en direction plus
rostrale ou plus caudale jusqu’à obtenir ce contact osseux.
Une fois ce contact obtenu, l’aiguille est progressivement
déplacée pour raser le bord supérieur de l’apophyse trans-
verse puis progresser ensuite en profondeur, jusqu’à ce qu’une
perte de résistance au sérum physiologique ou un “pop”
soient perçus, habituellement à une profondeur de 1 à 1,5 cm.
Après les tests d’aspiration usuels, la solution anesthésique
est injectée de façon fractionnée et/ou un cathéter est intro-
duit sur une longueur de 1 à 3 cm. Un cathéter paravertébral
peut également être positionné de visu par le chirurgien
thoracique. La diffusion de la solution anesthésique peut
rester localisée au niveau d’injection ou diffuser en direc-
tion rostrale, médiale, latérale ou, plus souvent, caudale.
L’administration de 15 à 20 mL (ou 0,3 mL/kg) de bupiva-
caïne à 0,375-0,5 % en injection unique serait aussi efficace
que l’injection de 3 à 4 mL de la même solution à plusieurs
étages anesthésiques pour obtenir une anesthésie unilaté-
rale couvrant 4 à 5 dermatomes thoraciques. Si l’objectif
est de couvrir plus de 5 dermatomes, il faut privilégier les
injections multiples.
Les indications d’analgésie par bloc paravertébral sont nom-
breuses pour l’analgésie postopératoire (chirurgie thoracique
et du sein, cholécystectomie, chirurgie du rein et de l’uretère,
chirurgie herniaire, appendicectomie, etc.), pour l’anes-
thésie chirurgicale (chirurgie du sein, chirurgie herniaire,
exploration chirurgicale d’une plaie thoracique, etc.) et dans
diverses indications aiguës ou chroniques (névralgies post-
herpétiques et postzostériennes, fractures de côtes, douleur
de la capsule hépatique après un traumatisme abdominal,
etc.). Les contre-indications doivent être respectées : infec-
tion locale, empyème thoracique, allergie vraie aux anes-
thésiques locaux, tumeurs paravertébrales, coagulopathies,
et une réflexion préalable sur le rapport risque/bénéfice
doit être menée en présence d’antécédents de cyphoscoliose
ou de thoracotomie. Au total, cette technique est d’appren-
tissage facile, et le taux d’échec varie de 6,8 à 10 %. Les
complications sont les ponctions vasculaires (3,8 %), l’hypo-
tension artérielle (4,6 %), les ponctions pleurales (1,1 %)
et le pneumothorax (0,5 %) (Karmakar, Anesthesiology
2001;95:771-80).
Cet engouement pour le bloc paravertébral s’est concrétisé,
lors du congrès 2004 de l’ASA, par une série de travaux
cliniques dont le but était d’en évaluer l’efficacité.
Sur une courte série de patients programmés pour une
cure de hernie inguinale sous laparoscopie, Halpern et al.
(abstract A-943) ont montré l’efficacité antalgique d’un
bloc paravertébral sur quatre dermatomes (T11 à L2). À
chaque niveau, 5 à 7 mL de ropivacaïne adrénalinée ont été
injectés après identification de l’espace paravertébral. Le
geste chirurgical était ensuite mené sous anesthésie géné-
rale. L’analgésie postopératoire était efficace, à en juger par
la faible consommation antalgique et par la satisfaction des
patients vis-à-vis de cette prise en charge.
Dans le travail de Mebazaa et al. (abstract A-922),le bloc
paravertébral continu a été comparé à un bloc extrapleural
Figure 3. Bloc paravertébral (d’après J. Ripart,
CHU de Nîmes).Figure 4. Technique du bloc paravertébral (noter le changement d’orientation de l’aiguille
après obtention du contact osseux). D’après J. Ripart, CHU de Nîmes.
Peau
Plèvre
Nerf
intercostal
Ligament
costo-transverse
supérieur
Ligament
costo-transverse
inférieur
Apophyse
transverse
Côte

9
Le Courrier de l’algologie (4), no1, janvier/février/mars 2005
ASA 2004
ASA 2004
continu, ce dernier étant mis en place par le chirurgien thora-
cique en période peropératoire. Les deux techniques avaient
une efficacité comparable, qu’il s’agisse des scores de dou-
leur au repos et à la toux, de la consommation de morphine
ou des capacités ventilatoires postopératoires.
Enfin, dans la mesure où la survenue de douleurs chroniques
est corrélée à l’existence de douleurs postopératoires
sévères après chirurgie thoracique ou cure de hernie ingui-
nale, Iohom et al. (abstract A-1129) ont évalué l’incidence
des douleurs chroniques après chirurgie carcinologique du
sein en fonction de la qualité de prise en charge postopéra-
toire de la douleur. Un groupe de patientes avait une prise
en charge “agressive” de la douleur aiguë postopératoire
avec utilisation d’un cathéter paravertébral continu et prise
systématique d’antalgiques, alors que l’autre groupe avait
un traitement antalgique à la demande. Comme on pouvait
s’y attendre, l’évaluation de la douleur postopératoire était
bien meilleure dans le groupe traité activement. De plus,
une interview téléphonique réalisée à 2 et à 3 mois après
la chirurgie a montré qu’aucune des 13 patientes du groupe
ayant eu une prise en charge “agressive” ne présentait de
douleurs chroniques, contre 75 % des 15 patientes de l’autre
groupe. Ces résultats montrent bien que la prise en charge
active de la douleur aiguë en postopératoire (incluant ici l’uti-
lisation d’un cathéter paravertébral) apporte un bénéfice au
patient et à la société, puisque la diminution de l’incidence
des douleurs chroniques s’accompagne d’une diminution des
coûts inhérents à la prise en charge de ces pathologies.
Au total, même si ces études peuvent faire l’objet de cri-
tiques méthodologiques, elles traduisent le fait que le bloc
paravertébral est une technique d’ALR émergente, poten-
tiellement intéressante en chirurgie thoracique et en chi-
rurgie carcinologique mammaire. Lors des lambeaux de
rotation pour reconstruction mammaire, un travail récem-
ment publié montre en outre une amélioration de la pres-
sion tissulaire en oxygène à l’intérieur de ces lambeaux
(Buggy et Kerin, Anesthesiology 2004;100:375-80).
Le bloc parasacré
Le bloc parasacré a été décrit par Mansour en 1993 (Reg
Anesth1993;18:322-3). Plus tard, Morris et al. (Reg Anesth
1997;22:223-8) ont montré que, dans 93 % des cas, on
retrouve un bloc du nerf obturateur au décours de la réali-
sation d’un bloc parasacré. En réalité, l’évaluation du bloc
moteur des adducteurs de cuisse était subjective, et les
auteurs ont donc voulu vérifier ces résultats en utilisant une
méthodologie différente, permettant entre autres d’évaluer
de façon objective la diminution de la force musculaire des
adducteurs de cuisse. Pour ce faire, Iohom et al. (abstract
A-1121) ont emprunté la méthodologie utilisée par Lang
et al. (J Clin Anesth 1993;5:292-6),qui consistait à deman-
der au patient de serrer entre ses genoux un brassard à ten-
sion préalablement gonflé à 40 mmHg. De cette manière,
il suffit de mesurer l’augmentation de pression sur le
sphygmomanomètre : 36 patients opérés du genou ont été
étudiés et ont bénéficié d’un bloc parasacré, dont l’effi-
cacité était jugée sur l’évaluation sensitive. Trente minutes
après la réalisation du bloc parasacré était pratiqué un bloc
sélectif du nerf obturateur, et l’évaluation motrice des adduc-
teurs était poursuivie pendant 15 minutes. Le patient béné-
ficiait en outre d’un bloc fémoral avant d’être amené en salle
d’opération. Les résultats montrent une diminution discrète
de la force des adducteurs au décours du bloc parasacré, sui-
vie d’un véritable effondrement de ce même paramètre au
décours du bloc sélectif du nerf obturateur (figure 5). Le
bloc parasacré s’accompagne rarement d’un bloc du nerf
obturateur, et la diminution de force des adducteurs rap-
portée par Morris et al. était probablement en rapport avec
le bloc du nerf sciatique qui prend en charge une petite partie
de l’innervation des adducteurs de cuisse. Les résultats ont
été confirmés par une étude anatomique chez deux sujets
pour lesquels la diffusion du colorant injecté selon l’ap-
proche simulée du bloc parasacré n’a pu atteindre le nerf
obturateur.
Figure 5. Force musculaire des adducteurs.
*****
*
**
Temps (mn)
Pression générée (mmHg)
0
20
T0
40
60
80
100
120
* p < 0,05
T1 T2 T3 T4 T5 T6 T7 T8 T9
Bloc parasacré
T0 = valeurs préopératoires ; T1 à T6 = 5, 10, 15, 20, 25 et
30 mn après le bloc parasacré ; T7 à T9 = 5, 10 et 15 mn
après le bloc obturateur.
Bloc obturateur
 6
6
 7
7
 8
8
 9
9
1
/
9
100%