Lire l'article complet

Actualité
Actualité
6
Actualité
6
La Lettre d’ORL et de chirurgie cervico-faciale - n° 311 - octobre-décembre 2007
Congrès de l’AFOP 2007
Congress of the French Pediatric ENT Society
M. François*
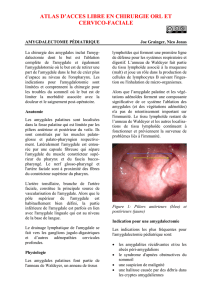
La réunion de printemps de l’Association française d’ORL
pédiatrique s’est tenue cette année au centre de confé-
rence de l’UICP, au pied de la tour Eiff el.
Le thème choisi était l’amygdalectomie.
DONNÉES ÉPIDÉMIOLOGIQUES
(Pr Françoise Denoyelle, hôpital Trousseau, Paris)
Selon les données du PMSI, 72 800 amygdalectomies ont été
pratiquées en France, en l’an 2000, dont 90 % chez des enfants.
Selon l’Agence technique d’information sur l’hospitalisation,
154 000 amygdalectomies et/ou adénoïdectomies ont été
réalisées en 2004, dont 24 % dans le secteur hospitalier public.
En 2002, la Société française d’ORL a fait une enquête par voie
postale auprès de 1 900 ORL français membres de la SFORL
sur les 2 885 en exercice. Trente pour cent ont répondu. Ces
opérateurs faisaient 43 456 amygdalectomies par an, ce qui,
si l’on se réfère aux données du PMSI, représente environ
60 % des amygdalectomies pratiquées. La moyenne d’âge
des opérateurs était de 48 ans, avec des extrêmes de 27 et
77 ans. Vingt pour cent des opérateurs avaient un exercice
hospitalier pur, 55 % une activité purement libérale et 25 %
une activité mixte. L’amygdalectomie était pratiquée dans
74 % des cas par dissection, sous intubation, et dans 26 %
des cas au Sluder
®
: 18 % au Sluder
®
sans intubation et 8 %
au Sluder
®
avec intubation.
RELEVÉ ET ANALYSE DES ACCIDENTS ET INCIDENTS
(Pr François Legent, consultant à la MACSF, Sou Médical)
Le Pr Legent a repris les dossiers de déclaration de sinistre
au cours d’amygdalectomie de l’enfant entre 1997 et 2006.
Il y a eu 29 déclarations, dont 10 avec décès de l’enfant. Les
19 sinistres avec issue médicale favorable se répartissent
comme suit :
• hémorragie ............................................................................ 5
• hyponatrémie avec œdème cérébral ................................ 3
• compresse ou Surgicel
®
laissé(e) dans une loge ............ 4
• brûlure du mollet ou de la commissure labiale ............. 2
• trouble de la phonation ...................................................... 1
• dent lésée ............................................................................... 1
• hépatite virale ....................................................................... 1
• lymphome découvert 1 mois après l’amygdalectomie .... 1
• pneumothorax ........................................................................ 1
Parmi les 10 décès, cinq étaient dus à une hémorragie incon-
trôlée. Dans un cas, le saignement a pu être imputé à l’arra-
chage d’une artère pharyngienne par une pince de Taptas
®
utilisée pour retirer un moignon au pôle inférieur. Le saigne-
ment a été méconnu probablement pendant plusieurs heures
dans deux cas. Dans les deux derniers cas, l’enfant a saigné
a plusieurs reprises et est décédé malgré plusieurs reprises
chirurgicales pour hémostase. Les autres causes de décès
sont l’inhalation au moment de l’intubation, l’hyponatrémie
majeure due à une perfusion mal contrôlée (deux cas), une
surcharge d’anesthésiques et des convulsions.
ÉVOLUTION DES PRATIQUES ANESTHÉSIQUES :
LES NOUVELLES CONTRAINTES
ET LEURS CONSÉQUENCES POUR L’ORL
(Pr Gilles Orliaguet, hôpital Necker, Paris)
Les conclusions du groupe d’experts réunis par la Société
française d’anesthésie et de réanimation (SFAR), l’ADARPEF
et le GAR ORL sur l’anesthésie pour amygdalectomie chez
l’enfant ont été publiées en octobre 2006 et sont disponi-
bles sur le site de la SFAR. Ces recommandations ont été
établies à partir d’une revue de la littérature et de recom-
mandations en médecine factuelle. L’évaluation préopéra-
toire, lors de la consultation d’anesthésie, a pour objectif
d’évaluer le risque et d’informer les parents et l’enfant. Le
bilan préopératoire est fondé avant tout sur l’interrogatoire
et l’examen clinique. Un bilan d’hémostase doit être demandé
chez les enfants de moins de trois ans et chez ceux ayant des
antécédents hémorragiques. L’infection des voies aériennes
au moment de l’intervention majore le risque de complica-
tions respiratoires, en particulier encombrement et pauses.
L’intervention doit être reportée d’au moins trois semaines
en cas de signes spastiques bronchiques, de laryngite aiguë,
de température supérieure à 38 °C. En cas de forme grave
de syndrome d’apnées obstructives du sommeil (SAOS),
il faut faire évaluer la fonction cardiaque (échographie et
consultation) et maintenir une surveillance rapprochée en
salle de réveil pendant 24 heures à cause du risque majoré
de désaturation. Pendant l’intervention, les voies aériennes
doivent être sécurisées, au mieux avec une sonde d’intuba-
tion à ballonnet. La surveillance postopératoire porte sur
* Hôpital Robert-Debré, Paris.

Actualité
Actualité
7
La Lettre d’ORL et de chirurgie cervico-faciale - n° 311 - octobre-décembre 2007
les constantes habituelles, mais aussi sur la vérifi cation de
l’absence de saignement oropharyngé. Les liquides peuvent
être autorisés au bout de 2 heures et l’alimentation au bout
de 6 heures. La douleur postopératoire dure en moyenne une
semaine et est maximale les trois premiers jours. Il faut pres-
crire des antalgiques de paliers I et II, les AINS ne sont pas
recommandés. L’antibioprophylaxie n’est pas recommandée,
hors cas particuliers (valvulopathie, drépanocytose, etc.). Les
apports hydroélectrolytiques doivent être précisés par écrit
et surveillés avec un contrôle du débit. Les complications les
plus graves sont respiratoires et hémorragiques (0,5 à 3 % des
cas), mais les plus fréquentes sont les nausées et les vomisse-
ments (40 à 70 % des cas). L’intervention ne sera réalisée en
ambulatoire qu’en cas d’accord consensuel des parents, de
l’anesthésiste et du chirurgien. Certaines conditions doivent
être réunies (parents comprenant les consignes, ayant un
téléphone, une voiture, n’habitant pas trop loin de l’hôpital
ou de la clinique… et sur le plan médical : enfant de plus de
3 ans, n’ayant pas de SAOS ni de comorbidité).
AMYGDALES OBSTRUCTIVES
(Table ronde modérée par Michel Mondain [Montpellier]
avec la participation de Vincent Couloigner [hôpital Necker],
Henri Girschig [Boulogne-sur-Mer] et Philippe Contencin
[hôpital Necker])
Des études épidémiologiques ont montré que 1 à 3 % des
enfants ont des troubles respiratoires lors du sommeil, avec
un pic de fréquence entre 2 et 6 ans. Ces troubles comportent
à des degrés divers ronfl ements, réveils nocturnes, sueurs,
bavage, pauses, voire apnées. Il s’y associe des troubles diurnes
à type d’asthénie plus que de somnolence. L’obésité est moins
souvent en cause que chez l’adulte. Il faut rechercher une
malformation craniofaciale favorisante, une maladie métabo-
lique ou neuromusculaire et des antécédents de prématurité.
L’examen clinique retrouve bien souvent une hypertrophie
amygdalienne bilatérale, mais doit vérifi er qu’il n’existe pas un
autre obstacle sur les voies aériennes supérieures. Les risques
sont un fl échissement de la croissance staturo-pondérale,
des risques cardiovasculaires et des troubles neurocognitifs,
qui sont trois fois plus fréquents chez les enfants ronfl eurs
que chez les autres.
L’examen de référence pour mettre en évidence la gène
respiratoire lors du sommeil est la polysomnographie, qui
comporte un enregistrement du ronfl ement, par un micro-
phone posé sur le cou, des fl ux ventilatoires pour mettre en
évidence apnées et hypopnées, des mouvements respiratoires
pour diff érencier un trouble périphérique d’un trouble central,
des échanges gazeux par oxymétrie de pouls, de la capnie,
et du sommeil.
Cet examen peut ainsi diff érencier un ronfl ement simple
d’un SAOS et d’un syndrome d’augmentation des résistances
des voies aériennes supérieures (SARVA). Cet examen a été
développé, car la spécifi cité et la sensibilité de la clinique
sont faibles. Il a aussi un intérêt pronostique, car en cas
de SAOS il y a un risque majoré d’apnées en postopéra-
toire, ce qui contre-indique l’ambulatoire, et il y a un risque
d’échec de l’adéno-amygdalectomie sur les symptômes.
Mais l’examen est coûteux, il y a peu de centres, surtout
pour les enfants, et il y a des limites techniques, car les
valeurs normales sont variables selon les laboratoires du
sommeil et les sociétés savantes. L’oxymétrie de pouls et
la polysomnographie de la sieste n’ont de valeur que si
elles sont anormales. La polygraphie à domicile est moins
sensible que la polysomnographie car il manque l’EEG et
la détection des microréveils. L’enregistrement de la capnie
est une technique diffi cile, mais elle a une bonne valeur
prédictive de l’hypertension artérielle pulmonaire et du
risque d’apnées postopératoires par levée de l’hypercapnie.
L’enregistrement audio ou vidéo du sommeil par les parents
permet de rechercher un tirage.
C’est une pathologie de plus en plus fréquente. Cependant,
l’amygdalectomie pour amygdales obstructives n’augmente
pas le risque hémorragique. L’extubation doit se faire préfé-
rentiellement en salle d’opération, pas trop tôt (risque d’in-
halation de sang) ni trop tard (risque de laryngospasme). Les
morphiniques doivent être réduits en cas de SAOS.
La persistance ou la réapparition d’une obstruction des
VAS après adéno-amygdalectomie doit faire rechercher
une repousse de végétations adénoïdes ou un autre facteur
d’obstruction, comme une morphologie craniofaciale
favorisante.
TECHNIQUES CHIRURGICALES
(Table ronde modérée par Gilles Roger,
avec la participation de Seth Pransky [San Diego,
Californie], Martine François [hôpital Robert-Debré, Paris],
Jean Abitbol [Paris] et Pierre Fayoux [Lille])
Parmi les techniques présentées, la plus ancienne est l’amyg-
dalectomie au Sluder
®
. Le principe est d’isoler la base d’im-
plantation de l’amygdale palatine dans la fenêtre du Sluder
®
,
puis de faire une énucléation au doigt. L’hémostase se fait,
car les vaisseaux sont plus arrachés que sectionnés. Cette
technique, qui existe depuis des décennies, donne moins d’hé-
morragies postopératoires que la technique par dissection.
Les douleurs seraient aussi moindres, mais sur ce sujet les
résultats des études sont variés. Ce que l’on peut reprocher
à la technique, c’est le risque de laisser en place un reliquat
amygdalien et la diffi culté d’enseignement lorsqu’elle est
pratiquée sans intubation. Mais cet argument tombe puis-
qu’il y a un consensus des anesthésistes pour intuber tous
les enfants opérés d’amygdalectomie.

Actualité
Actualité
8
La Lettre d’ORL et de chirurgie cervico-faciale - n° 311 - octobre-décembre 2007
L’amygdalectomie par dissection provient des travaux d’ana-
tomie réalisés sur la capsule amygdalienne et menés à la fi n
du XIXe siècle. Le principe est d’inciser le pilier antérieur de
l’amygdale, de mettre en évidence le plan de décollement entre
la capsule et la loge et de dégager progressivement l’amygdale
de celle-ci. Il existe plusieurs variantes : dissection aux ciseaux,
au peigne, à la curette, etc. L’hémostase se fait au bistouri élec-
trique bipolaire (il faut éviter la monopolaire), mais certains
font des points appuyés, ou des ligatures de piliers.
J. Abitbol a présenté la technique d’amygdalectomie au laser
CO
2
. Il s’agit en fait d’une réduction de 30 à 40 % du volume
des amygdales palatines, emportant au moins toute la zone
des cryptes amygdaliennes. Cette technique se pratique
sous anesthésie générale, avec intubation nasale. Le tissu
amygdalien est vaporisé de proche en proche au laser CO2,
sous microscope. S’il apparaît des lumières vasculaires supé-
rieures à 1,6 mm de diamètre, le vaisseau est coagulé à la
pince bipolaire. L’intervention peut se pratiquer à partir
de 4 ans. L’indication principale en est les angines récidivantes.
Les parents choisissent cette technique par opposition à une
autre plus classique soit par peur de la douleur postopératoire
(cette technique est en eff et moins douloureuse), soit parce
qu’ils ont connaissance dans leur entourage de complications
postamygdalectomie. La technique est effi cace dans 85 %
des cas. Dans 15 % des cas, il y a soit un échec immédiat et
l’auteur propose une amygdalectomie par dissection, soit un
échec tardif, après 10 mois, et il propose soit une deuxième
séance laser, soit une amygdalectomie par dissection. Point
non négligeable : comme il est impossible de coter deux
amygdalectomies chez le même patient, l’auteur ne prend
pas d’honoraires pour le deuxième geste chirurgical.
G. Roger a présenté deux techniques plus récentes : la
coblation et le microdébrideur. L’utilisation du microdé-
brideur permet de réduire de 80 à 90 % le volume de tissu
amygdalien. Il s’agit d’une exérèse intracapsulaire, avec un
risque d’hémorragie postopératoire très réduit et moins de
douleur, puisque les muscles de la loge ne sont pas étirés
ni mis à nu.
La coblation combine l’eff et d’une radiofréquence à une solution
saline conductrice. Il y a transfert d’énergie sans échauff ement.
Cette technique permet de faire une exérèse extracapsulaire ou
simplement une réduction amygdalienne. Elle est, d’après les
études publiées (petites séries), moins douloureuse et moins
hémorragique que la technique par dissection.
Le frein pour l’utilisation des deux dernières techniques est
le coût de l’équipement et du consommable.
HÉMORRAGIES PER ET POSTOPÉRATOIRES
(Table ronde modérée par Eréa-Noël Garabédian [hôpital
Trousseau] Esther Harboun-Cohen [Boulogne-Billancourt],
François Legent, Richard Nicollas [hôpital de la Timone,
Marseille] et Sébastien Pierrot [hôpital Necker])
Un à trois pour cent des amygdalectomies se compliquent
d’hémorragies postopératoires. Ces hémorragies surviennent
dans 80 % des cas avant la sixième heure. Une hémorragie
peut survenir jusqu’à 20 jours après l’intervention. Les parents
doivent être informés de ce risque, disposer d’un numéro
de téléphone à appeler quels que soient l’heure et le jour
et doivent rester disponibles pendant toute cette période.
Cependant, trois quarts des hémorragies ne nécessitent pas
de reprise chirurgicale.
S. Pierrot a présenté une étude rétrospective menée sur
100 cas consécutifs d’enfants ayant consulté au service d’ur-
gence ORL de l’hôpital Necker-Enfants Malades pour une
hémorragie postamygdalectomie. Il y a un pic de fréquence à
J10 et l’hémorragie la plus tardive est survenue à J16. Dans la
plupart des cas, l’enfant est vu dès les premiers saignements,
mais dans 6 cas il n’est venu que le lendemain, et dans un
cas l’enfant saignait de manière répétée depuis 7 jours ! Au
total, un tiers des enfants ont eu une reprise chirurgicale
pour hémostase. Les arguments pour décider d’une reprise
chirurgicale sont le terrain (cardiopathie), l’abondance ou la
durée de l’hémorragie, l’aspect des loges (saignement actif
ou caillot) et le taux d’hémoglobine. Celle-ci a été faite à
la coagulation bipolaire dans deux tiers des cas, 21 % des
enfants ont eu un ou plusieurs points d’hémostase au fi l
résorbable et 11 %, une ligature de piliers. Près de la moitié
des enfants ont été mis sous antibiotiques et 21 % sous corti-
coïdes. Une supplémentation martiale a été prescrite à un
quart des enfants. Le bilan d’hémostase est peu contributif
pour donner une explication à cette complication.
F. Legent a ensuite parlé des formes graves d’hémorragie per- et
postopératoires. Les décès par hémorragie postamygdalectomie
sont secondaires à des lésions des gros vaisseaux de la région :
palatine ascendante, pharyngienne ascendante, linguale, faciale,
sans oublier les carotides interne et externe qui peuvent avoir
des trajets aberrants. Il a particulièrement insisté sur la ligature
de la carotide externe, technique que la plupart des médecins
ORL possèdent et qui ne nécessite pas de matériel sophis-
tiqué ni de praticiens hyperspécialisés comme la radiologie
interventionnelle. Windfuhr a publié en 2002 25 ligatures de
la carotide externe sur 5 000 amygdalectomies.
PRISE EN CHARGE DE LA DOULEUR
(Table ronde modérée par Rémi Marianowski,
avec Marie-Paule Morisseau-Durand [Boulogne-
Billancourt], Anne-Laure Mansbach [Bruxelles]
et Natacha Teissier [hôpital Robert-Debré, Paris])
L’expression de la douleur dépend de l’âge de l’enfant, de son
apprentissage de la douleur, de sa personnalité, de son milieu

Actualité
Actualité
9
Largeur 176 mm (La Lettre, Le Courrier)
La Lettre d’ORL et de chirurgie cervico-faciale - n° 311 - octobre-décembre 2007
ethno-culturel, et des stratégies pour y faire face. L’évaluation
de la douleur fait appel à des échelles d’auto-évaluation comme
l’EVA, chez les enfants en âge de coopérer, à des échelles d’hé-
téro-évaluation, comme les échelles OPS (Objective Pain Scale,
pour les enfants jusqu’à 2 ans), CHEOPS (Children Hospital
East Ontario Pain Scale) ou l’EVA mesurée par l’infi rmière pour
les enfants plus jeunes. Une enquête récente faite à l’hôpital
Robert-Debré (Paris) sur 48 enfants a montré que 21 avaient
encore mal au bout d’une semaine, pour 7 d’entre eux la douleur
était localisée à l’oreille, 18 ne mangeaient toujours pas bien
et 9 n’avaient pas repris leurs activités habituelles. Pour les
illettrés et les non-francophones il est prévu une “traduction”
de l’ordonnance sous forme de dessins.
L’objectif du traitement est d’obtenir une EVA inférieure à 3/10
et une reprise aussi rapide que possible d’une activité normale.
Cela passe par la prise systématique pendant une durée déter-
minée de diverses médications, une adaptation des traitements
à leur eff et sur l’enfant et une information des parents des eff ets
indésirables de ces médications. Quatre classes de médicaments
ont été étudiées. Les corticoïdes fi gurent parmi les médica-
ments reconnus comme effi caces, sur 8 études ayant rassemblé
626 enfants. Le premier jour, ils diminuent la douleur d’un point
sur l’échelle EVA. Mais le dosage optimal est encore à trouver.
Ils diminuent aussi les vomissements. En cure courte, ils n’ont
pratiquement pas d’eff et indésirable.
Les antibiotiques sont réputés diminuer la douleur, le risque
de septicémie (mais il est déjà si faible…) ainsi que l’halitose,
et accélérer la cicatrisation des loges amygdaliennes. En fait
sur 5 études, ayant rassemblé 345 patients, les eff ets sur la
douleur ne sont pas si nets que cela. Par ailleurs, ils ont des
effets secondaires mineurs très fréquents (rash, nausées,
douleurs abdominales, etc.). Le Conseil supérieur d’hygiène
belge (recommandations pour l’utilisation prophylactique
des antibiotiques en chirurgie 2002) ne les recommande pas
(tout comme la conférence d’experts de la SFAR en France,
en 2006).
Les anesthésiques locaux peropératoires : sur 6 études ayant
rassemblé 284 patients, l’infi ltration d’anesthésiques locaux
facilite la dissection et diminue le saignement postopératoire,
mais n’a pas d’eff et sur la douleur ni sur le recours à des anal-
gésiques supplémentaires. En revanche, quelques accidents
graves ont été décrits.
Les études les plus nombreuses concernent les analgésiques.
Mais les séries sont souvent petites. Ce qu’il y a de sûr c’est
qu’une dose unique est insuffi sante, qu’il faut combiner les
antalgiques de paliers I et II, et que le paracétamol est plus actif
par voie orale (quand l’enfant veut bien le prendre) que par voie
rectale. Les anti-infl ammatoires non stéroïdiens ne sont pas
recommandés dans le doute d’un eff et délétère sur l’hémostase
secondaire. En ce qui concerne les antalgiques de palier II chez
le jeune enfant, le seul autorisé est le Codenfan
®
. La posologie
initiale, récemment rappelée tant par le laboratoire que par
l’Afssaps est de 0,5 mg/kg 4 fois par jour. En cas de douleur
persistante, la posologie peut être augmentée à 0,75 à 1 mg/
kg/prise. La dose maximale ne doit pas dépasser 6 mg/kg/j.
Si la constipation est l’eff et secondaire le plus fréquent, il faut
se méfi er des céphalées secondaires à la codéine (et plus on
donne de Codenfan
®
, moins on soulage les douleurs si ce sont
en fait des céphalées). Par ailleurs, environ 7 % des enfants sont
des métaboliseurs lents ou dépourvus du cytochrome 2D6, et
chez eux le Codenfan
®
est ineffi cace.
Depuis quelques mois, le tramadol (Topalgic gouttes
®
) peut
être prescrit à partir de 3 ans à raison de 4 à 8 gouttes/10 kg
3 à 4 fois par jour. La limite d’utilisation est les nausées qui
peuvent nécessiter l’administration d’ondansetron (Zophren
®
)
ou de métoclopramide (Primpéran
®
). ■
1
/
4
100%