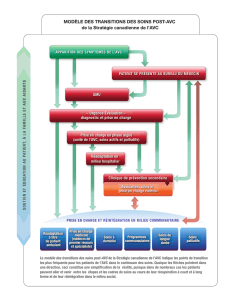
L Quelle place pour le neurologue dans la consultation post-AVC ?

La Lettre du Neurologue • Vol. XVIII - no 3 - mars 2014 | 87
MISE AU POINT
Quelle place
pour le neurologue
dans la consultation post-AVC ?
What role for the neurologist in stroke follow-up?
M. Poli*, I. Sibon*
* Unité neurovasculaire, CHU de
Bordeaux.
L
es accidents vasculaires cérébraux (AVC) repré-
sentent la première cause de handicap acquis
de l’adulte et la deuxième cause de syndrome
démentiel. En dehors de la phase aiguë dédiée à la
mise en place de thérapeutiques d’urgence, la prise
en charge de la pathologie vasculaire cérébrale a pour
objectifs principaux l’identication des mécanismes
étiologiques an d’adapter les stratégies des préven-
tions secondaires et d’apprécier les conséquences des
lésions cérébrovasculaires pouvant interférer dans
la qualité de vie du patient. L’enquête étiologique et
la prise en charge des facteurs de risque vasculaire
reposent sur une étroite collaboration entre neuro-
logues et cardiologues alors que la prise en charge de
certaines séquelles pouvant requérir l’utilisation de
stratégies spéciques de réadaptation − telles que la
spasticité, l’héminégligence ou les troubles vésico-
sphinctériens −, justie une prise en charge spéci-
que dans des structures de médecine physique et
de réadaptation. Le neurologue a un rôle de coordi-
nation entre les différents acteurs, mais possède
aussi une place spécique dans l’évaluation et la prise
en charge thérapeutique de certaines complications,
ce qui implique une organisation spécique de la
consultation neurologique après un AVC.
Qualité de vie et évaluation
du handicap physique
Une première étape indispensable est l’évaluation
de la qualité de vie qui constitue un reflet de
l’inuence d’un éventuel décit séquellaire sur le
mode de fonctionnement des patients dans leur vie
sociale et professionnelle. Il semble évident que la
simple question d’accueil “Comment allez-vous ?”
ne permet pas une analyse able de leur qualité de
vie, et que cette évaluation devrait reposer sur des
données objectives représentées par des échelles
standardisées. L’inconvénient majeur de ces échelles
est souvent représenté par la durée de leur passation.
Dans le contexte de la consultation post-AVC,
l’utilisation de questionnaires simpliés ou d’auto-
questionnaires remplis avant la consultation semble
être une option qui doit être développée (1, 2).
En dehors de cette évaluation globale, la consultation
post-AVC a pour premier objectif de mesurer la qualité
de la récupération du handicap physique dans les
suites de l’événement aigu. Les échelles utilisées
comme le score de Rankin modié ou l’échelle de
Barthel représentent des éléments objectifs indispen-
sables à l’évaluation du retentissement du handicap
dans la vie quotidienne ; elles permettent un suivi au
long cours de l’évolution du patient (3, 4).
La réalisation de ces évaluations globales ne peut
cependant pas sufre à décrire l’état neurologique
du patient, élément qui requiert une évaluation
clinique systématique. Dans le cadre spécifique
de l’évaluation à distance de l’événement aigu,
la place de l’échelle NIHSS (National Institute of
Health Stroke Score) pourrait être discutable en
termes d’apport clinique. En effet, si le score total
permet d’analyser l’évolution du patient depuis la
phase aiguë, il ne permet pas d’évaluer l’ensemble
des séquelles, et même l’analyse indépendante des
différents items n’autorise pas une évaluation ne de
certains paramètres tels que la spasticité, l’apraxie
mélokinétique, la bradykinésie ou les dysesthésies,
qui peuvent pourtant avoir un retentissement majeur
sur la qualité de vie des patients au quotidien.

88 | La Lettre du Neurologue • Vol. XVIII - no 3 - mars 2014
Points forts
»La consultation neurologique post-AVC doit comprendre:
–une évaluation des séquelles physiques et du handicap fonctionnel;
–une évaluation du retentissement cognitif et émotionnel;
–la recherche de récidive d’événements neurologiques focaux;
–la vérification du mécanisme étiologique;
–
l’adaptation des stratégies de prévention secondaire en fonction des objectifs et de la tolérance dechaque
thérapeutique.
Mots-clés
AVC
Handicap
Cognition
Émotions et douleur
Highlights
»
Neurological post-stroke
evaluation should include:
–
An assessment of physical
damage and functional
disability;
–
An assessment of cognitive
and emotional consequences;
–
The research of recurrent
focal neurologic events;
–
Verification of the stroke
mechanism;
–
Adaptation of secondary
prevention strategies based
on objectives and tolerance of
each therapeutic.
Keywords
Stroke
Handicap
Cognition
Emotion and pain
En dehors de l’évaluation du handicap, cette consul-
tation devra s’attacher à identier les différentes
complications neurologiques, émotionnelles et
cognitives pouvant survenir au décours de l’épisode
aigu. L’utilisation d’échelles standardisées, validées
et reproductibles devra être privilégiée pour assurer
le suivi des patients.
Syndromes parkinsoniens
et mouvements anormaux
Peu d’études épidémiologiques se sont intéressées
à évaluer l’incidence des syndromes parkinsoniens
dans les suites d’un événement cérébrovas culaire (5).
Des fréquences variables ont été rapportées en
fonction des dénitions utilisées (6, 7). L’identi-
cation clinique des syndromes parkinsoniens est
souvent compliquée par la coexistence d’un élément
décitaire moteur homolatéral. C’est donc le plus
souvent chez des patients ayant eu une bonne
évolution du décit inaugural qu’il pourra être noté
des éléments bradykinétiques souvent qualiés de
sous-utilisation motrice. Un tremblement de repos
et une hypertonie extrapyramidale sont rarement
observés (8). Le plus souvent, la traduction clinique
de ce syndrome parkinsonien est un trouble de la
marche avec une très nette prédominance de la
bradykinésie aux membres inférieurs et la survenue
de troubles des adaptations posturales (5, 8).
La survenue d’un syndrome parkinsonien uni latéral
dans les suites d’un AVC isolé est exceptionnelle,
il est préférentiellement rencontré dans les lésions
affectant les noyaux gris centraux. En revanche, la
survenue d’un syndrome parkinsonien bilatéral est
plus fréquente, principalement chez les patients
présentant une leucoencéphalopathie vasculaire
étendue (7). Au niveau du diagnostic, une exploration
de type DAT-scan ne peut pas être recommandée de
façon systématique car ces manifestations peuvent
être la conséquence de lésions pré- ou post-synap-
tiques ne permettant pas d’établir de conclusion
formelle (9). Certains travaux récents suggèrent
l’intérêt du 123I-FP-CIT SPECT dans le diagnostic
différentiel avec la maladie de Parkinson (10).
Au niveau thérapeutique, la grande diversité des
lésions cérébrales impliquées dans la survenue de
ces syndromes parkinsoniens rend probablement
compte de la faible réponse habituellement
rapportée à la L-dopa et aux agonistes dopami-
nergiques (10). De plus, le risque de confusion lié
à l’utilisation de ces traitements en limite l’utili-
sation après un AVC. La prise en charge kinésithé-
rapique constitue donc un élément déterminant.
Le bénéce potentiel de la stimulation magnétique
trans crânienne doit, quant à lui, être précisé dans
cette indication (11).
En dehors des syndromes parkinsoniens, les mouve-
ments anormaux hyperkinétiques de type chorée,
athétose, dystonie, astérixis ou myoclonies peuvent
être rencontrés après un AVC. Ces complications
sont rares (1 à 4 % des cas) [7], parfois révélatrices
et survenant le plus souvent dans les premiers jours
post-AVC pour s’amender rapidement. La persistance
ou la survenue tardive de mouvements hyperkiné-
tiques sont donc rares, dominées par les dystonies.
Ces dernières sont favorisées par les lésions du noyau
lenticulaire, plus particulièrement du putamen,
mais peuvent être observées dans les suites de
lésions de localisations diverses (thalamus, noyau
caudé, capsule interne, lésions corticales frontales,
etc.) [12]. La prise en charge thérapeutique repose
le plus souvent sur l’injection de toxine botulique
et, plus exceptionnellement, sur l’utilisation d’anti-
cholinergiques, de benzodiazépines, de neurolep-
tiques ou de tétrabénazine (7, 11).
“Docteur, je suis fatigué…”
Après un AVC, la fatigue est un symptôme rencontré
chez plus de 40 % des patients lors d’une évaluation
à 3 mois (13). Les facteurs de risque sont dominés par
l’existence de maladies chroniques et d’une fatigue
antérieure à l’événement cérébrovasculaire. Bien que
peu étudiée, la localisation lésionnelle pourrait avoir
une inuence spécique. Les infarctus du noyau caudé
sont pour certains plus fréquemment responsables
d’une fatigue post-AVC ce qui fait évoquer le rôle
déterminant des voies sous-cortico-frontales (14).
L’évaluation pourra reposer sur des échelles spéciques
grâce à des auto- ou à des hétéroquestionnaires (15).
Parmi les différents facteurs associés à une augmen-
tation du risque de fatigue post-AVC, H. Naess et

Douleur
neuropathique
Spasticité
Douleur musculo-
squelettique
Douleur d’origine
iatrogène
(statines, etc.)
Syndrome régional
complexe
Douleur
segmentaire
Figure 1. Principales orientations diagnostiques devant des douleurs segmentaires post-
AVC.
La Lettre du Neurologue • Vol. XVIII - no 3 - mars 2014 | 89
MISE AU POINT
al. (16) ont identié le sexe féminin, un antécédent de
dépression et d’infarctus du myocarde, et la présence
d’une leucoencéphalopathie vasculaire étendue. La
fatigue post-AVC peut relever de nombreux facteurs
dominés par la lourdeur du handicap physique, la
présence de douleurs, la survenue de troubles du
sommeil ou l’existence d’un syndrome dépressif.
L’évaluation de ces différents paramètres est un point
déterminant dans la prise en charge thérapeutique
de cette fatigue. Toutefois, la survenue d’une fatigue
isolée peut aussi être rencontrée indépendamment
de ces différents facteurs, y compris chez des patients
ayant présenté un événement transitoire (17). À ce
jour, aucune prise en charge spécique ne peut être
proposée (18).
Douleurs
De mécanismes multiples, elles sont présentes chez
11 à 55 % des patients selon les études (figure 1)
[19]. Les douleurs d’origine musculo-squelettique
représentent le mécanisme le plus fréquent ; elles
sont dominées par des épaules douloureuses et
sont parfois favorisées par le développement d’une
spasticité. Les douleurs chroniques d’origine centrale
seraient pour leur part présentes chez 1 à 12 % des
patients. Ces douleurs − souvent associées à des
dysesthésies − se caractérisent cliniquement par
leur survenue spontanée ou provoquée, une distri-
bution variable pouvant être focale (péri-orbitaire,
segment de membre) ou diffuse. Elles s’accom-
pagnent d’une anomalie de l’examen clinique dans
90 % des cas. L’utilisation systématique d’échelles
de type DN4 dans le suivi post-AVC pourrait
permettre leur meilleure identication. La survenue
de douleurs neuropathiques fait le plus souvent
suite à la présence de lésions localisées dans le tronc
cérébral (syndrome de Wallenberg), le thalamus,
ou, plus rarement, de lésions corticales (20). Dans
un travail récent, T. Sprenger et al. ont identié un
risque de survenue plus important lors de lésions
du pulvinar (21). La prise en charge thérapeutique
de ces manifestations douloureuses reste difcile
et bien que des facteurs prédictifs aient pu être
identiés, aucune thérapeutique prophylactique n’a,
à ce jour, démontré un bénéce quelconque (22).
Dans le cadre spécique des douleurs neuropa-
thiques post-AVC, peu d’essais randomisés ont été
menés. Par analogie aux douleurs neuropathiques
d’une autre origine, les tricycliques ou inhibiteurs
spéciques de la recapture mixte (sérotoninergique
et noradrénergique) sont fréquemment utilisés.
La place des antiépileptiques dans la prise en charge
des douleurs post-AVC reste encore incertaine (22).
Dans les rares essais randomisés menés, le lévéti-
racétam (3 g/j) et la prégabaline (150 à 600 mg/j)
n’ont pas pu démontrer leur efcacité (23, 24).
Une étude a suggéré l’efficacité potentielle du
zonisamide (200 mg/j) dans les douleurs thala-
miques (25). Par ailleurs, la place respective de la
gabapentine, du topiramate ou de la lamotrigine
parfois utilisés reste encore indéterminée dans cette
indication (26). En dehors des stratégies médica-
menteuses, des prises en charge interventionnelles
telles que la stimulation du cortex moteur ou du
thalamus sont actuellement en cours d’évaluation
dans le cadre de douleurs pharmacorésistantes (27).
Troubles du sommeil
La présence de troubles du sommeil (figure 2, p. 90),
d’origine multifactorielle, contribue à la persistance
d’une fatigue post-AVC ainsi qu’à une altération des
capacités de récupération. Leur dépistage est donc
une étape déterminante de la prise en charge. L’une
des principales causes d’une altération du sommeil
réside dans la présence de syndromes apnéiques.
Ainsi, plus de 60 % des patients victimes d’un
AVC seraient affectés par un syndrome d’apnées
obstructives du sommeil (28). Leur dépistage est
fondamental car leur prise en charge permet une
optimisation de la prévention secondaire au travers

Syndrome
anxiodépressif
Pathologie
du sommeil :
SAOS, SJSR, MPS
Iatrogène
(β-bloquant,
antiépileptique, etc.)
Douleur
Trouble
du sommeil
MPS : mouvements périodiques du sommeil ; SAOS : syndrome d’apnées obstructives du sommeil ;
SJSR : syndrome des jambes sans repos.
Figure 2. Principales orientations diagnostiques devant des troubles du sommeil post-AVC.
90 | La Lettre du Neurologue • Vol. XVIII - no 3 - mars 2014
Quelle place pourleneurologue danslaconsultation post-AVC ?
MISE AU POINT
notamment d’un meilleur contrôle de la tension
artérielle. Dans les suites d’un AVC, il importe de
distinguer les apnées centrales des apnées obstruc-
tives. Les échelles de Berlin et d’Epworth permettent
d’évaluer le niveau de risque des patients ainsi que le
retentissement du syndrome apnéique. Néanmoins,
la sensibilité très modérée de ces évaluations à la
détection du syndrome apnéique et leur absence de
discrimination entre apnées centrales et obstructives
devra laisser une large place à la réalisation d’une
polysomnographie ou d’une simple polygraphie (29).
En dehors du syndrome d’apnées obstructives du
sommeil, la survenue d’un syndrome des jambes
sans repos et de mouvements périodiques pendant
le sommeil a été rapportée chez 12 % des patients
1 mois après un AVC (30). Ils seraient favorisés par la
présence de lésions des ganglions de la base et de la voie
pyramidale et altéreraient le pronostic fonctionnel (31).
Aucune donnée de la littérature ne permet, à ce jour,
de préciser la stratégie thérapeutique optimale à
recommander chez ces patients, et le bénéce des
agonistes dopaminergiques reste à préciser. En outre,
toute carence martiale potentiellement liée à un
traitement antithrombotique doit être recherchée.
Enfin, les troubles du sommeil peuvent être la
conséquence directe d’éléments douloureux ou d’un
syndrome anxiodépressif qu’il convient d’identier
précocement.
Manifestations psychiatriques
Elles peuvent revêtir des expressions cliniques
variées à type de syndrome dépressif et anxieux,
de syndrome de stress post-traumatique ou, plus
rarement, d’état maniaque. La dépression post-AVC
affecte plus de 30 % des patients à 3 mois. Les
principaux facteurs prédictifs cliniques sont les
antécédents de dépression, le sexe féminin, l’iso-
lement social, la sévérité du handicap, l’aphasie et
l’intensité du syndrome anxieux à la phase précoce
de l’AVC (32). Au niveau neuroradiologique, les
lésions hémisphériques gauches et affectant les
boucles sous-cortico-frontales seraient plus à
même de favoriser la survenue d’une dépression
après un AVC (33, 34). De même, l’étendue de
la leucoencéphalopathie vasculaire constitue
un cofacteur probable augmentant le risque de
survenue d’une dépression (35). La dépression a une
inuence négative sur la récupération fonctionnelle
et le pronostic des patients, justiant son dépistage
précoce et sa prise en charge thérapeutique. De
nombreuses échelles peuvent être utilisées pour
évaluer l’intensité du syndrome dépressif (Beck,
MADRS [Montgomery and Asberg Depression Rating
Scale], HAD [Hospital Anxiety and Depression Scale],
HDRS [Hamilton Depression Rating Scale], etc.),
toutes partageant une sensibilité équivalente. Au
niveau thérapeutique, la lutte contre l’isolement
social et le soutien familial sont 2 éléments déter-
minants auxquels pourront être associées une
psychothérapie de type thérapie par résolution
de problème ou cognitivocomportementale et une
prise en charge pharmacologique. Bien que n’ayant
pas fait l’objet d’essais randomisés spéciques de
grande taille, le bénéce des antidépresseurs de type
tricyclique, inhibiteurs spéciques de la recapture
de la sérotonine (ISRS) et inhibiteurs spéciques de
la recapture de la noradrénaline (ISRNA) est actuel-
lement admis (36, 37). Par ailleurs, dans les formes
pharmacorésistantes, l’électroconvulsivothérapie et
la stimulation magnétique transcrânienne peuvent
être proposées dans des cas spéciques (38).
Et l’apathie…
Présente chez 20 à 40 % des patients 3 mois après
un AVC, elle est fréquemment associée à la présence
d’un syndrome dépressif. Néanmoins, elle peut être
présente de façon isolée et constituer un facteur
indépendant de mauvais pronostic (33). Encore
méconnus, les facteurs de risque sont incertains,
mais les récents travaux de W.K. Tang et al. (39)
suggèrent l’inuence des lésions du tronc cérébral,
possiblement au travers d’une dysfonction des
noyaux pédiculopontin et du raphé. Par ailleurs,
l’identification d’une hypoperfusion des noyaux

Syndrome
anxiodépressif
Pathologie
du sommeil : SAOS
Mécanisme iatrogène
(antidépresseur,
antiépileptique,
anxiolytiques, etc.)
Syndrome
démentiel
vasculaire ou mixte
Trouble
cognitif
Figure 3. Principales orientations diagnostiques devant des troubles cognitifs post-AVC.
La Lettre du Neurologue • Vol. XVIII - no 3 - mars 2014 | 91
MISE AU POINT
gris centraux suggère l’inuence de l’altération des
boucles cortico-sous-corticales frontales dans l’émer-
gence de ce syndrome (40). L’évaluation clinique est
effectuée grâce à des échelles spéciques telles que
la LARS (Lille Apathy Rating Scale) ou l’inventaire
d’apathie. Au niveau thérapeutique, K. Mikami et
al. (41) ont récemment identié le bénéce potentiel
du citalopram et de la thérapie par résolution de
problème sur la prévention du syndrome apathique
post-AVC. Ce résultat renforce l’hypothèse d’un lien
étroit entre la survenue d’une dépression post-AVC
et le syndrome apathique. Le bénéce potentiel des
agonistes dopaminergiques, des anticholinestérasiques
et des psychostimulants a été évoqué mais demeure
à ce jour indéterminé. Par ailleurs, l’apathie, comme
la dépression, pourrait constituer une expression
clinique précoce de troubles cognitifs vasculaires.
Leur survenue justie donc une surveillance accrue
de l’évolution cognitive après un AVC (42).
Troubles cognitifs
La fréquence des troubles cognitifs non démentiels
(figure 3) est extrêmement importante dans les
suites d’un infarctus cérébral. A. Jaillard et al. (43)
rapportent ainsi sur une série de 177 patients que
91,5 % des sujets ont une altération dans au moins
un domaine cognitif, l’atteinte la plus fréquente
concernant la mémoire de travail. Ces désordres
cognitifs, souvent apparents uniquement lors de la
réalisation de batteries cognitives spéciques, sont
pour autant susceptibles d’altérer la qualité de vie
des patients et, pour les plus jeunes, de constituer
un facteur limitant à la reprise d’une activité profes-
sionnelle. À l’inverse, la présence d’un syndrome
démentiel dans l’année qui suit la survenue d’un AVC
indépendamment d’un syndrome démentiel antérieur
serait d’environ 7 % (44). Ces troubles cognitifs sont
rarement la conséquence d’une lésion dans un site
stratégique (par exemple, le thalamus) et sont plus
souvent observés au cours des états multilacu-
naires ou lors d’infarctus corticaux multiples. Outre
la localisation de la lésion cérébro-vasculaire, les
principaux facteurs de risque clinique de détérioration
cognitive sont le sexe féminin, l’âge avancé, le faible
niveau d’éducation, l’existence d’une détérioration
cognitive antérieure à l’AVC (pouvant être évaluée
par l’IQ-code) et la présence d’une brillation (44).
L’inuence des facteurs de risque cardiovasculaire
est également déterminante, le risque s’accroissant
de façon notable avec l’augmentation de leur
nombre (Allan, 2011). Par ailleurs, l’existence d’une
leucoencéphalopathie étendue et d’une atrophie
corticale, notamment médio-temporale, consti-
tuent des facteurs de risque de déclin cognitif (44).
Le dépistage de ces troubles cognitifs repose au mieux
sur la réalisation d’un bilan neuropsychologique et
au minimum sur une batterie d’évaluation rapide
de type MOCA (Montreal Cognitive Assessment) ou
MMSE (Mini-Mental State Examination). La prise en
charge thérapeutique pharmacologique reste à ce
jour décevante, les inhibiteurs de l’acétylcholines-
térase n’ayant pas démontré un effet signicatif. La
prévention des facteurs de risque cardiovasculaire
et notamment de l’hypertension semble donc être
la meilleure option de prévention et de limitation de
l’aggravation de ces troubles cognitifs (45).
Évaluation des récidives
d’événements neurologiques
focaux
La recherche de survenue d’événements neuro-
logiques représente une étape majeure de la consul-
tation post-AVC (figure 4, p. 92). La description
par le patient de symptômes productifs (pares-
thésies, clonies, hallucinations, etc.) doit faire
évoquer la possibilité d’une épilepsie vasculaire.
Cette complication affecte 2,5 à 10 % des patients
à 5 ans. Les facteurs prédictifs les plus associés sont
représentés par un NIHSS élevé, l’existence d’un
syndrome démentiel antérieur à l’AVC et la survenue
de crises précoces. Les crises comitiales sont plus
fréquemment observées dans les infarctus multiples
et les hémorragies intracérébrales affectant le cortex
frontal (46). À ce jour, il n’existe pas de bénéce
démontré de l’introduction d’un traitement
 6
6
1
/
6
100%