Fiche outils

Rappels :
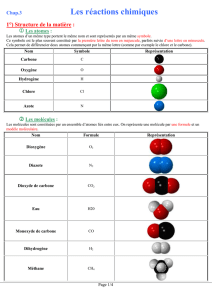
Formules d’espèces chimiques
Niveau
3ème
Thème
Corps et Santé
Chapitre n°1 : Des espèces chimiques pour soigner
Compétences travaillées
PRATIQUER DES
LANGAGES
1S
Passer d'une forme de langage
scientifique à une autre
Objectif de formation
Organisation et transformations de la matière
Attendus de fin de cycle
Décrire et expliquer les transformations chimiques
Connaissances et
Capacités
Notion de molécules, atomes.
Associer leurs symboles aux éléments à l’aide de la classification périodique.
Interpréter une formule chimique en termes atomiques.
Description de l’activité
Rappels de notions vues en 4ème pour pouvoir introduire les ions dans la prochaine
activité.
Type d’activité
Mobilisation de connaissances antérieures
Travail réalisé par les
élèves
Revoir la composition de la matière.
Retrouver les éléments les plus courants dans la classification périodique.
Trouver la composition en terme atomiques d’une molécule à partir d’une formule.
Trouver la formule d’une molécule à partir de la composition ou du modèle.
Pré-requis
Notion de molécules et d’atomes (vu en 4ème)
Institutionnalisation
Durée
30 min
Matériel
Modèle moléculaire

Corps et Santé – Chapitre n°1
RAPPELS : Formules d’espèces chimiques
Max a un devoir à faire sur les formules des espèces chimiques. Il réfléchit :
A toi de l’aider à répondre aux questions suivantes :
1. Comment appelle-t-on les particules qui constituent une molécule ?
2. Compléter le tableau ci-dessous regroupant les éléments les plus couramment rencontrés dans les
espèces chimiques :
3. L’éthanol peut être utilisé comme antiseptique. La formule chimique de cette molécule est C2H6O.
La composition atomique d’une molécule d’éthanol est :
□ 1 atome de carbone + 2 atomes d’hydrogène + 6 atomes d’oxygène
□ 2 atomes de carbone + 6 atomes d’hydrogène
□ 2 atomes de carbone + 6 atomes d’hydrogène + 1 atome d’oxygène
□ 2 atomes de carbone + 6 atomes d’hydrogène + 6 atomes d’oxygène
4. Donner la composition de la molécule d’acide acétylsalicylique (anti-inflammatoire) sachant que sa
formule est : C9H8O4.
5. La molécule d’acide ascorbique que l’on trouve dans la vitamine C contient 6 atomes de carbone, 8
atomes d’hydrogène et 6 atomes d’oxygène. Donner sa formule.
6. Voici la modélisation d’une molécule de protoxyde d’azote (gaz utilisé comme anestésiant en bloc
opératoire) :
Donner sa formule.
Elément
Carbone
Hydrogène
Oxygène
Azote
Position dans la
classification périodique
Symbole
Représentation
de l’atome
Une espèce chimique est un corps pur.
Elle doit donc être constituée de molécules identiques !
La formule d’une espèce chimique est donc la formule
des molécules qui la constitue.
1
/
2
100%