Lire l'article complet

Images en Dermatologie • Vol. II • n° 2 • avril-mai-juin 2009
63
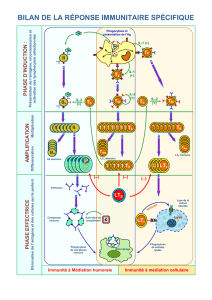
Figure 1. Manifestations systémiques associées à l’interleukine-1b
(d’après Dinarello [2]).
Thérapeutique
L’anakinra (Kineret®) : indications en dermatologie
Anakinra (Kineret®): its use in dermatology
N. Kluger1, B. Fautrel2
(1 Service de dermatologie, hôpital Saint-Éloi, CHU de Montpellier ; 2 UFR de médecine, Paris-VI ; service de rhumatologie,
groupe hospitalier Pitié-Salpêtrière, AP-HP, Paris)
Mots-clés : Anakinra • IL-1 • Infl ammasome • Inhibiteur de l’IL-1
• Syndrome auto-inflammatoire héréditaire • Syndrome de
Schnitzler
Keywords: Anakinra • IL-1 • Infl ammasome • IL-1 inhibitor • Here-
ditary auto-infl ammatory syndrome • Schnitzler syndrome
L’ anakinra (Kineret®) est un inhibiteur sélectif du
récepteur de l’interleukine-1 (IL-1). Il a été développé
initialement par les laboratoires Amgen (1). L’anakinra
fait partie de l’arsenal des biothérapies au même titre
que les anti-TNFα ou les anti-intégrines. Son mode d’ac-
tion est original car il bloque la voie de l’IL-1, cytokine-clé
de l’infl ammation et de l’immunité innée (2-5).
L’anakinra a actuellement l’AMM en France uniquement dans le
traitement de la polyarthrite rhumatoïde en association avec le
méthotrexate, chez les patients dont la réponse au méthotrexate
seul n’est pas satisfaisante. Cependant, plusieurs études et cas
cliniques isolés ont clairement montré que l’anakinra avait un
intérêt très clair dans un certain nombre de pathologies in am-
matoires certes rares, mais réputées dif ciles à traiter, et ce
avec une ef cacité spectaculaire. Ces dernières concernent de
près les dermatologues : les syndromes auto-in ammatoires
héréditaires, la maladie de Still de l’adulte et de l’enfant et,
plus récemment, le syndrome de Schnitzler, la polychondrite
atrophiante et certaines dermatoses neutrophiliques.
L’interleukine-1 et l’infl ammation
L’in ammation est un mécanisme homéostatique important
qui limite les effets délétères des agents infectieux. L’IL-1
représente la cytokine pro-in ammatoire clé intervenant dans
l’immunité innée. Elle est produite par les macrophages, les
monocytes, les cellules dendritiques, les broblastes et les
cellules épithéliales. L’IL-1 est habituellement produite en
réponse à une infection, un traumatisme ou une stimulation
immune. Il s’agit du prototype même de la cytokine disposant
d’une action pléiotrope seule ou en combinaison avec d’autres
cytokines sur un grand nombre de types cellulaires de l’or-
ganisme.
La famille de l’IL-1 comprend actuellement 11 ligands
(4)
dont
IL-1α et IL-1β
(fi gure 1)
qui se lient au même récepteur, mais
aussi l’antagoniste des récepteurs de IL-1 (IL-1Ra), IL-18, IL-33
et d’autres membres caractérisés par la conservation d’homo-
logies de séquences d’acides aminés. IL-1α et IL-1β sont toutes
les deux sécrétées sous la forme de précurseurs pro-IL-1α et
pro-IL-1β (35 kDa), qui sont ensuite clivés respectivement par
les protéases calpaïnes et caspase I en formes matures IL-1α
et IL-1β (17 kDa). La principale différence est que la pro-IL-1α
est active contrairement au pro-IL-1β. L’IL-1Ra se lie au même
récepteur que l’IL-1α et IL-1β sans induire de réponse intracel-
lulaire et agit donc comme un inhibiteur naturel de l’IL-1
(4)
.
La famille des récepteurs de IL-1 (IL-1R) comprend 10 membres
dont IL-1RI, IL-1RII et la protéine accessoire de IL-1R (IL-1RacP)
[fi gure 2]
. IL-1 se xe à ces 3 récepteurs ou à leurs formes
solubles. IL-1RI est capable de transduire les signaux activa-
teurs et de favoriser la réponse in ammatoire par opposition
à IL-1RII, qui n’a aucune activité de transduction du signal
et fonctionne comme un inhibiteur naturel de la forme IL-1β.
Par ailleurs, IL-1Rα a la plus grande af nité pour IL-1RI. De la
même façon, IL-1RacP favorise la xation de IL-1 sur la forme
soluble d’IL-1RII
(4)
.

Images en Dermatologie • Vol. II • n° 2 • avril-mai-juin 2009
64
Figure 2. IL-1, ses récepteurs (IL-1RI et II) et son antagoniste (IL-1Ra)
(d’après Chauffi er et al [6]).
Cellule
productrice
d'IL-1
Procaspase 1
Caspase 1 Clivage
icIL-1α
mIL-1α
s IL-1β
Pro-IL-1β
sIL-1RII
IL-1RII IL-1RI IL-1RI
icIL-1Ra
Il-1Ra
Transduction
du signal
–
––
+
Thérapeutique
Une fois sécrétée, l’IL-1 entre dans la circulation et stimule les
récepteurs centraux hypothalamiques vasculaires, entraînant
la synthèse de cyclo-oxygénase-2, elle-même responsable
d’une élévation de prostaglandine E2 activant le centre ther-
morégulateur et la èvre.
En périphérie, l’IL-1 active des récepteurs endothéliaux respon-
sables d’une éruption cutanée et de la production d’IL-6.
L’IL-6 circulante stimule les hépatocytes pour synthétiser des
protéines de l’in ammation aiguë (protéine C réactive, brino-
gène, etc.) et augmente également la vitesse de sédimentation.
L’IL-1 agit sur la moelle osseuse en stimulant la myélopoïèse,
ce qui conduit à une neutrophilie circulante. L’IL-6 stimule la
thrombopoïèse. En n, l’IL-1 diminue la sécrétion d’érythro-
poïétine et elle est donc responsable de l’anémie observée en
cas d’in ammation chronique
(2) [fi gure 2].
L’IL-1 est également responsable de l’adhésion et de la migra-
tion des cellules de l’in ammation via les molécules d’adhésion
VCAM-1 et ICAM-1 des cellules endothéliales, de la prolifération
et la différenciation des lymphocytes B et T, des macrophages
et des cellules
Natural Killers
ainsi que de la différenciation des
lymphocytes T en Th17 (lymphocytes producteurs d’IL-17)
[6]
.
L’antagoniste naturel du récepteur de l’IL-1
et l’anakinra
Les inhibiteurs de l’IL-1 se lient de façon compétitive au récep-
teur de l’IL-1 : IL-1Ra
(IL-1 receptor antagonist)
. Une forme
soluble (soluble IL-1Ra) est produite par différents types cellu-
laires (polynucléaires neutrophiles, broblastes, etc.). Cette
production est inductible avec n’importe quel type cellulaire.
Quatre membres de cette famille d’antagonistes ont été décrits :
une forme soluble et trois formes intracellulaires. L’anakinra
est un antagoniste recombinant non glycosylé humain soluble
des récepteurs de l’IL-1 (anti-IL-1R). Le rôle de ces antago-
nistes dans la genèse de rhumatismes in ammatoires a été
montré par des modèles expérimentaux de souris délétées
pour toutes les isoformes de l’IL-1Ra. De plus, le rôle de la
balance dans la modulation de la réponse in ammatoire IL-1β/
IL-1Ra est mise en évidence dans les synoviales de patients
présentant une polyarthrite rhumatoïde
(4)
.
La polyarthrite rhumatoïde :
une indication décevante de l’anakinra
(7)
L’IL-1 est présente dans le plasma et le liquide synovial des
patients atteints de polyarthrite rhumatoïde et une corrélation
a été rapportée entre les concentrations plasmatiques d’IL-1 et
l’activité de la maladie. L’anakinra inhibe les réponses induites
par l’IL-1 in vitro, y compris la production de monoxyde d’azote
et de prostaglandine E
2
et/ou celle de collagénase par les
cellules synoviales, les broblastes et les chondrocytes. L’ana-
kinra a actuellement l’AMM dans l’unique indication suivante : le
traitement de la polyarthrite rhumatoïde en association avec le
méthotrexate, chez les patients dont la réponse au méthotrexate
seul n’est pas satisfaisante. Pourtant, cette molécule est peu
utilisée dans cette indication. En effet, il apparaît moins ef cace
que les anti-TNFα dans cette indication rhumatologique. De
plus, la nécessité des injections quotidiennes et le coût élevé
du traitement (12 000 euros par an), sensiblement équivalent
à celui des autres biothérapies, constituent des limites non
négligeables de ce traitement lorsqu’on le compare aux autres
traitements biologiques, notamment par anti-TNFα
(6)
.
Maladie de Still de l’adulte et forme systémique
des arthrites juvéniles idiopathiques
Plusieurs études ont montré une ef cacité spectaculaire de
l’anakinra dans des formes réfractaires de maladie de Still
de l’adulte (MSA) ainsi que dans son équivalent pédiatrique,
l’arthrite juvénile systémique idiopathique (sAJI), respective-
ment aux doses de 100 mg/j et de 1 à 2 mg/kg/j
(8-13)
. Des
arguments expérimentaux plaident pour une dysrégulation de
la voie de l’IL-1β dans la pathogénie de la MSA et de l’sAJI
(2, 5)
.
Aucune mutation de la régulation de l’IL-1β n’a été identi ée
dans la sAJI pour le moment
(5)
. Néanmoins, la régulation de
la voie de l’IL-1β étant extrêmement ne, une dysrégulation au
niveau aussi bien de la production que de la dégradation ou de
l’inhibition pourrait être responsable de la sAJI. Par ailleurs,
l’IL-18 est élevée dans la sJIA sans que l’on sache actuellement
s’il s’agit d’une cause ou d’une conséquence dans la physiopa-
thogénie. L’IL-18 est également élevée dans la MSA
(5)
. Ainsi,
certains auteurs ont-ils proposé de rattacher ces pathologies
au groupe des syndromes auto-in ammatoires plutôt qu’à celui
des maladies auto-immunes.

Images en Dermatologie • Vol. II • n° 2 • avril-mai-juin 2009
65
Thérapeutique
Les syndromes auto-infl ammatoires
héréditaires
Les syndromes auto-in ammatoires (ou èvres récurrentes
héréditaires) sont des maladies génétiques rares caractérisées
par l’apparition soudaine d’épisodes in ammatoires avec des
épisodes de èvre récidivants
(6,14,15)
. Les manifestations
cliniques, l’âge de début et l’évolution permettent de poser le
diagnostic du syndrome. Une meilleure compréhension de la
physiopathogénie et de la génétique a permis de mieux classer
ces maladies. Actuellement, on dénombre au moins 7 maladies
bien déterminées :
– la èvre méditerranéenne familiale (ou maladie périodique,
FMF, MIM 249100) est caractérisée par une mutation de la
pyrine, protéine qui inhibe la caspase 1 (qui elle-même trans-
forme la pro-IL-1β en forme active). Il résulte de l’inactivation
de la pyrine une activation non contrôlée de l’IL-1 ;
– le syndrome périodique associé au récepteur du TNF (TNF
receptor associated periodic syndrom
, TRAPS, MIM 142680)
est la conséquence d’une mutation du gène codant pour le
récepteur 1 du TNFα. Le récepteur ainsi modi é n’est plus
clivé et il est libéré sous forme soluble pour xer (et inhiber)
le TNFα circulant ;
– le syndrome hyper-IgD (HIDS, MIM 260920) est dû à une
mutation du gène de la mévalonate kinase. La physiopatho-
génie du HIDS n’est pas encore bien comprise ;
– le syndrome acné-arthrite pyogène-
Pyoderma gangrenosum
(syndrome PAPA, MIM 604416) est lié à une mutation de la
CD2
binding protein 1
qui entraîne l’augmentation de son interaction
avec la pyrine et sa séquestration. Il existe encore une fois une
levée d’inhibition de la production de l’IL-1 ;
– les èvres périodiques associées aux mutations du gène CIAS1/
NALP3 (CIAS1 pour
Cold induced auto-in ammatory syndrome 1
).
Ces èvres périodiques sont aussi dénommées “cryo-pyrino-
pathies” (car la mutation du CIAS1 code pour une protéine, la
cryopyrine). Ce groupe comprend trois maladies qui doivent
être actuellement considérées comme des variants cliniques
d’une même entité : une forme “modérée”, l’urticaire familial
au froid (MIM 120100), une forme “intermédiaire”, le syndrome
de Muckle-Wells (MIM 191900), et une forme “sévère”, le CINCA/
NOMID (
chronic infantile neurological cutaneous and articular/
neonatal-onset multisystemic inflammatory disease
, MIM
607115). Les cryopyrinopathies résultent de la mutation de la
cryopyrine qui active la caspase 1 et la production d’IL-1β active.
La cryopyrine est une protéine de la superfamille des protéines
avec un domaine dit “de mort”
(death domain)
. Elle participe avec
Tableau. Caractéristiques des principaux syndromes auto-infl ammatoires héréditaires (6,14,15).
FMF TRAPS HIDS PAPA FCAS MW CINCA/NOMID
Transmission AR AD AR AD AD AD De novo ou AD
Gène MEFV TNFRSF1A MVK CD2BP1/PSTPIPI CIAS1 CIAS1 CIAS1
Produit
du gène Pyrine/
marénostrine Récepteur au
TNF 1 Mévalonate
kinase CD2BP1/PSTPIPI Cryopyrine
(NALP3) Cryopyrine
(NALP3) Cryopyrine
(NALP3)
Durée
de la poussée 1-3 jours
Début vers l’âge de
20 ans
7-21 jours,
6 épisodes/an
environ
3-7 jours,
toutes les 4
à 8 semaines
Variable < 12-24 h 1-2 jours Constant
Atteinte
cutanée Pseudo-érysipèle ;
érythème acral ;
urticaire atypique ;
purpura
rhumatoïde ;
purpura non
spécifi que
Macules et papules
migratrices
intermittentes en
regard des zones
de myalgies ;
plaques
œdémateuses ;
purpura
Éruption
morbiliforme
intermittente ;
Ulcères
buccaux/
génitaux
Acné sévère ;
Pyoderma
gangrenosum
Urticaire
atypique induit
par le froid
Urticaire
atypique
quotidien
depuis la
naissance
Urticaire atypique
quotidien
depuis la naissance
Atteinte
digestive Fréquente Oui Fréquente Non Non Non Rare
Amylose Fréquente Oui (10 %) Très rare Non Non Oui (25 %) Possible
Atteinte
articulaire Arthrite (50-75 %) Arthrite rare Arthrite rare Arthrite pyogène
aseptique Arthralgies Arthralgies Arthropathies
déformantes
Autres Péritonite, pleurésie,
pleurite, méningite,
myalgies
Pleurésie ;
myalgies
migratrices
Adénopathies Surdité neuro-
sensorielle ;
conjonctivite
Méningite aseptique,
œdème papillaire ;
retard mental
Traitements
conventionnels Colchicine Colchicine à fortes
doses; anti-TNF Corticoïdes,
AINS, statines,
anti-TNF
Corticoïdes,
anti-TNF Corticoïdes,
éviction du froid AINS,
corticoïdes,
anti-TNF,
thalidomide
Corticoides,
immunosuppresseurs,
anti-TNF
AR : transmission autosomique récessive ; AD : transmission autosomique dominante.

Images en Dermatologie • Vol. II • n° 2 • avril-mai-juin 2009
66
Thérapeutique
d’autres molécules de la même famille pour former un complexe
macromoléculaire, l’in ammasome impliqué dans l’activation de
l’IL-1β et de l’IL-18 ainsi qu’une régulation positive de NF-κB,
qui augmente l’expression du gène IL-1. La fonction précise
de la cryopyrine est d’associer des molécules de caspase-1
ensemble, association qui active ces dernières.
Les syndromes auto-inflammatoires diffèrent des maladies
auto-immunes en raison de l’absence d’anticorps circulants ou
de lymphocytes auto-réactifs à un antigène donné. Les syndromes
auto-in ammatoires sont la conséquence d’une régulation anor-
male des cytokines pro-in ammatoires avec une activation perma-
nente de l’in ammation en l’absence de processus infectieux
patent. Ces syndromes présentent des caractéristiques cliniques
communes : èvre, éruption cutanée, arthralgies, troubles neuro-
logiques, possibilité d’amylose et anomalies hématologiques. Les
principales caractéristiques des syndromes auto-in ammatoires
sont résumées dans le
tableau, p. 65
. L’anakinra a fait preuve de
son ef cacité dans tous ces syndromes
(6, 16)
.
Le syndrome de Schnitzler
L’anakinra a connu un regain d’intérêt en dermatologie ces
dernières années à la suite de la publication par Martínez-Taboada
et al. en 2005 de résultats témoignant de l’ef cacité spectaculaire
de ce traitement dans le syndrome de Schnitzler connu pourtant
pour être extrêmement dif cile à traiter
(17)
. Très rapidement, près
d’une quinzaine de cas similaires ont suivi, démontrant l’ef cacité
du traitement dans les 24 heures après sa mise en route
(18-20)
.
Cependant, ce traitement s’avère être suspensif puisque des réci-
dives sont notées rapidement après l’arrêt du traitement
(20)
.
L’IL-1 semble avoir un rôle important dans ce syndrome (taux
élevés dans le sang, corrélation du taux à la rémission)
[21],
à tel
point que certains considèrent le syndrome de Schnitzler comme
apparenté aux syndromes auto-in ammatoires
(19, 22)
. Pour
certains, l’anakinra pourrait être proposé rapidement en alterna-
tive à la corticothérapie systémique en cas d’échec
(19)
. Il n’existe
à ce jour aucun échappement rapporté sous traitement.
Vers de nouvelles indications ?
L’anakinra a été essayé de façon plus anecdotique, mais avec
une ef cacité toujours aussi spectaculaire dans d’autres indi-
cations où une résistance à plusieurs lignes de traitement était
observée : le syndrome de Sweet
(23)
, la polychondrite chro-
nique atrophiante
(6, 24, 25)
ou la maladie de Behçet
(26)
.
Conclusion
Si l’anakinra a “déçu” dans l’indication de la polyarthrite rhuma-
toïde, il a trouvé un créneau dans le traitement des syndromes
auto-in ammatoires où la voie de l’IL-1 occupe une place
centrale dans la physiopathogénie.
L’anakinra constitue le premier traitement de sa classe théra-
peutique. Néanmoins, les principaux écueils restent le prix et la
nécessité d’injections quotidiennes avec une récidive à l’arrêt
du traitement. Par ailleurs, seuls les rhumatologues et les
internistes sont habilités à prescrire ce traitement.
Il existe d’autres stratégies thérapeutiques visant à bloquer
la voie de l’IL-1
(4)
: des récepteurs solubles comme le récep-
teur soluble de l’IL-1 (sIL-1R1) ou l’IL-1 trap, une protéine de
fusion xant l’IL-1α et IL-1β avec une plus grande af nité. Ainsi,
récemment, le rilonacept (IL-1 trap) a fait la preuve de son
ef cacité dans les cryopyrinopathies et a obtenu l’accord de
la FDA dans cette indication
(27-30)
. L’inhibition de la produc-
tion de l’IL-1β est une autre voie de développement comme le
pralnacasan, un inhibiteur de la caspase 1. D’autres compa-
gnies pharmaceutiques développent d’autres antagonistes du
récepteur de la IL-1, des anticorps anti-IL-RI, des inhibiteurs
de la signalisation de IL-1.
La première génération d’inhibiteurs de l’IL-1 devrait donc
laisser place à des nouvelles molécules inhibitrices plus
ef caces.
II
Références bibliographiques
1.
http://www.kineretrx.com/
2.
Dinarello CA. Blocking IL-1 in systemic inflammation. J Exp Med
2005;201(9):1355-9.
3.
Dinarello CA. The many worlds of reducing interleukin-1. Arthritis Rheum
2005;52(7):1960-7.
4.
Burger D, Dayer JM, Palmer G, Gabay C. Is IL-1 a good therapeutic target in
the treatment of arthritis? Best Pract Res Clin Rheumatol 2006;20(5):879-96.
5.
Church LD, Cook GP, McDermott MF. Primer: inflammasomes and
interleukin 1 beta in inflammatory disorders. Nat Clin Pract Rheumatol
2008;4(1):34-42.
6.
Chauf er K, London J, Beaudouin C, Fautrel B. Indications de l’anakinra.
Presse Med 2009;38(5):799-807.
7.
Furst DE. Anakinra: review of recombinant human interleukin-I receptor anta-
gonist in the treatment of rheumatoid arthritis. Clin Ther 2004;26(12):1960-75.
8.
Verbsky JW, White AJ. Effective use of the recombinant interleukin 1
receptor antagonist anakinra in therapy resistant systemic onset juvenile
rheumatoid arthritis. J Rheumatol 2004;31(10):2071-5.
9.
Pascual V, Allantaz F, Arce E, Punaro M, Banchereau J. Role of interleukin-1
(IL-1) in the pathogenesis of systemic onset juvenile idiopathic arthritis and
clinical response to IL-1 blockade. J Exp Med 2005;201(9):1479-86.
10.
Fitzgerald AA, Leclercq SA, Yan A, Homik JE, Dinarello CA. Rapid responses
to anakinra in patients with refractory adult-onset Still’s disease. Arthritis
Rheum 2005;52(6):1794-803.
11.
Lequerré T, Quartier P, Rosellini D et al. Société francophone pour la
rhumatologie et les maladies inflammatoires en pédiatrie (SOFREMIP);
Club rhumatismes et infl ammation (CRI). Interleukin-1 receptor antagonist
(anakinra) treatment in patients with systemic-onset juvenile idiopathic
arthritis or adult onset Still disease: preliminary experience in France. Ann
Rheum Dis 2008;67(3):302-8.
12.
Gattorno M, Piccini A, Lasigliè D et al. The pattern of response to anti-
interleukin-1 treatment distinguishes two subsets of patients with systemic-
onset juvenile idiopathic arthritis. Arthritis Rheum 2008;58(5):1505-15.
13.
Ohlsson V, Baildam E, Foster H et al. Anakinra treatment for systemic onset
juvenile idiopathic arthritis (SOJIA). Rheumatology (Oxford) 2008;47(4):555-6.

Images en Dermatologie • Vol. II • n° 2 • avril-mai-juin 2009
67
Thérapeutique
14.
Stankovic K, Grateau G. Auto infl ammatory syndromes: Diagnosis and
treatment. Joint Bone Spine. 2007;74(6):544-50.
15.
Shinkai K, McCalmont TH, Leslie KS. Cryopyrin-associated periodic
syndromes and autoinfl ammation. Clin Exp Dermatol 2008;33(1):1-9.
16.
Leslie KS, Lachmann HJ, Bruning E et al. Phenotype, genotype, and
sustained response to anakinra in 22 patients with autoinfl ammatory disease
associated with CIAS-1/NALP3 mutations. Arch Dermatol 2006;142(12):1591-7.
17.
Martinez-Taboada VM, Fontalba A, Blanco R, Fernández-Luna JL. Success-
ful treatment of refractory Schnitzler syndrome with anakinra: comment on
the article by Hawkins et al. Arthritis Rheum 2005;52(7):2226-7.
18.
De Koning HD, Bodar EJ, van der Meer JW, Simon A; Schnitzler Syndrome
Study Group. Schnitzler syndrome: beyond the case reports: review and
follow-up of 94 patients with an emphasis on prognosis and treatment. Semin
Arthritis Rheum 2007;37(3):137-48.
19.
Wastiaux H, Barbarot S, Gagey-Caron V, Berthelot JM, Hamidou M,
Stalder JF. Schnitzler syndrome: a dramatic improvement with anakinra. J
Eur Acad Dermatol Venereol 2009;23(1):85-7.
20.
Kluger N, Rivière S, Guillot B, Bessis D. Ef cacy of interleukin 1 receptor
antagonist (anakinra) on a refractory case of Schnitzler’s syndrome. Acta
Derm Venereol 2008;88(3):287-8.
21.
Ryan JG, de Koning HD, Beck LA, Booty MG, Kastner DL, Simon A. IL-1
blockade in Schnitzler syndrome: ex vivo findings correlate with clinical
remission. J Allergy Clin Immunol 2008;121(1):260-2.
22.
Eiling E, Schröder JO, Gross WL, Kreiselmaier I, Mrowietz U, Schwarz T.
The Schnitzler syndrome: chronic urticaria and monoclonal gammopathy-an
autoinfl ammatory syndrome? J Dtsch Dermatol Ges 2008;6(8):626-31.
23.
Delluc A, Limal N, Puéchal X, Francès C, Piette JC, Cacoub P. Ef cacy of
anakinra, an IL-1 receptor antagonist, in refractory Sweet syndrome. Ann
Rheum Dis 2008;67(2):278-9.
24.
Vounotrypidis P, Sakellariou GT, Zisopoulos D, Berberidis C. Refrac-
tory relapsing polychondritis: rapid and sustained response in the treat-
ment with an IL-1 receptor antagonist (anakinra). Rheumatology (Oxford)
2006;45(4):491-2.
25.
Wendling D, Govindaraju S, Prati C, Toussirot E, Bertolini E. Ef cacy of
anakinra in a patient with refractory relapsing polychondritis. Joint Bone
Spine 2008;75(5):622-4.
26.
Botsios C, Sfriso P, Furlan A, Punzi L, Dinarello CA. Resistant Behçet
disease responsive to anakinra. Ann Intern Med 2008;149(4):284-6.
27.
Goldbach-Mansky R, Shroff SD, Wilson M et al. A pilot study to evaluate
the safety and ef cacy of the long-acting interleukin-1 inhibitor rilonacept
(interleukin-1 trap) in patients with familial cold autoinfl ammatory syndrome.
Arthritis Rheum 2008;58(8):2432-42.
28.
Hoffman HM, Throne ML, Amar NJ et al. Ef cacy and safety of rilonacept
(interleukin-1 trap) in patients with cryopyrin-associated periodic syndromes:
results from two sequential placebo-controlled studies. Arthritis Rheum.
2008;58(8):2443-52.
29.
Church LD, McDermott MF. Rilonacept in cryopyrin-associated periodic
syndromes: the beginning of longer-acting interleukin-1 antagonism. Nat Clin
Pract Rheumatol 2009;5(1):14-5.
30.
Hoffman HM. Rilonacept for the treatment of cryopyrin-associated periodic
syndromes (CAPS). Expert Opin Biol Ther 2009;9(4):519-31.
Stelara®
Les laboratoires Janssen-Cilag ouvrent,
avec Stelara® (ustekinumab), une nouvelle
voie thérapeutique dans le psoriasis en
plaques modéré à sévère.
En France, plus de 1 million de personnes
souffrent de psoriasis, dont un quart d’une
forme modérée à sévère.
L’ustekinumab, thérapie ciblée, est un anti-
corps monoclonal anti-interleukine (anti-
IL-12/IL-23) entièrement humain. Il est
produit par une lignée cellulaire murine de
myélome en utilisant une technique d’ADN
recombinant.
L’ustekinumab présente une forte affi-
nité et une spécificité pour la sous-unité
protéique p40 des cytokines humaines
IL-12 et IL-23. En se liant à cette sous-
unité, il va bloquer la différenciation des
lymphocytes T en lymphocytes Th1 et Th17,
inhibant ainsi les signaux et les cascades
cytokiniques pro-inflammatoires qui jouent
une rôle important dans la pathogénie du
psoriasis.
Stelara
®
a obtenu une AMM européenne en
janvier 2009 grâce aux résultats de 2 études
pivot ayant inclus 1 996 patients : PHOENIX 1
et PHOENIX 2. Ces études de phase III multi-
centriques, randomisées en double aveugle
versus placebo, ont inclus des patients
adultes présentant un psoriasis en plaques
modéré à sévère depuis au moins 6 mois,
avec au moins 10 % de la surface corpo-
relle atteinte, un score PASI égal à 12 et qui
étaient candidats à la photothérapie ou à un
autre traitement systémique.
Dans chacune de ces 2 études, deux tiers
des patients (67 %) traités à la dose de
45 mg atteignaient une réponse PASI 75 à
la semaine 12, soit après seulement 2 injec-
tions, contre 4 % sous placebo.
Ces essais ont également montré que
l’amélioration importante de l’état cutané et
de la qualité de vie des patients obtenue à
12 semaines se maintenait à la 76e semaine
avec seulement 4 injections par an (toutes
les 12 semaines) après 2 doses initiales aux
semaines 0 et 4, avec un pro l de tolérance
comparable au placebo.
Stelara® béné cie d’un schéma d’adminis-
tration tant innovant que source de liberté
pour le patient : dose initiale de 45 mg par
voie sous-cutanée à la semaine 0 suivie
d’une 2e dose de 45 mg à la semaine 4, puis
d’une injection toutes les 4 semaines. Pour
les patients de plus de 100 kg, la posologie
de chaque injection sera de 90 mg.
Avant d’instaurer le traitement, les patients
doivent être dépistés pour la tuberculose. Il
est contre-indiqué en cas d’infection évolu-
tive sévère ou d’hypersensibilité au produit
ou à un de ses excipients.
Stelara
®
est soumis à prescription initiale
hospitalière de 6 mois. La prescription
initiale et le renouvellement sont réservés
aux spécialistes en dermatologie ou en
médecine interne.
Stelara® est conditionné sous forme de solu-
tion injectable en acon à usage unique de
0,5 ml de solution stérile contenant 45 mg
d’ustekinumab.
Une demande d’admission au rembourse-
ment est en cours d’évaluation.
MP
Communiqués des conférences de presse, symposiums, manifestations organisés par l’industrie pharmaceutique
Nouvelles de l’industrie pharmaceutique
1
/
5
100%