Les Centres d’investigation clinique : une révolution pour

La Lettre du Pharmacologue - vol. 21 - nos 1-2 - janvier-juin 2007
Mise au point
Mise au point
17
Les Centres d’investigation clinique : une révolution pour
la recherche et une opportunité pour les pharmacologues
Clinical investigation centers:
a revolution for research and an opportunity for pharmacologists
●● Christian Libersa*, Dominique Deplanque*
RÉSUMÉ
Les Centres d’investigation clinique (CIC), dont les plus anciens ont
déjà près de quinze ans d’existence, sont d’extra ordinaires outils pour
la recherche clinique. Les CIC, qui ont généralement une double
tutelle (INSERM et DHOS), parfois complétée par un soutien des
universités, permettent en e et un maillage complet du territoire
français. Forte de ce réseau, la France se place ainsi en très bonne
position dans le paysage européen des infrastructures institution-
nelles de recherche clinique. Cette dynamique de réseau a notam-
ment été concrétisée par la constitution de groupes de travail ayant
pour thèmes la mise en place de procédures opératoires standard,
l’évaluation du coût des essais cliniques, les systèmes d’information,
la recherche en soins in rmiers, dans une optique d’harmonisation
nationale. Le réseau des CIC a permis par ailleurs la coordination au
sein des CIC d’axes spéci ques de recherche clinique (neurologie et
maladies mentales, pédiatrie, pathologies cardiovas culaires, diabète-
métabolisme-nutrition, gastro-entérologie et hépatologie, throm-
bose). Cette approche nationale s’est complétée récemment par
l’implication des CIC dans le projet ECRIN (European Clinical Research
Infrastructures Network), dont l’objectif est de mettre en relation les
* Centre d’investigation clinique – Centre de ressources biologiques, CIC 9301 INSERM – CHU de Lille, 59037 Lille.
réseaux nationaux de centres de recherche clinique en Europe. Outre
les soutiens purement techniques et logistiques, les CIC apportent
aux collectivités institutionnelles et aux partenaires industriels une
réalisation dans les meilleures conditions d’assurance qualité, de
sécurité et d’e cacité des projets de recherche clinique. Dans ce
contexte, plus de la moitié des CIC français sont actuellement pilotés
par des pharmacologues, professionnels sans doute les plus adaptés
à la prise en charge de ces structures de recherche aux activités à
la fois multidisciplinaires et translationnelles. En e et, de par leurs
compétences et les liens qu’ils ont su tisser tant au sein des di érentes
institutions et autorités compétentes que vis-à-vis de l’industrie, les
pharmacologues ont toute leur place dans ces structures de recherche
clinique. L’implication toujours plus grande de chacun d’entre nous
est nécessaire et représente aussi une réelle opportunité de participer
au développement d’une recherche clinique de qualité.
Mots-clés : Pharmacologie clinique – Pharmacologie fonda-
mentale – Pharmacovigilance – Centres d’investigation clinique –
Recherche clinique – Réseaux.
SUMMARY
For more than 15 years, Clinical Investigation Centers (CIC) have taken
a growing place in the eld of clinical research in France. Usually pla-
ced under the auspices of both INSERM and DHOS, sometimes also
supported by University, the CIC actually constitute a robust network
that puts France at a leading position inside the European community
in terms of structures dedicated to clinical research. The French CIC
network has developed both working groups (operating procedures,
cost of clinical research, information systems, nurse care research…)
and speci c networks of research (neurology and mental diseases,
paediatrics, cardiovascular pathologies, diabetes-metabolism and nutri-
tion, bowel and liver diseases, thrombosis). This national approach has
been recently completed by the participation to the European Clinical
Research Infrastuctures Network (ECRIN), whose aim is to interconnect all
European clinical research centers and structures. Aside their implications
in technical and logistical aspects of clinical research, CIC could help both
public institutions and industries to develop secure, innovative and high
quality projects. In this context, many CIC are directed by pharmacolo-
gists, people who seem particularly able to conduct such translational
activities. Indeed, according to their various competences and to their
relationship with both public institutions, competent authorities and
industry, pharmacologists should have a prominent position in such
structures. A greater participation of everyone is now necessary when
such structures give us an interesting opportunity to participate in the
development of high quality clinical research.
Keywords: Clinical pharmacology – Fundamental pharmaco-
logy – Pharmacovigilance – Clinical investigation centers – Clinical
research – Network.

La Lettre du Pharmacologue - vol. 21 - nos 1-2 - janvier-juin 2007
Mise au point
Mise au point
18
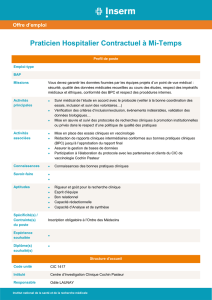
Figure 1.
Répartition des CIC en 2005. (Source INSERM).
HISTORIQUE ET CONCEPT
DES CENTRES D’INVESTIGATION CLINIQUE
Le concept de Centre d’investigation clinique (CIC) inspiré
des General Clinical Research Centers, soutenus par le NIH
(National Institute of Health) aux États-Unis, a été introduit et
défendu en France il y a plus de quinze ans par Pierre Corvol
et Claude Griscelli et a abouti en 1992 à la création des deux
premiers CIC “prototypes” plurithématiques, bientôt suivis,
à la suite d’appels d’off res conjoints INSERM et Direction de
l’hospitalisation et de l’organisation des soins (DHOS), par six
autres en 1994 pour atteindre un nombre de dix-sept centres
en 2001 et vingt-quatre en 2005. Ces structures ont ensuite été
complétées par la création de sept CIC-EC, CIC spécifi que-
ment orientés vers les essais en épidémiologie (fi gure 1). Le
développement de ces structures place ainsi la France en très
bonne position dans le paysage européen des infrastructures
institutionnelles de recherche clinique, et ce d’autant que des
structures plus spécifi quement consacrées aux biothérapies
ont été récemment soutenues et rattachées aux CIC, comme
le seront probablement bientôt d’autres structures dédiées aux
innovations technologiques.
IMPLANTATIONS ET TUTELLES
Les Centres d’investigation clinique représentent un partenariat
unique entre les hôpitaux et l’INSERM. Ce sont en eff et des
structures publiques, principalement implantées dans les Centres
hospitalo-universitaires sous la double tutelle INSERM et DHOS.
Quelques CIC ont été, dès leur création, placés également sous
une troisième tutelle, celle de l’Université. L’implication de cet
acteur universitaire reste cependant très dépendante de l’organi-
sation hospitalo-universitaire locale et du type généraliste ou à
plus forte connotation médicale de l’université impliquée. Il faut
cependant souligner que l’évolution semble se faire progressive-
ment vers ce triple partenariat INSERM-hôpital-université.
MISSIONS
À l’origine, les CIC étaient principalement envisagés comme de
simples lieux de réalisation d’essais cliniques off erts à la commu-
nauté des promoteurs et investigateurs institutionnels dans le
respect des bonnes pratiques cliniques et de laboratoire et des
très nombreuses dispositions médico-réglementaires. Avec

La Lettre du Pharmacologue - vol. 21 - nos 1-2 - janvier-juin 2007
Mise au point
Mise au point
19
plus de quinze ans de recul, il devient évident que cette simple
mission de départ a évolué et s’est enrichie. Les CIC sont désor-
mais des structures disposant de moyens matériels et humains
spécifi quement dédiés à la recherche clinique, permettant la
mise au point, la gestion, la coordination et la réalisation de
protocoles de recherche clinique, tant chez le sujet volontaire
sain que chez le patient. Ils sont par ailleurs le lieu idéal de
transfert des résultats de la recherche fondamentale vers des
évaluations et applications thérapeutiques et diagnostiques. Les
CIC occupent ainsi une position centrale dans la structuration
de la politique de recherche clinique des CHU et contribuent à
valider la mission de recherche médicale de l’INSERM.
Les CIC, en favorisant les transferts entre recherche fondamentale
expérimentale et pratiques de soins, participent de façon évidente
à la politique de valorisation universitaire de la recherche clinique
du site. Lieu de contact privilégié entre chercheurs fondamentaux
et cliniciens, les CIC constituent un élément fédérateur important
en permettant aux cliniciens de s’intégrer aux programmes de
recherche situés en amont de leurs problématiques cliniques et
aux chercheurs fondamentalistes de trouver un débouché et une
fi nalité clinique à leurs travaux fondamentaux. Les CIC, tout en
étant naturellement intégrés dans les structures hospitalières,
sont ouverts aux investigateurs de l’INSERM ou d’autres orga-
nismes publics (universités, EFS, FNCLCC, AFM…) ainsi qu’aux
partenaires industriels soucieux de mener des recherches à haute
valeur ajoutée sur l’homme sain et malade.
Ces recherches couvrent des investigations cliniques de toute
nature, qu’elles soient “avec ou sans bénéfi ce individuel direct”,
selon l’ancienne terminologie malheureusement abandonnée dans
les textes issus de la transposition des directives européennes. Sont
ainsi ciblés, sans exclusive, les domaines de la physiologie, de la
physiopathologie, de la pharmacologie, des essais thérapeutiques,
de la génétique et de l’épidémiologie, en privilégiant les aspects les
plus innovants. Bien entendu, les CIC ne concernent pas les études
expérimentales animales et n’y sont pas adaptés, mais ils peuvent
être le lieu de l’évaluation clinique des hypothèses émises par ces
expérimentations chez l’animal, concrétisant ainsi le continuum
entre recherche fondamentale et recherche clinique.
Dans ce contexte, les CIC bénéfi cient des agréments ministériels
pour eff ectuer des recherches biomédicales sans bénéfi ce indi-
viduel direct et sur le sujet volontaire sain, avec des spécifi cités
plus ou moins étendues en fonction de leur environnement ou
des axes thématiques éventuellement privilégiés.
Compte tenu de l’investissement important en moyens techniques
et des compétences des professionnels de la recherche clinique
impliqués dans ces structures, les CIC, en fonction de la demande
formulée par les investigateurs, peuvent apporter un soutien tout
au long de la vie de l’essai clinique, de la conception à la réalisation
et à la communication des résultats. Peuvent ainsi être proposés
un conseil méthodologique pour la formalisation des projets, une
assistance technique pour les démarches administratives (démar-
ches auprès du promoteur institutionnel, du Comité de protection
des personnes, des autorités compétentes, de la Commission
nationale de l’informatique et des libertés…), le recrutement de
volontaires sains ou de patients, l’obtention d’agréments ministé-
riels pour la réalisation de recherches biomédicales sans bénéfi ce
individuel direct, le soutien technique et/ou logistique pour la
réalisation d’essais cliniques complexes ou nécessitant l’appui de
réseaux de patients ou d’investigateurs, la mise en place éventuelle
d’équipes soignantes mobiles en dehors des locaux mêmes du CIC
(dans des services du CHU ou d’hôpitaux généraux, voire dans des
réseaux de médecine de ville), une aide à la saisie des données et/ou
à l’analyse des résultats, un accompagnement pour les réponses
aux appels d’off res fi nançant la recherche clinique…
Ces compétences multiples font des CIC des lieux privilégiés
de formation aux métiers de la recherche clinique, aux bonnes
pratiques cliniques et à l’assurance-qualité.
LOCAUX ET MODES DE FONCTIONNEMENT
Les CIC bénéficient de locaux spécifiques consacrés à la
recherche, permettant une prise en charge sécurisée diurne
et/ou nocturne des sujets volontaires sains ou des patients inclus
dans des essais cliniques ainsi que la réalisation d’explorations
paracliniques nécessaires à chaque projet. Même si le déve-
loppement des CIC s’est fait de façon inégale, la plupart sont
actuellement équipés de lits (3 à 10) et de matériels permettant
les explorations paracliniques de base requises dans les essais de
phase I. Certains CIC se sont par ailleurs équipés de matériels
plus spécifi ques, en fonction de leurs éventuelles thématiques
de prédilection et de l’environnement de recherche de l’établis-
sement où ils sont implantés.
Certains CIC ont par ailleurs développé une infrastructure
spécifi que de conservation des produits biologiques et ont pu
être reconnus par l’ANR comme ayant une activité de Centres de
ressources biologiques, structures qui off rent toutes les garanties
de sécurité et de qualité vis-à-vis des prélèvements conservés.
Ces activités spécifi ques sont actuellement en cours de label-
lisation par une démarche de certifi cation selon le référentiel
iso 9001:2000.
En termes d’organisation, les CIC sont pilotés par un médecin
coordonnateur assisté d’un médecin délégué. Ils s’appuient
sur des professionnels de la recherche clinique (praticiens,
infi rmières[iers], techniciens, assistants de recherche clinique…)
et, pour certains CIC, de gestionnaires d’essais cliniques, phar-
maciens, ingénieurs de recherche, techniciens de laboratoire,
biostatisticiens, etc. Le recrutement de ces professionnels tient
généralement compte d’une formation spécifi que telle que le
DIU-FARC (diplôme interuniversitaire en recherche clinique)
ou équivalents (master en méthodologie de recherche clinique,
ingénierie de la santé…), le DIU-FIEC (diplôme interuniversi-
taire de formation des investigateurs en recherche clinique) ou
équivalents (DIU de logistique des essais cliniques…).
Les projets mis en place dans les CIC sont préalablement évalués
par un comité technique qui a pour mission d’en examiner la
qualité scientifi que et de vérifi er l’adéquation entre le projet,
l’infrastructure et les démarches stratégiques de recherche des
établissements tutélaires, puis d’en contrôler régulièrement l’état
d’avancement. Le comité technique est généralement composé du

La Lettre du Pharmacologue - vol. 21 - nos 1-2 - janvier-juin 2007
Mise au point
Mise au point
20
médecin coordonnateur et du médecin délégué, de représentants
des services hospitaliers et des unités INSERM participant à l’acti-
vité du CIC, d’un représentant du comité médical d’établissement
ou de la commission mixte hospitalo-universitaire, d’un métho-
dologiste et biostatisticien, d’un médecin extérieur à la structure
hospitalo-universitaire, d’un représentant des cadres infi rmiers
et d’un représentant du directeur de l’établissement. Ce comité
se réunit une fois par mois ou plus en cas de besoin.
ÉVALUATIONS
L’une des caractéristiques des CIC – et cela les distingue de
certains centres de recherches cliniques non labellisés – est
qu’après la diffi cile reconnaissance initiale contemporaine de leur
création, ils sont soumis à des évaluations menées conjointement
par l’INSERM et les hôpitaux sur une base quadriennale. Cette
évaluation s’appuie sur une expertise de l’activité scientifi que,
sur une évaluation du respect des bonnes pratiques cliniques
et de laboratoire et des procédures d’assurance-qualité, ainsi
que sur les capacités de gestion structurelle.
Pour chaque CIC sont donc désignés des rapporteurs proposés
par l’INSERM et le CHU impliqué, rapporteurs qui auront
pour mission de rendre un avis sur l’activité des CIC selon des
critères défi nis et approuvés par un comité mixte d’évaluation.
Ces critères portent, entre autres, sur la contribution du CIC
au développement local de la recherche, son articulation entre
la recherche menée dans les laboratoires et équipes d’accueil
du site et les services cliniques, ainsi que sur l’interaction avec
les plateaux techniques de recherche innovante disponibles sur
le site. Sont également pris en compte l’aide méthodologique
aux investigateurs en amont de la réalisation des protocoles,
l’équilibre entre les thématiques développées en fonction des
axes “forts” du site, la quantité et la qualité des publications, les
retombées potentielles en thérapeutique et en santé publique.
L’évaluation quadriennale se fait au vu d’un rapport d’activité dans
lequel le médecin coordonnateur présente le bilan des quatre
dernières années et expose ses projets de développement pour le
quadriennat suivant, rapport complété par une visite sur site. À
l’issue de ces visites, les rapporteurs cosignent un compte-rendu
commun, qui sera présenté en séance plénière à la commission
d’évaluation devant laquelle le médecin coordonnateur aura préa-
lablement exposé par oral le bilan et les perspectives envisagées.
D’autre part, outre les éventuels audits industriels et les inspections
menés par l’AFSSAPS, tous les CIC ont fait l’objet d’un ou de deux
audits mandatés conjointement par l’INSERM et la DHOS. Ces
audits externes ont comporté un audit transversal des processus
et un audit vertical de la structure.
Le comité mixte d’évaluation prend en compte l’ensemble des
rapports d’activité, présentations et audits pour proposer au
conseil scientifi que de l’INSERM et aux directeurs généraux de
l’INSERM et du CHU concerné la reconduction, la fermeture ou
la mise sous surveillance rapprochée (évaluation à deux ans) du
CIC évalué. Le résultat de cette évaluation contribue également
à la modulation du soutien budgétaire attribué.
RÉSEAU NATIONAL DES CIC
ET GROUPES DE TRAVAIL
Depuis 2002, les CIC se sont groupés en réseau sous l’égide
de l’INSERM. Ils ont tenu leur première réunion nationale le
lundi 14 avril 2003 à Lille, dans le cadre de la réunion annuelle
de la Société française de pharmacologie. Ce réseau des CIC
est animé par un coordinateur et un bureau composé de quatre
membres coordonnateurs ou médecins délégués de CIC. Ses
missions essentielles sont de défi nir les programmes des réunions
bimestrielles des CIC et des séminaires réalisés annuellement
(les représentants des CIC se réunissent tous les deux mois et
organisent un séminaire annuel du réseau des CIC qui a lieu
traditionnellement lors de la réunion de la Société française
de pharmacologie et de thérapeutique), de mettre en place et
de suivre les groupes de travail du réseau, de représenter le
réseau des CIC lors des réunions externes et d’en être le point
de contact. Ce bureau permet ainsi de défi nir les stratégies pour
améliorer les collaborations interCIC et la visibilité auprès des
institutions et des industriels.
De cette manière, institutions et industriels bénéfi cient d’un
réseau de compétences et d’expertises et d’un système d’assu-
rance-qualité reconnu, permettant notamment de faciliter et
d’accélérer le recrutement des sujets dans les études. La proxi-
mité des équipes de recherche fondamentales et leur implication
dans les CIC sont un attrait supplémentaire pour les entreprises
de biotechnologie. Ce réseau pourrait ainsi également contri-
buer à l’amélioration de la visibilité de la recherche clinique
et de l’attractivité de la France vis-à-vis des industriels et des
chercheurs cliniciens étrangers.
Groupes de travail
Sous l’impulsion du bureau du réseau national des CIC, ont
été mis en place des groupes de travail visant à harmoniser les
pratiques dans les CIC et à favoriser leur visibilité en tant qu’outil
de qualité pour mener des recherches de la preuve de concept
aux études post-AMM. Les quatre groupes “Harmonisation
des procédures”, “Harmonisation des pratiques fi nancières des
CIC”, “Harmonisation des systèmes d’information”, “Recherche
en soins infi rmiers” se réunissent régulièrement et présentent
leurs travaux lors des réunions bimestrielles ou annuelles.
✓ Ainsi le groupe “Harmonisation des procédures” (Cathe-
rine Cornu) a permis de sensibiliser les diff érents partenaires
de la recherche à la démarche qualité, qui est essentielle pour
assurer à la fois une prise en charge optimale des participants
aux études et un niveau de certitude élevé quant aux conclu-
sions tirées de l’analyse des données recueillies. Les procédures
opératoires standard et processus sont ainsi progressivement
harmonisés dans l’ensemble des CIC, conduisant à la mise en
place d’un contrôle de la qualité avec des stratégies de correc-
tions des anomalies ou écarts par rapport aux objectifs et au
respect strict des textes réglementaires et des référentiels dans
le domaine de la recherche clinique (Bonnes Pratiques Cliniques
et de Laboratoire), garantissant ainsi un niveau d’excellence et
d’expertise.

La Lettre du Pharmacologue - vol. 21 - nos 1-2 - janvier-juin 2007
Mise au point
Mise au point
21
✓ Le groupe “Harmonisation des pratiques fi nancières des
CIC” (Christian Funck-Brentano, Fabienne Lecomte), tout en
prenant en compte certaines spécifi cités locorégionales, a permis
d’individualiser les diff érents postes budgétaires et les coûts induits
par les projets de recherche clinique et, ainsi, de s’approcher d’une
harmonisation des coûts : les diff érences primitivement constatées
se sont révélées être dues non pas tant à des diff érences de coûts
par poste dans les diff érents CIC qu’à des non-prises en compte de
certains de ces postes, le plus souvent par oubli ou mauvaise prise
en compte du cahier des charges. Le travail de ce groupe a égale-
ment permis de démarrer une réfl exion au niveau de la Fédération
hospitalière de France dans le cadre plus général de l’évaluation
du coût des essais cliniques dans les structures hospitalières et au
niveau des Centres de Ressources Biologiques. La mise en exergue
du coût plus élevé des études réalisées dans les CIC, quelquefois
faite par certains investigateurs ou industriels, s’avère dès lors
être plutôt en rapport avec une médiocre évaluation fi nancière
par les services cliniques classiques et avec une transparence des
fl ux fi nanciers pas toujours très claire vis-à-vis des institutions.
Cependant, même dans ces conditions, le surcoût apparent ou
réel est largement compensé par la qualité du service rendu, tant
au niveau scientifi que qu’au niveau de la réalisation du cahier des
charges, notamment en termes de données recueillies. Sachant
que les coûts des essais cliniques en France sont environ quatre
fois moindres qu’aux États-Unis, il reste une certaine marge de
manœuvre quant à l’évaluation correcte des services rendus par
ce type de structure.
✓ Le groupe de travail “Harmonisation des systèmes d’infor-
mation” (François Gueyffi er) s’est heurté au problème général
de la grande disparité des outils informatiques, tant sur le plan
qualitatif que sécuritaire, et à la diffi culté d’obtenir un compromis
acceptable coût/sécurité/fonctionnalité. Ce groupe a néanmoins
permis de faire le point sur les diff érents systèmes existants,
parfois innovants, et a entraîné une réfl exion sur les avantages et
les inconvénients des diff érents systèmes de saisie et de contrôle
de données. Il a abouti à la réalisation d’un site Web dédié au
réseau qui a été formaté pour faciliter les échanges entre les
groupes de travail et le réseau des CIC et pourrait préfi gurer un
outil collaboratif commun d’échange ou de transfert de données.
Il permet l’amélioration de la lisibilité et de l’attractivité des CIC
avec peut-être, à terme, la mise en place d’un guichet unique de
gestion des relations partenariales et l’affi chage des compétences
humaines et techniques du réseau. Il permettra également le
développement d’outils de communication à visée extérieure
(site Internet), centralisés et régulièrement mis à jour.
✓ Le groupe de travail “Recherche en soins infirmiers”
(Marie-Laure Bourhis) répond à la volonté de développer des
travaux eff ectués et/ou conduits par les infi rmières des CIC pour
développer leurs connaissances professionnelles et améliorer
leurs pratiques. Ces travaux peuvent concerner des recherches
cliniques en soins infi rmiers, des recherches en éducation, en
gestion de soins infi rmiers et/ou des recherches sur la profession
infi rmière de recherche clinique. Le premier travail de ce groupe
a été d’analyser au niveau national le travail des infi rmières
dans les CIC et de mettre en commun leurs connaissances sur
des thématiques diff érentes (douleur, éducation du patient,
nutrition…). Ce groupe a également réfl échi sur le parcours
professionnel, les formations et le rôle spécifi que de l’infi rmière
de CIC, et a proposé des projets de recherche en soins.
Ces réfl exions et enquêtes ont permis de constater que près de
90 % du personnel infi rmier a suivi une formation spécifi que
(dont plus de la moitié le DIU FARC [diplôme interuniversitaire
de formation des assistants de recherche clinique] et qu’il était
indispensable d’unir les compétences des diff érents acteurs de la
recherche clinique, à savoir d’une part les personnels impliqués
dans le fonctionnement des CIC, qui ont une bonne maîtrise des
aspects de bonnes pratiques, de logistique et dans le domaine
médico-réglementaire et, d’autre part, les infi rmières des services
cliniques, qui connaissent bien les problématiques “de terrain”
et les aspects spécifi ques des pathologies prises en charge.
Axes thématiques de recherche
En 2004, le bureau du réseau national a engagé une réfl exion qui a
abouti à la mise en place de six réseaux thématiques de recherche
regroupant plusieurs CIC en fonction de leurs spécifi cités ou
capacités de prise en charge. Ont ainsi été créés un réseau Neuro-
logie et maladies mentales (Philippe Damier, Nantes) regroupant
14 CIC, un réseau Pédiatrie (Pr Évelyne Jacqz-Aigrain, Paris)
regroupant 8 CIC, un réseau Cardiovasculaire (Faiez Zannad,
Nancy) regroupant 16 CIC, un réseau Diabète-métabolisme-
nutrition (Pierre Petit, Montpellier) regroupant 12 CIC, un
réseau Gastro-entérologie et Hépatologie (Christian Libersa, Lille)
regroupant 17 CIC et un réseau rombose (Hervé Decousus,
Saint-Étienne). Une réfl exion est en cours pour la constitution
d’un réseau en Cancérologie (Fabien Calvo, Paris – Saint-Louis –)
et en Biothérapie.
Cette organisation en réseaux thématisés renforce la collabora-
tion entre les CIC travaillant sur les mêmes thématiques, favorise
la mise en place de projets de recherche communs et vient en
appui aux réseaux de spécialités existants, qui peuvent ainsi
bénéfi cier de l’expérience et du professionnalisme des CIC.
Réseau européen
La dynamique du réseau national des CIC a tout naturellement
conduit vers une off re d’ouverture européenne. Cela s’est concré-
tisé par l’implication de l’INSERM et de certains coordonna-
teurs de CIC dans le projet ECRIN (European Clinical Research
Infrastructures Network), qui s’inscrit naturellement dans le
projet ambitieux de construction de l’espace européen de la
recherche clinique. Ce projet ECRIN, soutenu par le 7e PCRDT,
vise à connecter les réseaux nationaux de centres de recherche
clinique en Europe. Coordonné par l’INSERM, le projet réunit
actuellement six pays et leurs réseaux de recherche clinique
(réseau des KKS allemands, réseau des centres d’essais cliniques
danois, réseau italien du CIRM [Consortium pour la recherche
médicale] et Institut Mario Negri italiens, réseau suédois, réseau
espagnol et réseau français des CIC).
L’objectif de ce réseau européen est de tendre vers une harmo-
nisation de la formation, des pratiques et des supports de la
recherche clinique, de l’éthique, de la réglementation, de la
 6
6
1
/
6
100%