Lire l'article complet

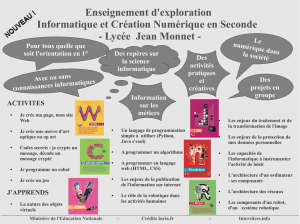
Figure 1. Installation de la salle d’opération pour une chirurgie transorale robotisée d’un
cancer du pharyngo-larynx.
Console
du chirurgien Bras
du robot
Instrumentiste
Aide
Tête du patient
122 | La Lettre du Cancérologue • Vol. XX - n° 2 - février 2011
DOSSIER THÉMATIQUE
Cancérologie et ORL
La chirurgie robotique
par voie transorale
en cancérologie ORL :
indications et perspectives
Transoral robotic surgery in head and neck cancers:
indications and prospects
S. Morinière*, Y. Mallet**
* Service d’ORL, hôpital Bretonneau,
Tours.
** Service d’ORL, centre Oscar-
Lambret, Lille.
L
a chirurgie des cancers des voies aéro-digestives
supérieures (VADS) a pour objectif de faire une
exérèse tumorale de qualité tout en limitant les
séquelles fonctionnelles et esthétiques. Le dévelop-
pement de la chirurgie partielle pour le traitement des
tumeurs pharyngo-laryngées dans les années 1970 (1)
puis la chirurgie minimale invasive par voie
endoscopique au laser CO2 dans les années 1990 (2)
se sont inscrits dans cette démarche d’efficacité
thérapeutique s’associant à une amélioration des
suites postopératoires. La chirurgie robot-assistée
émergente a également pour objectif la réduction
des morbidités associées. Le robot Da Vinci®, initia-
lement conçu pour la chirurgie cœlioscopique, a
été “détourné” de cette première indication pour
être utilisé en chirurgie endoscopique au niveau du
pharyngo-larynx par une équipe chirurgicale ORL de
l’hôpital universitaire de Philadelphie (États-Unis)
en 2005 (3). N.G. Hockstein et al. ont évalué les
modalités d’utilisation de ce robot dans le pharynx et
le larynx en termes de faisabilité et de sécurité. Ce sont
I.K. McLeod et al. (4) qui ont publié la première inter-
vention réalisée avec succès au robot pour l’exérèse
d’un kyste valléculaire. En 2006, les trois premiers
cas de cancers débutants de la base de la langue sont
publiés par B.W. O’Maley Jr et al. Les premières séries
chirurgicales apparaissent dès 2007 (5, 6). En France,
la chirurgie transorale robotisée (TORS) a débuté
en 2008 au centre hospitalier universitaire de Tours
et au centre Oscar-Lambret de Lille (7). Actuellement
une douzaine de centres réalisent cette chirurgie et
plus de 100 patients ont été traités pour un cancer
des VADS par cette technique innovante.
Les grands principes
de la chirurgie transorale
robotisée
Le robot Da Vinci® comporte 3 composantes : le
robot, la console du chirurgien et la colonne technique
avec les sources de lumière, la caméra 3D, les généra-
teurs monopolaire et bipolaire et l’écran de contrôle
(fi gure 1). L’utilisation d’un écarteur de bouche spéci-
fi que (FK société Olympus) permet de positionner,
dans le pharynx, l’optique de 8 mm à 0 ou 30° ainsi
que 2 bras porteurs d’instruments de 5 mm (une pince

Figure 2. Position du chirurgien à la console lors de
la réalisation d’une chirurgie transorale robotisée
d’un cancer du pharyngo-larynx.
La Lettre du Cancérologue • Vol. XX - n° 2 - février 2011 | 123
Points forts
»
La chirurgie endoscopique robot-assistée dans le traitement des cancers du pharyngo-larynx a pour
objectif la réduction des morbidités associées.
»
Les premières séries chirurgicales sont apparues dès 2006 aux États-Unis ; en France, cette pratique
remonte à 2008.
»Les indications actuellement retenues sont les tumeurs T1-T2 de l’oropharynx, de la margelle laryngée
et de l’hypopharynx haut.
»
En postopératoire, 90 % des patients n’ont pas de trachéotomie et 60 % d’entre eux peuvent s’alimenter
avant le 7
e
jour.
»Dans la majorité des études, les marges d’exérèse sont satisfaisantes.
»
Les résultats carcinologiques sont en cours d’évaluation du fait du manque de recul dont on dispose
par rapport à cette nouvelle technique.
Mots-clés
Chirurgie transorale
robot-assistée
Chirurgie
endoscopique robot-
assistée
Cancer des voies aéro-
digestives supérieures
Highlights
»
Robotic assisted surgery
is a new field of developing
program in head and neck
oncology. This new procedure
potentially offers alternatives
to conventional surgery with
decreased morbidity. The aim of
this article was a description of
the state of the art via a review
of the literature. We emphasize
limits and future prospects on
this topic. T1 and T2 squa-
mous-cell carcinomas of the
pharyngolarynx are nowadays
the main indications for this
procedure.
»
Transoral robotic surgery
(TORS) prospects are the
development of new associated
functions like an image guid-
ance system or a force feed-
back control. The expanding of
this new tool will also depend
on the quality of clinical works
and research programs. Such
are the goals the French ENT
robotic group pursue.
Keywords
Transoral robotic surgery
(TORS)
Endoscopic head and neck
surgery
Robot-assisted endoscopic
surgery
Head and neck cancer
Minimally invasive surgery
et un bistouri électrique monopolaire). Ces bras sont
commandés par le chirurgien qui travaille à côté du
malade, sur une console avec la vision en 3D et un
grossissement possible jusqu’à 10 fois. Le temps d’ins-
tallation (aux alentours de 30 mn) de l’écarteur et
des bras est essentiel pour permettre une chirurgie
optimale. Un assistant est en permanence positionné
à la tête du patient pour aspirer, vérifi er la position des
bras dans la bouche et prévenir des confl its éventuels.
Un instrumentiste assure le chargement des instru-
ments sur les bras du robot et leur nettoyage ainsi
que la préparation des fi ls de suture. À la console,
le chirurgien manipule, avec la pince pouce-index,
2 manettes qui transmettent les mouvements
aux instruments avec un rapport de 5 (mains du
chirurgien) pour 1 (instruments dans le larynx). Cela
permet de conférer au geste une grande précision et
supprime totalement les tremblements (fi gure 2).
L’utilisation de ces manettes est très naturelle, ce qui
donne une dextérité très appréciable à l’opérateur, qui
travaille de plus en position assise, avec les bras sur
un support et donc dans une position très confortable.
Il faut régulièrement repositionner l’écarteur ou les
bras au fur et à mesure que la résection tumorale
progresse. Ce rôle revient à l’assistant.
Les indications
Comme le précise l’équipe de G.S. Weinstein (8),
c’est la réalisation d’une endoscopie préopératoire
qui permet de sélectionner les patients candidats
à une chirurgie endoscopique robotisée. Elle doit
être faite par le chirurgien qui réalisera la chirurgie
robotique. Les principaux critères étudiés sont la
situation anatomique de la lésion, sa taille, la qualité
de l’ouverture buccale, le caractère denté ou non du
patient et la morphologie maxillo-mandibulaire. Une
petite ouverture de bouche, une dent sur pivot ou
un rétrognatisme et/ou une grosse base de langue
sont des contre-indications relatives que seul le
chirurgien robotique peut évaluer. Ainsi, grâce à
cette présélection, un nombre très faible de patients
sont exclus du fait d’une mauvaise exposition. Seuls
3 patients sur 150 étaient inexposables dans la série
de G.S. Weinstein et al. (8).
Les indications actuellement retenues sont les
tumeurs T1-T2 de l’oropharynx, de la margelle
laryngée et de l’hypopharynx haut (9). L’absence de
retour de force à la console rend la palpation des
tissus impossible avec les instruments, donc les
tumeurs très infi ltrantes en profondeur sont, dans
notre expérience, des contre-indications. La taille des
instruments (5 mm) permet diffi cilement de travailler
dans l’endolarynx, et la chirurgie endoscopique au
laser CO2 a notre préférence dans ces localisations.
Les suites postopératoires
et les résultats fonctionnels
(tableau, p. 124)
Même si cette chirurgie est moins invasive, elle est
réalisée dans une zone étroite richement vascula-
risée avec la fonction essentielle qu’est la coordi-
nation respiration-déglutition. Dans la majorité des
procédures de chirurgie télérobotisée endoscopique,
l’estimation de la perte sanguine est très faible
(< 200 ml) [8]. Cependant, des complications
hémorragiques ont été rapportées. Sur 27 patients
opérés pour un cancer des amygdales, G.S. Weinstein
et al. ont observé 1 cas de saignement justifi ant d’un
contrôle d’hémostase au bloc opératoire (6). T.A. Iseli
et al. (10) ont observé 3 cas de saignement, tous
contrôlés, dans une série de 54 patients, essentiel-
lement des T1 ou des T2 (80 %) de l’oropharynx (61 %).

124 | La Lettre du Cancérologue • Vol. XX - n° 2 - février 2011
La chirurgie robotique par voie transorale en cancérologie ORL :
indications et perspectives
DOSSIER THÉMATIQUE
Cancérologie et ORL
Cette chirurgie robotique endoscopique a pour
objectif une reprise de l’alimentation précoce et
une diminution du nombre de trachéotomies dites
“de sécurité”. Dans la publication de l’équipe de
B.A. Boudreaux (11), 13 patients sur 29 justifi èrent
d’une sonde naso-gastrique à l’issue de leur hospi-
talisation (médiane : 2,9 jours ; extrêmes : 1-13 jours).
Les facteurs associés à la dépendance à l’égard d’une
sonde naso-gastrique étaient l’âge avancé (p = 0,02),
une localisation laryngée (p < 0,001) et la taille de
la tumeur (p = 0,02). La réalisation ou pas d’une
trachéotomie et sa durée est régulièrement rapportée
par les principales équipes. E.M. Genden et al. (9)
n’ont rapporté aucun cas de trachéotomie pour les
18 patients opérés d’un T1-T2 de l’oropharynx ou
de la margelle laryngée. Certaines équipes réalisent
une intubation prolongée de 48 h pour passer la
phase critique postopératoire (11). Dans la série de
E.J. Moore et al. (12), une trachéotomie a été réalisée
pour 14 des 45 patients. Tous les patients ont été
décanulés à l’issue du traitement.
La durée d’hospitalisation
Lors de la réalisation d’une chirurgie partielle supra-
glottique par voie cervicale, les durées d’hospitali-
sation dépendent du sevrage de la trachéotomie
et de la reprise de l’alimentation orale. Ainsi, pour
L. Laccourreye et al., la durée moyenne de la trachéo-
tomie est de 5 jours avec une alimentation par sonde
pendant 15 à 20 jours en moyenne (13). En chirurgie
endoscopique au laser, ces chiffres diminuent car la
plupart des patients n’ont pas de trachéotomie et
reprennent l’alimentation vers le 7e jour ; la durée
moyenne d’hospitalisation est de 10 à 13 jours (14).
Après TORS, les différentes série de la littérature
rapportent des durées d’hospitalisation moyennes
de 2 jours (9), 3 jours (11) et 7 jours (8), essentiel-
lement du fait du faible pourcentage de trachéo-
tomies (inférieur à 10 %) et d’une reprise alimentaire
précoce (moins de 7 jours).
Les résultats carcinologiques
précoces
Compte tenu du caractère récent de la mise en
place de cette nouvelle technique, il n’est pas
encore possible d’évaluer les résultats oncologiques
à long terme. Cependant, la qualité des marges
d’exérèse est un facteur pronostique important
dans le contrôle local. Les principaux auteurs
rapportent des marges négatives dans la quasi-
totalité des cas de leurs séries respectives (8, 9, 11).
Les résultats carcinologiques se sont révélés très
satisfaisants (marge in sano : 27 patients sur 29,
soit 96 %) dans la série de patients opérés d’un
carcinome de l’amygdale (6). Pour les 29 patients
opérés de la série de B.A. Boudreaux et al. (11), les
marges étaient négatives dans la totalité des cas.
G.S. Weinstein et al. ont observé, avec un recul
moyen de 26 mois (8), 47 patients traités pour
un cancer de l’oropharynx de stade III ou IV. Ils
ne déplorent qu’une seule marge positive (2,1 %).
Les patients ont tous bénéficié d’un évidement
cervical et d’un traitement complémentaire confor-
mément aux recommandations. Le contrôle local,
le contrôle régional et le contrôle à distance étaient
de 46 (97,9 %), 45 (95,7 %) et 43 (91,5 %) patients
sur 47. La survie globale à 1 et à 2 ans était de 95,7 %
(45 patients sur 47) et de 81,8 % (27 patients sur 33).
Les survies spécifi ques à 1 et à 2 ans étaient respecti-
vement de 97,8 % (45 patients sur 46) et de 90,0 %
(27 patients sur 30). Ces très bons résultats, en parti-
culier pour un nombre non négligeable de tumeurs
évoluées, ouvrent la voie à des indications plus larges
portant sur des tumeurs avancées localement.
Les perspectives
Ce nouvel outil appliqué à la chirurgie endoscopique
se révèle très prometteur. L’ensemble des équipes
précitées confirment l’intérêt de cette nouvelle
technologie en application chirurgicale ORL par
voie endoscopique. Le couplage récent au système
robotisé Da Vinci® du laser CO
2
, instrument
maintenant routinier en chirurgie ORL endoscopique,
élargit plus encore l’offre chirurgicale de ce système,
notamment pour l’endolarynx (9, 15).
L’absence de palpation en chirurgie robotique rend
actuellement très diffi cile l’exérèse de lésions infi l-
trantes de la base de la langue ou de la loge amygda-
lienne et plus encore de l’hypopharynx. Le couplage
du robot avec un système de guidance par l’image
serait susceptible de lever cette diffi culté balistique,
essentielle dans l’essor de cette technique en chirurgie
Tableau. Durée de la sonde naso-gastrique, pourcentage de trachéotomies, de saignements
et de sorties avant la première semaine en postopératoire d’une chirurgie transorale robotisée
pour un cancer du pharyngo-larynx dans les séries de la littérature.
SNG < 7 j
(%)
Trachéotomies
(%)
Saignements
(%)
Sortie < J7
(%)
T.A. Iseli et al., 2009
(10)
,
n = 54
70
10
6
62
B.A. Boudreaux et al., 2009
(11)
,
n = 35
62
3
14 % réanimation
6
80
E.J. Moore et al., 2009
(12)
,
n = 45
53
31
0
75
SNG : sonde naso-gastrique.

DOSSIER THÉMATIQUE
oncologique. Il serait ainsi plus aisé de s’affranchir
d’une voie d’abord cervicale plus ou moins associée
à une mandibulotomie et à une section de lèvre,
étape espérée dans le cadre du développement de
la chirurgie minimale invasive à l’aide d’un robot.
Le développement d’un monoport permettant
d’introduire les instruments et la caméra par un
même orifi ce serait susceptible d’améliorer l’accès
au pharynx. L’avènement d’optiques souples et d’une
plus grande miniaturisation des instruments irait
dans le même sens.
L’utilisation du robot peut être couplée à une chirurgie
de reconstruction soit par des lambeaux locaux,
soit par des lambeaux libres microanastomosés.
E.M. Genden et al. (9) ont décrit différents lambeaux
de voisinage réalisables par une intervention robotisée
pour combler des défects après exérèse tumorale :
lambeaux d’avancement muqueux de pharyngo-
plastie, aux niveaux du sinus piriforme ou du mur
pharyngé postérieur. J.C. Selber et al. ont publié
récemment une série de 8 reconstructions robot-
assistées comprenant 5 lambeaux libres dont les
microanastomoses ont été réalisées à l’aide du robot,
sans échec ni reprise pour thrombose (16). Tous les
patients ont justifi é d’une trachéotomie compte tenu
de l’étendue de l’exérèse, mais aucun n’a justifi é d’un
abord translabial ou transmandibulaire. Les auteurs
n’ont pas observé de fi stule et chaque patient a été
décanulé et a repris une alimentation per os.
Les diffi cultés
Il est nécessaire d’évaluer le service médical rendu
par cet outil très récemment mis en place dans nos
hôpitaux et cliniques. Dans notre spécialité, une
coordination nationale des utilisateurs de ce robot,
soutenu par le Groupe d’étude des tumeurs tête
et cou (GETTEC), a permis la création d’un obser-
vatoire et d’un programme cohérent de recherche
clinique et de qualité et gestion des risques (7). Le
robot est souvent partagé entre plusieurs spécia-
lités et, parfois, il est même utilisé par plusieurs
établissements de soins. Cela peut générer des
diffi cultés d’organisation, de programmation, et
conduire à des délais de prise en charge allongés.
Ces données doivent être maîtrisées lors de la
mise en place d’une chirurgie robotisée. Enfi n, une
évaluation médico-économique doit être réalisée
puisque à ce jour aucune étude n’a été publiée sur
ce sujet. À l’achat, le robot coûte plus de 2 millions
d’euros et, pour chaque intervention, 800 euros de
consommables sont utilisés. Il faut donc évaluer si
ce surcoût est compensé par des durées d’hospita-
lisation plus courtes qu’avec une chirurgie classique
et une radio-chimiothérapie. Un projet de soutien
aux technologies innovantes et coûteuses (STIC)
est en cours pour réaliser cette étude.
Conclusion
Le développement de la télérobotique en chirurgie
des VADS est, sans nul doute, une étape importante
dans l’essor de la spécialité dans les années à venir.
La grande maniabilité des instruments, l’excellente
exposition des tumeurs, le confort opératoire pour
le chirurgien et l’amélioration des suites opératoires
expliquent le succès mondial de cette nouvelle
approche chirurgicale depuis 4 ans. De nombreuses
équipes françaises envisagent de pratiquer à leur
tour cette chirurgie dans les prochaines années. La
constitution d’un groupe français de chirurgie téléro-
botisée en ORL, dès ses débuts, a permis de réunir
toutes les équipes qui le souhaitaient (actuellement
au nombre de 8). Ce groupe propose des formations
et peut aussi aider les équipes qui veulent débuter.
Il a également pour but de colliger le maximum
de données cliniques relatives aux patients traités
pour pouvoir publier et présenter les résultats
fonctionnels et carcinologiques sur un grand nombre
d’interventions dans les prochaines années. ■
1. Piquet JJ. Functional laryngectomy (cricohyoidopexy).
Clin Otolaryngol Allied Sci 1976;1(1):7-16.
2. Ambrosch P, Kron M, Steiner W. Carbon dioxide laser
microsurgery for early supraglottic carcinoma. Ann Otol
Rhinol Laryngol 1998;107(8):680-8.
3. Hockstein NG, O’Malley BW Jr, Weinstein GS. Assess-
ment of intraoperative safety in transoral robotic surgery.
Laryngoscope 2006;116(2):165-8.
4. McLeod IK, Melder PC. Da Vinci robot-assisted exci-
sion of a vallecular cyst: a case report. Ear Nose Throat J
2005;84(3):170-2.
5. O’Malley BW Jr, Weinstein GS, Snyder W, Hockstein
NG. Transoral robotic surgery (TORS) for base of tongue
neoplasms. Laryngoscope 116(8):1465-72.
6. Weinstein GS, O’Malley BW Jr, Snyder W, Sherman E,
Quon H. Transoral robotic surgery: radical tonsillectomy.
Arch Otolaryngol Head Neck Surg 2007;133(12):1220-6.
7. Mallet Y, Morinière S, Ceruse P, El Bedoui S. New challenge
in head and neck oncology surgery: the transoral robotic
surgery. Bull Cancer 2010;97(1):97-105.
8. Weinstein GS, O’Malley BW Jr, Desai SC, Quon H. Tran-
soral robotic surgery: does the ends justify the means? Curr
Opin Otolaryngol Head Neck Surg 2009;17(2):126-31.
9. Genden EM, Desai S, Sung CK. Transoral robotic surgery
for the management of head and neck cancer: a preliminary
experience. Head Neck 2009;31(3):283-9.
10. Iseli TA, Kulbersh BD, Iseli CE, Carroll WR, Rosenthal EL,
Magnuson JS. Functional outcomes after transoral robotic
surgery for head and neck cancer. Otolaryngol Head and
Neck Surg 2009;141(2):166-71.
11. Boudreaux BA, Rosenthal EL, Magnuson JS et al. Robot-
assisted surgery for upper aerodigestive tract neoplasms.
Arch Otolaryngol Head Neck Surg 2009;135(4):
397-401.
12. Moore EJ, Olsen KD, Kasperbauer JL. Transoral robotic
surgery for oropharyngeal squamous- cell carcinoma: a
prospective study of feasibility and functional outcomes.
Laryngoscope 2009;119(11):2156-64.
13. Laccourreye L, Garcia D, Ménard M, Brasnu D, Laccour-
reye O, Holsinger FC. Horizontal supraglottic partial laryn-
gectomy for selected squamous carcinoma of the vallecula.
Head Neck 2008;30(6):756-64.
14. Remacle M, Lawson G, Hantzakos A, Jamart J. Endoscopic
partial supraglottic laryngectomies: techniques and results.
Otolaryngol Head Neck Surg 2009;141(3):374-81.
15. Solares CA, Strome M. Transoral robot-assisted CO2
laser supraglottic laryngectomy: experimental and clinical
data. Laryngoscope 2007;117(5):817-20.
16. Selber JC. Transoral robotic reconstruction of
oropharyngeal defects: a case series. Plast Reconstr Surg
2010;126(6):1978-87.
Références bibliographiques
1
/
4
100%