microbiologie analytique

!"#$%&$"%'%(")*+,+'-."/0)*1+0'23."),,)*4%,.+,5%,*6)!)6.$)*7*
*
8*
!
"#$%&'!()*+,)*-!+.(-!
/%0/1%123#4'!!
2%15136!7%#$/8'!(9*-!82!+:*-!+.(-!
/%0&842123#4!2%15136'!;*9,+.*9!+.(-!
!
(<!=3"%#>3#6#738!1416?23@$8A!+<!2%15136!B8!7%#$/8!C<!2%15136!/8%ᆆ!D68"2$%8!B8!B8$E!1%23"68&<!-<!8E1=84!-.!
=34$28&!+!@$8&23#4&!&$%!C!#$!C!@$8&23#4&!&$%!-!F!B0586#//8%!158"!28&2!82!&"G0=1&!D(!/178!,!(!/178!82!B8=3!/1%!
@$8&23#4<!H!@$8&23#4&!#I!#4!B#32!/1%68%!B8!6J1%23"68!B$!2%15136!/8%ᆆ!KL!@$8&23#4!&$%!68!2%15136!B8!7%#$/8'!
"328%! 82! %0&$=8%! 6J1%23"68! #$! 68! B#=1348M! D232%8A! /%0&842123#4! 84! (! 63748A! /%0&842123#4! B8&! =02G#B8&! 68&! /6$&!
"#$%1428&A!%0&$6212&A!"#4"6$&3#4<!
!
"#$%%&'('!/1$6,8238448*=#4214B#4N5328#&*"G!
!
)*!+,-%#.$"-&#,!
)*/!0%12',-3-&#,!.$!"#$%2!
!
• O42%#B$"23#4!
– P8!61!>3#28"G4#6#738!F!61!
=3"%#>3#6#738!=#B8%48!
– QR$2363&123#4!B8&!=3"%##%7143&=8&!!
• Q1!/%#>60=123@$8!B8&!B0"G82&!
– Q1!78&23#4!B8&!B0"G82&!
– Q8!2%1328=842!B8&!B0"G82&!
o QR34"340%123#4!
o Q1!=3&8!84!B0"G1%78!
o Q1!>3#%0=0B3123#4!
o QR0/$%123#4!B8&!81$E!
• S//%#"G8!1416?23@$8!
– S416?&8!>1"20%3#6#73@$8!
– S416?&8!"G3=3@$8!
• T/$%123#4!412$%8668!82!>3#%0=0B3123#4!
– T/$%123#4!B14&!$4!&?&2U=8!V1%&23@$8!
– Q1!B07%1B123#4!B8&!G?B%#"1%>$%8&!
B14&!$4!&328!"#421=340!W!$4!
– /%#"8&&$&!=$623/G1&3@$8!
• Q1!>3#B07%1B123#4!
– Q8&!G?B%#"1%>$%8&X!
− Q8&!G?B%#"1%>$%8&!
1%#=123@$8&!W!68!2#6$U48!
− Q8&!G?B%#"1%>$%8&!
G16#7040&!
– Q8&!"#=/#&0&!/#6?"?"63@$8&!
1%#=123@$8&!
– P0586#//8=842!B8!4#$58668&!
&#$"G8&!>1"20%38448&!
• Q8&!>3#&84&8$%&!
– P028"23#4!B8!6R1%&843"!
– P028"23#4!B8!&$>&214"8&!/8%2$%>142!
68!&?&2U=8!84B#"%34384!
!
)*/*)!4%353&(!',!6%#$7'!'-!-%353&(!7'%2#,,'(!
!
Q8!2%15136!F!8YY8"2$8%!/1%!7%#$/8!B8!"34@!02$B3142&!"#4&3&28!F!"G#3&3%!$4!B#=1348!/1%=3!"8$E!
/%#/#&0&A!F!63%8!68&!1%23"68&!B#440&!82!F!/%0&8428%!$48!&?42GU&8!&#$&!61!Y#%=8!BR$4!B31/#%1=1!F!
=#42%8%!F!5#&!"#66U7$8&*!
• Q8!B31/#%1=1!"#=/%84B%1!68&!&8"23#4&!&$351428&!'!
1* Z32%8!B$!B#=1348!158"!68!4#=!B8&!02$B3142&!
>* O42%#B$"23#4!2G0=123@$8!
"* P8&"%3/23#4!B8&!/%34"3/168&!=02G#B8&!
B* [0&$6212&!
8* \#4"6$&3#4!
Y* [0Y0%84"8&!>3>63#7%1/G3@$8&!
• Q8&!B#=1348&!/%#/#&0&!Y37$%842!B14&!$48!63&28!1448E08*!
Q8!2%15136!/8%ᆆ!"#=/%84B!61!68"2$%8!B8!B8$E!1%23"68&!&8!%1//#%2142!B3%8"28=842!F!61!=123U%8!
2%13208!B14&!68!"#$%&*!O6!&R1732!B8&!1%23"68&!+!82!C!@$3!Y37$%842!B14&!61!63&28!1448E08*!Q8&!2%151$E!
/8%ᆆ!82!84!7%#$/8!/8$5842!Y13%8!6J#>]82!BJ$48!@$8&23#4!F!6J8E1=84*!

!"#$%&$"%'%(")*+,+'-."/0)*1+0'23."),,)*4%,.+,5%,*6)!)6.$)*7*
*
9*
)*)!8'!(3!9&#-'":,#(#6&'!;!(3!<&"%#9&#(#6&'!<#.'%,'!
!
Q1! >3#28"G4#6#738! 48! /%#53842! /1&! BJ$4!!
B0586#//8=842! %0"842*! Q8&! =3"%##%7143&=8&!
#42!020!$2363&0&!!B8/$3&!6#4728=/&!/#$%!/%#B$3%8!
B8&!163=842&A!286&!@$8!61!>3U%8A!68!534A!68!534137%8A!
68&! ?#7G#$%2&! 82! 68&! Y%#=178&*! =3!
9&#-'":,#(#6&'! '2-! .#,"! (>',2'<9('! .'2!
<1-:#.'2! #$! .'2! -'":,&?$'2! $-&(&23,-! .'2!
1(1<',-2! .$! 5&53,-! @#%63,&2<'2A! "'(($('2A!
1(1<',-2! 2$9B"'(($(3&%'2! #$! <#(1"$('2C! 7#$%!
%'":'%":'%A!7%#.$&%'!#$!<#.&D&'%!.'2!1(1<',-2!
#$!#%63,&2<'2!.>#%&6&,'!3,&<3('!#$!5161-3('*!!
^$86@$8&!8E8=/68&'!
• Q8&!_$=0%384&!#42!3458420!61!>3U%8!
DC...,+...!14&!15*!`\<!
• Q8&![#=134&!"#4413&&13842!61!>3U%8!82!68!
534!
Q1!Y1>%3"123#4!B8!61!>3U%8!"#4&3&28!2#$2!BR1>#%B!
F!2%14&Y#%=8%!68&!76$"3B8&!B8&! 7%134&!BR#%78!84!
$4! &$>&2%12! /#$%! 61! Y8%=842123#4! Da37*! (<*!
_$35842! 68&! 021/8&! B8! =162178A! BR1BB323#4! B8!
G#$>6#4! 82! B8! 61! "$3&A!@$3! 341"2358! 68&!
84b?=8&!B8!=162178!82!1&&$%8!$48!"61%3Y3"123#4*!!
Q1!Y8%=842123#4!&$%53842!84&$328!7%c"8!F!6J1]#$2!
B8!685$%8&*!
!
!
!
• QJ02G14#6!'!"J8&2!61!/%8=3U%8!&$>&214"8!"G3=3@$8!/%#B$328!/1%!61!>3#28"G4#6#738*!QJ#%37348!B8!
61! B3&2366123#4! BJ$48! $23#4! 16"##63@$8! %8=#428! 1$! (-U=8! &3U"68*! T4! 8YY82A! 68&! Y%14d13&!
/%#B$3&13842!B0]F!B$!"#741"!82!68&!0"#&&13&!#42!1//%3&!F!B3&23668%!68$%!>3U%8!/#$%!/%0/1%8%!B$!
efG3&V?! B8&! Y%14d13&! g*! +9! h! B8! 61! /%#B$"23#4! 1"2$8668! 84! 02G14#6! /%#53842! B8! 61!
>3#28"G4#6#738*!
• (;;)'! S42#348! 514! Q88$f84G##V! #>&8%58! B8&! !"#$%&'()!DB8&! i! 143=163"$68&! g<! 158"! $4!
=3"%#&"#/8*!
• ();9'!j21>63&&8=842!B8&!6#3&!B8!*+,%&%-'$%!Dk84B86<!
• S$!(:8!&3U"68A!l1&28$%!=#42%8!@$8!68&!685$%8&!"#458%23&&842!68&!&$"%8&!84!16"##6!84!1>&84"8!
E&6$%'!)!!(3!D39%&"3-&#,!.'!(3!9&F%'!

!"#$%&$"%'%(")*+,+'-."/0)*1+0'23."),,)*4%,.+,5%,*6)!)6.$)*7*
*
:*
BJ13%*! K4! B0"#$5%8! @$8! 6J137%8$%! B$! 534A! @$3! &$%53842! 1/%U&!61! .(&/(0$"$'10!"*#11*'23(A! 8&2!
B$8!F!6J1"235320!B8!>1"20%38&!@$3!/%#B$3&842!B8!6J1"3B8!1"023@$8A!"#458%23&&142!134&3!6J16"##6!84!
534137%8*!
• l1&28$%! =#42%8! 07168=842! @$8! 68! "G1$YY178! B8! 6J16"##6! /8%=82! B8! B02%$3%8! "8&! =3"%#,
#%7143&=8&! D4")$(3&')"$'10<*! Q8&! =3"%#,#%7143&=8&! 34Y8"238$E!*! 1$&&3! 341"2350&! /1%! 61!
"G168$%*!
• a34! B$! (:U=8! ,! B0>$2! B$! +.U=8! &3U"68'!k1%234$&! m83]8%34"V! 021>632! F! 6R13B8! BR$4! Y362%8! @$8!
6R17842!/12G#7U48!B8!61!=#b1n@$8!B$!21>1"2!8&2!/6$&!/8232!@$R$48!>1"20%38*!\R8&2!68!Y#4B128$%!
B8! 61! 5'&1*16'(*! G&%$2H! 73%32&-'! "'(($(3&%'! "#<7#21! .IJ8K! #$! JLK! @5&%$2! .'! 93"-1%&'H!
93"-1%:36'C! ',-#$%1! .I$,'! "372&.'! 7%#-1&,&?$'! #$! .I$,'! ',5'(#77'! 7(32<&?$'! .'! (3!
"'(($('!:M-'!',!7($2!.'!(3!"372&.'!7%#-1&,&?$'*!
• P0>$2!B$!+.U=8!&3U"68'!_8%7$83!o34#7%1B&V3!02$B38!6R1"235320!=3"%#>38448!B$!*!O6!B0=#42%8!
@$8!B8&!>1"20%38&!-%6&"-(0$7*"!#(**3*1)(*!
• Q1! .(&/(0$"$'107 '0-3)$&'(**(!8&2! 1//1%$8! 1$! B0>$2! B$! +.U=8! 82! 1! 1228342! ! 1/#708! 1$!
"#$%&!B8!61!&8"#4B8!7$8%%8!=#4B3168!158"!61!/%#B$"23#4!B$!76?"0%#6!DY1>%3"123#4!BJ8E/6#&3Y&<A!
B8! 6J1"02#48! D=$4323#4&<A! B$! >$214#6!D"1#$2"G#$"! &?42G023@$8<*! \8&! Y8%=842123#4&! Y$%842!
1>14B#4408&!B14&!68&!14408&!(:9.*!\8&!/%#B$32&!*!1"2$8668=842!8E2%132&!B8! B0%350&!B$!
/02%#68*!
• QR1"3B8!/?%$53@$8!8&2!61!=#60"$68!B8!>1&8!B8!"8&!Y8%=842123#4&!B8!76$"3B8&'!
*
! ! E&6$%'!N!=I3"&.'!7O%$5&?$'A!<#(1"$('!7&5#-!.'!(3!D'%<',-3-&#,!.'2!6($"&.'2!
o 1"3B8!61"23@$8!8&2!/%#B$32!84!1>&84"8!BJ#E?7U48!/1%!8E8=/68!/84B142!$4!8YY#%2!
o 68&!8,!/%#B$32&!/84B142!68!"?"68!B8!p%8>&!&8!63842!F!6JK+!F!61!Y34!B8!61!"G1q48!%8&/3%12#3%8!
• (:--'!8+9:;!8&2!68!/%34"3/8!1"23Y!%8&/#4&1>68!B8!61!2%14&Y#%=123#4!"866$613%8*!
o l48$=#"#@$8! r! >1"20%38! @$3! &J02168! 84! >#q28! B8! /82%3! r!
&=##2G! D7%c"8! F! 61! Y#%=123#4! B8! "1/&$68&<! @&<36'! .$! 932C*!
L4!/48$=#"#@$8!=$2142!4J1%%358!/1&!F!/%#B$3%8!&1!/%#/%8!
"1/&$68! 16#%&! 36! Y#%=8! B8&! "#6#438&! @$3! 48! &J0216842! /1&! r!
%#$7G! @&<36'! .$! :3$-C*! S58%?! 1! =3&! B8! (IJ8K!D84238%! r!
8453%#4! -=3#! B8! >1&8&! "#42%8! C! =31! /#$%! 6JG#==8<! B8&!
&=##2G&! B14&! 68! =3638$! B8! "$62$%8! B8! %#$7G! 82! %#$7G! 8&2!
B8584$8! &=##2G*! QJSPs! 8&2! B#4"! 68! &$//#%2! B8!
6J34Y#%=123#4!704023@$8*!!
o O6&!#42!=1%@$0!B8&!53%$&!158"!B$!&#$Y%8!C9!/#$%!61!"1/&$68!82!B$!/G#&/G128!C+!/#$%!
6JSPs!82!#42!%8=1%@$0!@$J$48!Y#3&!@$8!68!53%$&!1!"#6#43&0!61!>1"20%38A!68!&#$Y%8!%8&28!
B8G#%&!82!68!/G#&/G128!842%8A!134&3!"J8&2!6JSPs!@$3!"#423842!6J34Y#%=123#4!704023@$8!
• (:-;'!T"G1478! B8! =120%386!704023@$8! 842%8!B8$E!>1"20%38&A!61!#10<36"')10!6#%&! B8! 61@$8668!
2#$2!#$!$48!/1%238!B$!704#=8!B8!6R$48!8&2!2%14&Y0%0!F!6R1$2%8!Da37*!(*-X!Q8B8%>8%7!82!Z12$=<!
o !"#$%&''!$48!>1"20%38!158"!$4!/61&=3B8!a!"%#3&08!158"!$48!>1"20%38!&14&!/61&=3B8!51!
%0/63@$8%!82!B#448%!!/61&=3B8a'!aH!E!a,!rt!aH!E!aH!

!"#$%&$"%'%(")*+,+'-."/0)*1+0'23."),,)*4%,.+,5%,*6)!)6.$)*7*
*
7*
o P,!7(32<&.'!7'$-!2I322#"&'%!;!(IJ8K!93"-1%&',H!93"-1%&'!QD%!@('!7(32<&.'!36&-!3(#%2!
"#<<'!2I&(!1-3&-!2'$(A!<3&2!3$!(&'$!.'!,'!-%3,2<'--%'!7($2!?$'!('!7(32<&.'!;!(I3$-%'!
93"-1%&'A!(3!93"-1%&'!7#$%%3!-%3,2D1%'%!-#$-!('!61,#<'*!!
o a#%=123#4!BJ$4!/36$&A!2%14&=3&&3#4!B8!++!7U48&!B#42!"8$E!@$3!/8%=822842!B8!Y13%8!$4!
/36$&A!82!B#4"!BJ8YY8"2$8%!$48!"#4]$713*!!
o 2%14&=3&&3#4!BJ$48!/1%238!B$!/61&=3B8!82!B8&!7U48&!/%#"G8!B8!"8!&328!BJ34207%123#4*!
0($2!#,!(3&22'!3(('%!"'!-%3,2D'%-!.IJ8K!'-!7($2!#,!53!-%3,2<'--%'!.'!6F,'2*!!
o Q8!2%14&Y8%2!B8!6JSPs!"#==84"8!2#$]#$%&!1$!=u=8!84B%#32A!134&3!68&!/%8=38%&!7U48&!
2%14&=3&!*!2#$]#$%&!61",2&E,716,2%/*!
o R,!7'$-!.#,"!(#"3(&2'%!?$'(!6F,'!"#.'!7#$%!?$#&!',!%'63%.3,-!"#<9&',!.'!-'<72!
#,!(3&22'!;!(3!93"-1%&'!7#$%!2'!"#,S$6$'%*!J7%F2!T!<&,$-'2A!#,!%'63%.'!('!,#$5'3$!
6F,'!&,-16%1!'-!7#$%!?$#&!&(!"#.'*!U'(3!3!7'%<&2!.'!"#,,3V-%'!"'!?$'!":3?$'!6F,'!
"#.'!":'W!X*"#(&!'-!2#,!'<7(3"'<',-!.3,2!('!61,#<'*!
!
!
!
• (:9C'!Q1!&2%$"2$%8!B8!6RSPs!1!61!Y#%=8!BR$48!-13!*(!,%*'#(!Dv12!14B!\%3"V<!
• Y&(&'$!.'2!3,,1'2!)Z[/H!.'2!2"&',-&D&?$'2!.1"#$5%',-!?$'!.'2!<&"%##%63,&2<'2!.$!2#(!2#,-!
"3739('2! .'! -%6&"-(&7 -()7 )3!)$"0#()7 =%01!'1$'23()A! ">'2-B;B.&%'! ,#,! ,3-$%'(('2! #$!
2O,-:1-&?$'2*!
• (:;:'!j6$"3B123#4!B$!#1-(!6%0%$'23(!Ds3%84>8%7A!pG#%141!14B!\%3"V<!
• )Z\]H!+2#(3-&#,!'-!<$(-&7(&"3-&#,!.'2!6F,'2!73%!"(#,36'!@E&6!)*^_!`#O'%!3,.!U#:',C!'-!,#,!
7($2!$,&?$'<',-!('!61,#<'!',-&'%a!U'(3!'2-!-%F2!$-&('a!
!

!"#$%&$"%'%(")*+,+'-."/0)*1+0'23."),,)*4%,.+,5%,*6)!)6.$)*7*
*
;*
!
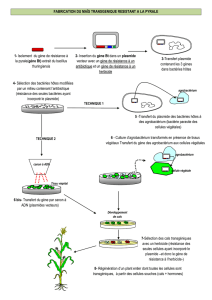
()#*+'&',-#.-,#-)/01-,#.-#2-,+2'$+'%)#3%*2#42561-)+-2#&789:"#()#*+'&',-#.-,#&'65,-,#3%*2#&'-2#&789:#
$';&-#<#*)#=-$+-*2>#,%*=-)+#*)#3&5,1'.-#.-#;5$+?2'%3@56-#$52#'-*+#,-#1*&+'3&'-2#').'='.*-&&-1-)+#
*)-#4%',#')+?62?#<#*)-#;5$+?2'-"#()#')+2%.*'+#&-#=-$+-*2#$%)+-)5)+#&789:#$';&-#.5),#*)-#;5$+?2'-"#
#
• (:w9'!>%23(0?"6(!-(!*+9:;!Dk1E1=!14B!x36>8%2X!_1478%<!
• +..C'!:%#&'4$"6(!-3!6%01/(!,3/"'0'!C.R...!7U48&A!(R...R...!/%#20348&A!&2%$"2$%8&!
&3=/68&!-+A+!h!B$!704#=8A!&0@$84"8&!%0/0208&!i!&348!g!(*)!E!(.;!"#/38&A!i!S6$!g!(*C!E!
(.;!"#/38&!D(-A(.h!704#=8<!
!
='2!.&DD1%',-'2!.1"#$5'%-'2!?$&!#,-!3<1(&#%1!(3!<&"%#9&#(#6&'!2#,-!;!"#,,3V-%'*!
!
)*N!=>$-&(&23-&#,!.'2!<&"%#B#%63,&2<'2!
!
Q8&!=3"%#,#%7143&=8&!*!$2363&0&!B8/$3&!6#4728=/&!/#$%!/%#B$3%8!B8&!163=842&!#$!B8&!&$>&214"8&!
3420%8&&1428&! /#$%!6RG#==8A!B8&!1423>3#23@$8&A! B8&!1"3B8&!1=340&A!B8&!5321=348&!82"*! QR15U48=842!
B8! 61! 704023@$8! =#60"$613%8! 1! /8%=3&! BR8453&178%! 6R8E/6#32123#4! B8&! =3"%#,#%7143&=8&! /#$%! 2#$28&!
&#%28&!BR1//63"123#4&*!
='2!93"-1%&'2A!73%!'b'<7('A!7'$5',-!c-%'!<#.&D&1'2!61,1-&?$'<',-*!P,!6F,'!1-%3,6'%!'2-!&,-%#.$&-!
.3,2! $,'! 93"-1%&'! ?$&! .'5&',-! 3(#%2! "3739('! .'! 7%#.$&%'! $,'! ,#$5'(('! 7%#-1&,'!@(I&,2$(&,'A!
(I&,-'%D1%#,! @$-&('! "#,-%'! ('! "3,"'%C! 73%! 'b'<7('CA! $,'! ',WO<'A! $,'! 2$92-3,"'! $,&?$'! #$! $,!
7#(O<F%'!9&#(#6&?$'*!!
Q8&!7U48&!BR#%7143&=8&!/12G#7U48&!#42!07168=842!020!"6#40&!/#$%!u2%8!$2363&0&!"#==8!)10-()!/#$%!
B3174#&23@$8%! B8&! =161B38&! 704023@$8&! "G8b! 6Ru2%8! G$=134! #$! B14&! 68! >02136A! #$! /#$%! /%#B$3%8! B8!
4#$581$E!5"##'0)*!
K4! /8$2!  ! B#448%! $48! /%#20348! B3%8"28=842! 82! 8668! &8%1! 3==$4#7U48! 82! B#4"! $2363&08! "#==8!
51""34A! !#4!B#448!68!/12G#7U48!B3%8"28=842!@$3!/%#B$3%1!61!/%#20348!3==$4#7U48*!
='2! <#.&D&"3-&#,2! 61,1-&?$'2! .'! <&"%#B#%63,&2<'2! 5&2',-! 3$22&! ;! 3$6<',-'%! ('2! "373"&-12!
,3-$%'(('2!.'!"'%-3&,'2!93"-1%&'2!&<7(&?$1'2!.3,2!.'2!7%#"'22$2!9&#(#6&?$'2!271"&D&?$'2*!
S34&3A!B8!4#$58668&!&#$"G8&!B8!>1"20%38&!#42!020!B0586#//08&!/#$%!-%6&"-(&!B8&!#1/41)%)!$1='23()A!
"/%*'1&(&!61!"%#3&&14"8!B8&!4*"0$()A!%*'/'0(&!B8&!'0)(#$()!34B0&3%1>68&A!-%$(#$(&!B8&!)3!)$"0#()!82"*!!
Q1!=1q2%3&8!B8&!28"G43@$8&!B8!"$62$%8&!B8&!>1"20%38&!8&2!$4!060=842!8&&842386!/#$%!B0586#//8%!"8&!
4#$58668&!&#$"G8&*!!
83,2! "'! "#$%2A! ,#$2! <#,-%#,2! 73%! ?$'(?$'2! 'b'<7('2! "#<<',-! ('2! 93"-1%&'2! .16%3.',-! .'2!
2$92-3,"'2!,3-$%'(('2!'-!b1,#9&#-&?$'2*!!
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
 53
53
 54
54
 55
55
 56
56
 57
57
 58
58
 59
59
 60
60
 61
61
 62
62
 63
63
 64
64
 65
65
1
/
65
100%