OBJECTIFS D’ENSEIGNEMENT PROFESSIONNEL CONTINU

Figure 1. Léiomyomes cutanés du bras :
multiples nodules érythémateux regrou-
pés de façon segmentaire.
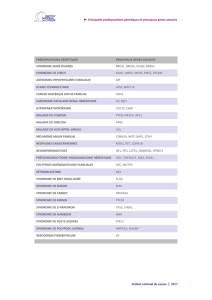
Figure 2. Fibrofolliculomes du visage :
macules, papules blanc-gris, en dômes
de surface lisse.
246 | La Lettre du Cancérologue • Vol. XX - n° 4 - avril 2011
Oncogénétique
OBJECTIFS D’ENSEIGNEMENT
PROFESSIONNEL CONTINU
* Maladie liée à l’existence d’hamartomes, lésions correspondant au développement
architectural anormal d’un tissu donné.
associée dans environ 85 %
des cas à une atteinte de
l’utérus. Les léiomyomes
utérins varient en nombre
de 10 à 20 et peuvent
mesurer de 1 à 10 cm.
L’âge moyen au diagnostic
est de 30 ans (18-53 ans).
Dans plus de 50 % des
cas, les léiomyomes
utérins conduisent à une
hystérectomie avant l’âge
de 30 ans. La léiomyo-
matose cutanée et utérine
prédispose au cancer du rein papillaire de type 2. Il s’agit de tumeurs
de haut grade, de très mauvais pronostic, souvent métastatiques
au moment du diagnostic. Dans la majorité des cas, la tumeur du
rein est solitaire et unilatérale, d’une taille allant de 3,8 à 14 cm.
L’âge moyen au diagnostic est de 44 ans ; cependant, plusieurs cas
de sujets de moins de 30 ans ont été décrits dans la littérature (16,
23, 26 et 28 ans). Le risque cumulé de cancer du rein en présence
d’une mutation délétère du gène FH varie, selon les études, de
15,6 à 24 %. Certains auteurs rapportent un risque de cancer du sein
et de cancer de la vessie, associé aux mutations du gène FH. Ces
données nécessitent d’être confi rmées. Une surveillance dermato-
logique, rénale et gynécologique doit être proposée aux patients
porteurs d’une mutation du gène FH.
Syndrome de Birt-Hogg-Dubé
De transmission autosomique dominante, le syndrome de Birt-
Hogg-Dubé est caractérisé, sur le plan dermatologique, par l’asso-
ciation de tumeurs cutanées à type de fi brofolliculomes (fi gure 2),
trichodiscomes et acrochordons (4). Ces lésions, non constantes,
apparaissent entre 30 et 40 ans. Elles prédominent sur le visage,
le cou, le haut du thorax et, parfois, le cuir chevelu. Les autres
manifestations cliniques sont des pneumothorax spontanés, des
kystes pulmonaires et des tumeurs rénales de différents types
histologiques : cancers chromophobes le plus souvent, mais aussi
oncocytomes et formes hybrides chromophobes-oncocytomes.
Les cancers du rein à cellules claires et papillaires sont rares.
Le risque de cancer du rein
est multiplié par 7, et l’âge
de survenue de la maladie
est variable. Les tumeurs
peuvent être uniques ou,
le plus souvent, bilaté-
rales et multifocales. Des
atteintes thyroïdiennes et
des polypes coliques ont
également été rapportés,
sans que leur appartenance
au spectre clinique soit
actuellement démontrée.
Une surveillance dermatologique, pulmonaire et rénale doit être
mise en place chez les patients porteurs d’une mutation du gène
BHD. Nous devons nous interroger sur la nécessité de mettre en
place une surveillance thyroïdienne et colique chez ces patients.
Références bibliographiques
1. Richard S, Joly D, Corréas JM et al. Prédispositions héréditaires au cancer rénal. Flam-
marion Médecine-Sciences éds. Actualités néphrologiques 2006:131-50.
2. Richard S, Parker F, Aghakhani N et al. Von Hippel-Lindau disease: recent advances in
genetics and clinical management. J Neuroradiol 2005;32(3):157-67.
3. Tomlinson IP, Alam NA, Rowan AJ et al. Germline mutations in FH predispose to domi-
nantly inherited uterine fi broids, skin leiomyomata and papillary renal cell cancer. Nat
Genet 2002;30(4):406-10.
4. Birt AR, Hogg GR, Dubé WJ. Hereditary multiple fi brofolliculomas with trichodiscomas
and acrochordons. Arch Dermatol 1977;113(12):1674-7.
Prédispositions génétiques
au cancer chez l’enfant
M. Gauthier-Villars
État des lieux
La plupart des cancers de l’enfant surviennent de façon sporadique, en
dehors de toute histoire familiale, et on ne retient pas de majoration
du risque chez les apparentés par rapport à la population générale.
L’existence d’une maladie génétique sous-jacente ou d’antécédents
familiaux de cancer a tout de même permis d’évoquer la possibilité
de prédispositions génétiques dans certains cas de cancer de l’enfant.
Maladies génétiques
prédisposant au cancer
Des maladies génétiques, et certaines anomalies chromosomiques,
peuvent être associées à une augmentation du risque de cancer dès
l’enfance. Cette augmentation peut être liée aux effets d’un gène
unique ou à un syndrome de gènes contigus. Le diagnostic peut
parfois être diffi cile, reposant sur l’examen soigneux du patient,
sur l’histoire médicale de ses apparentés et sur des éléments radio-
logiques, biologiques et cytogénétiques.
Ces maladies sont regroupées en trois classes :
➤
les syndromes avec des anomalies du développement diverses,
comme les prédispositions au néphroblastome (syndromes WAGR,
de Denys-Drash, de Beckwith-Wiedemann, etc.) ;
➤
les hamartomatoses*, associées à un risque tumoral très
variable d’un syndrome à l’autre et qui peut apparaître dès l’ enfance
(maladie de Cowden, syndrome de Peutz-Jeghers, etc.) ;
➤
les syndromes de fragilité chromosomique ou maladies cassantes
de l’ADN, qui sont des maladies héréditaires, de transmission auto-
somique récessive, associées à un risque accru de cancer (ataxie
télangiectasie, syndrome de Bloom, anémie de Fanconi, etc.).
Réunions présidées par :
•
Pr Bruno Chauffert et Dr Michel Ciupa ............................................................. Amiens
•
Prs Xavier Pivot et Pierre Fumoleau, Dr Thierry Altwegg ........................... Besançon/Dijon
•
Pr Dominique Jaubert ................................................................................ Bordeaux
•
Drs Gilles Robinet, Hervé Léna, Jean-Philippe Metges
et Laurent Miglianico ....................................................................... Bretagne/Lorient
•
Pr Pierre Kerbrat, Drs Anne-Claire Hardy-Bessard et Marc Spielmann ........ Bretagne/Vannes
•
Pr Jean-Marc Nabholtz .................................................................... Clermont-Ferrand
•
Prs Antoine Adenis et Mohamed Hebbar ................................................................ Lille
•
Pr Véronique Trillet-Lenoir et Dr Claire Garnier-Tixidre ......................... Lyon/Saint-Exupéry
•
Prs Jean-François Seitz, Patrice Viens et Fabrice Barlesi.................................... Marseille
•
Prs Marc Ychou et Jean-Louis Pujol, Dr André Mathieu .................................. Montpellier
•
Pr Thierry Conroy .......................................................................................... Nancy
•
Pr François-Régis Bataille .............................................................................. Nantes
•
À venir .......................................................................................................... Niort
•
Pas de président .............................................................................................. Pau
•
Prs Yacine Merrouche et Jean-Marc Phelip, Dr Nicolas Mottet ...................... Saint-Étienne
•
Drs Laurent Gasnault et Hassan Rhliouch .................................................... Saint-Omer
•
Prs Jean-Pierre Bergerat et Patrick Dufour ................................................... Strasbourg
•
À venir ..................................................................................................... Toulouse
•
Prs Philippe Bougnoux et Gilles Body .................................................................. Tours
Tours
Lille
Saint-Omer
Lyon/Saint-Exupéry
Bretagne/Vannes
Montpellier
Nancy
Strasbourg
Bordeaux
Marseille
Besançon/
Dijon
Nantes
Bretagne/Lorient
29 juin 2011
22 juin 2011
21 juin 2011
28 juin 2011
À venir
30 juin 2011
5 juillet 2011
21 juin 2011
30 juin 2011
30 juin 2011
Amiens
Paris
21 juin 2011
Clermont-Ferrand
Saint-Étienne
Niort
28 juin 2011
21 juin 2011
30 juin 2011
Toulouse
Pau
29 juin 2011
28 juin 2011
29 juin 2011
21 juin 2011
29 juin 2011
"Attention : ceci est un compte-rendu de congrès dont l'objectif est de fournir des informations sur l'état actuel de la recherche ;
ainsi, les données présentées sont susceptibles de ne pas être validées par les autorités françaises et ne doivent donc pas être mises en pratique."
"Ces informations sont sous la seule responsabilité des auteurs et du directeur de la publication qui sont garants de l’objectivité de cette publication."
Vos rendez-vous
régionaux post-Chicago
avec le soutien institutionnel de

248 | La Lettre du Cancérologue • Vol. XX - n° 4 - avril 2011
Oncogénétique
OBJECTIFS D’ENSEIGNEMENT
PROFESSIONNEL CONTINU
Prédispositions génétiques au cancer
chez l’enfant sans maladie associée
L’apparition d’une tumeur à un âge très jeune, la plurifocalité
de lésions primitives, la survenue de tumeurs multiples chez un
même individu et les antécédents familiaux de cancer sont des
éléments qui suggèrent une prédisposition génétique. L’histoire
familiale se montre extrêmement précieuse pour identifi er des
prédis positions à des cancers obéissant à un mode de transmission
simple, mono génique, dominant et à forte pénétrance. La proba-
bilité pour qu’une même tumeur (surtout s’il s’agit d’une tumeur
rare) survienne chez des apparentés de façon fortuite est faible :
une prédisposition génétique sera donc évoquée d’emblée dans un
tel cas. C’est l’observation de formes familiales de rétinoblastomes,
le plus souvent bilatéraux, qui a permis à A.G. Knudson, en 1972,
de proposer un modèle de prédisposition au rétinoblastome se
transmettant sur un mode autosomique dominant associé à
une pénétrance élevée. Cette théorie des deux événements (une
mutation constitutionnelle sur un allèle et une mutation acquise
sur le deuxième allèle du gène au niveau tumoral) a été confi rmée
par la suite, lors de l’identifi cation de mutations constitutionnelles
monoalléliques du gène RB1 chez des patients atteints de rétino-
blastomes bilatéraux (1).
La situation est plus diffi cile à appréhender lorsqu’il existe chez des
enfants apparentés plusieurs cas de tumeurs de sites différents. Ce
sont les études épidémiologiques qui ont pu mettre en évidence ici
la réalité de certaines associations tumorales. On peut ainsi citer
l’exemple de l’étude de F.P. Li et J.F. Fraumeni qui, en reprenant les
dossiers cliniques et l’histoire familiale de 700 cas de rhabdomyo-
sarcomes de l’enfant, ont pu mettre en évidence quatre familles
présentant au moins deux cas de cancers rares survenant chez
des sujets jeunes apparentés au premier ou au second degré (2).
On a mis en évidence depuis des mutations constitutionnelles
mono alléliques du gène TP53, à l’origine de ce syndrome (3).
À partir du registre des tumeurs du Royaume-Uni, et en repérant
un certain nombre de maladies génétiques associées à un risque
tumoral ainsi que des histoires familiales évocatrices de prédis-
positions génétiques connues, S.A. Narod et al. ont estimé que
4,2 % des tumeurs de l’enfant étaient liées à une prédisposition
génétique (4). Ils notaient cependant que cette fréquence était
probablement sous-estimée, sachant qu’il restait à mettre en
évidence des prédispositions associées à des modes de transmission
plus complexes que ceux identifi és jusqu’alors.
Faits nouveaux
Il est clair, maintenant, que des situations plus complexes restent
à mettre en évidence dans le cadre de prédispositions génétiques
déjà connues ou avec l’identifi cation de gènes dont les altérations
ne causeraient, isolément, qu’une faible augmentation du risque
tumoral, mais pourraient, en interagissant avec d’autres gènes de
susceptibilité, entraîner un risque tumoral élevé.
Risque tumoral chez l’enfant
dans le cadre de prédispositions
au cancer de l’adulte
Récemment, deux syndromes de prédisposition au cancer de
l’enfant ont été identifi és dans le cadre de syndromes de prédis-
position aux cancers touchant l’adulte. Dans chacun, il existe un
risque tumoral particulier chez l’enfant, associé à une inactivation
constitu tionnelle biallélique de gènes dont les mutations constitu-
tionnelles monoalléliques sont associées à des risques tumoraux
différents chez l’adulte. Ainsi, il a été identifi é des altérations
bialléliques de BRCA2 chez des enfants atteints d’une anémie de
Fanconi rare de type D1 associée à un risque tumoral particulier
touchant le jeune enfant (le diagnostic d’anémie de Fanconi pouvant
être méconnu lors du premier diagnostic tumoral) [5]. Ces enfants
peuvent être atteints dans les premiers mois de la vie de néphro-
blastome, de médulloblastome, de neuroblastome et d’hémopathie.
Les mutations constitutionnelles monoalléliques du gène BRCA2
sont associées à un risque élevé de cancer du sein ou de l’ovaire
chez l’adulte. De même, il a été identifi é un risque d’hémopathie et
de tumeur cérébrale touchant les enfants porteurs d’inactivations
bialléliques des gènes du système MMR (6). Les mutations constitu-
tionnelles monoalléliques de ces gènes sont décrites dans le cadre
du syndrome de Lynch (anciennement HNPCC) et sont associées
à un risque élevé de cancer du côlon et de l’utérus chez l’adulte. Il
s’agit de situations rares, du fait de la faible fréquence des mutations
hétérozygotes de ces gènes dans la population générale et d’une
possible mortalité embryonnaire ou fœtale. Elles peuvent apparaître
dans le cadre de familles consanguines. Ce type de prédisposition
génétique peut être évoqué devant l’atteinte tumorale de plusieurs
enfants dans une même fratrie. Si la pénétrance de ces prédispo-
sitions est élevée chez les adultes, elle n’est pas complète, et les
antécédents de cancer peuvent manquer dans les deux branches
parentales, surtout lorsque les parents sont jeunes. Ces différents
syndromes viennent en diagnostic différentiel du syndrome de Li
et Fraumeni, qui était jusqu’ici la seule prédisposition génétique
évoquée devant une histoire familiale de cancers chez l’enfant.
Prédispositions plus complexes
Pour certaines tumeurs, des cas familiaux ont été décrits, mais dans
une proportion beaucoup plus faible que pour le rétinoblastome. Le
lien entre les apparentés atteints est souvent éloigné, du fait d’une
pénétrance faible. Il a été ainsi retenu que les formes familiales de
neuroblastome sont compatibles avec une transmission dominante
associée à une faible pénétrance de l’ordre de 10 % (7).
Un nouveau gène de prédisposition au médulloblastome a été
récemment mis en évidence : le gène SUFU, qui appartient à la voie
de signalisation Sonic Hedgehog (SHH) [8]. C’est la découverte
de mutations constitutionnelles du gène PTCH dans le syndrome
de Gorlin (qui associe des anomalies du développement et un
risque de médulloblastome plutôt de type desmoplastique) qui
a permis de mettre en évidence le fait que les gènes intervenant

La Lettre du Cancérologue • Vol. XX - n° 4 - avril 2011 | 249
OBJECTIFS D’ENSEIGNEMENT
PROFESSIONNEL CONTINU
dans la voie SHH, déjà impliqués dans des syndromes comportant
des troubles du développement neurologique, pouvaient avoir un
rôle dans la tumorigenèse. Dans une série de 46 cas sporadiques
de médulloblastomes, trois mutations constitutionnelles du gène
SUFU (6,5 %) ont été identifi ées dans trois cas de médulloblastome
desmoplastique. De rares cas de familles avec une atteinte chez
des cousins germains ont été rapportés, ce qui suggère un mode de
transmission complexe, multigénique, multifactoriel associant, par
exemple, des altérations épigénétiques et des altérations survenant
au cours du développement.
Les prédispositions identifi ées à ce jour correspondent à un déter-
minisme génétique simple avec un mode de transmission dominant.
Actuellement, une vingtaine de prédispositions génétiques sont
connues, pour lesquelles un test génétique peut être proposé
chez l’enfant. Cependant, de nouvelles prédispositions sont en
train d’émerger, associées à des risques tumoraux moindres ; mais
les situations liées à une transmission récessive sont diffi ciles à
mettre en évidence avec des atteintes individuelles ou de fratrie.
L’identifi cation de ces prédispositions génétiques est importante
pour comprendre la pathogenèse de ces cancers, mais elle doit
être guidée par l’amélioration de la prise en charge de l’enfant
lui-même d’une part et de sa famille d’autre part.
Références bibliographiques
1. Lohmann DR. RB1 gene mutations in retinoblastoma. Hum Mutat 1999;14:283-8.
2. Li FP, Fraumeni JF Jr. Soft-tissue sarcomas, breast cancer, and another neoplasms.
A familial syndrome? Ann Intern Med 1969;71:747-52.
3. Frebourg T, Abel A, Bonaïti-Pellié C et al. Li-Fraumeni syndrome: update, new data and
guidelines for clinical management. Bull Cancer 2001;88(6):581-7.
4. Narod SA, Stiller C, Lenoir GM. An estimate of the heritable fraction of childhood
cancer. Br J Cancer 1991;63:993-9.
5. Howlett NG, Taniguchi T, Olson S et al. Biallelic inactivation of BRCA2 in Fanconi
anemia. Science 2002;297:606-9.
6. Bougeard G, Charbonnier F, Moerman A et al. Early onset brain tumor and lymphoma
in MSH2-defi cient children. Am J Hum Genet 2003;72:213-6.
7. Shojaei-Brosseau T, Chompret A, Abel A et al. Genetic epidemiology of neuroblastoma:
a study of 426 cases at the Institut Gustave-Roussy in France. Pediatr Blood Cancer
2004;42:99-105.
8. Taylor MD, Liu L, Raffel C et al. Mutations in SUFU predispose to medulloblastoma.
Nat Genet 2002;31:306-10.
Oncogénétique
des tumeurs endocrines
A.P. Gimenez-Roqueplo
État des lieux
Les tumeurs neuro-endocrines sont un groupe hétérogène de
tumeurs développées aux dépens de cellules endocrines situées
au niveau de l’hypophyse, de la thyroïde, de la parathyroïde, du
pancréas, de la glande surrénale, du tractus digestif et de l’appareil
respiratoire. Elles surviennent parfois dans un contexte familial et
peuvent être génétiquement déterminées. Dans les formes hérédi-
taires, que l’on appelle communément néoplasies endocriniennes
multiples (NEM), la maladie est le plus souvent syndromique,
les tumeurs sont souvent multiples et peuvent toucher plusieurs
glandes, voire différents tissus.
Différents types de NEM, dont le diagnostic moléculaire est
désormais possible, ont été identifi és (tableau III) : la NEM de
type 1, secondaire à des mutations sur le gène MEN1, associe
tumeur hypophysaire, hyperparathyroïdie et tumeur endocrine du
pancréas ; la NEM de type 2, secondaire à des mutations activatrices
du proto-oncogène RET, associe carcinome médullaire de la thyroïde
et hyperparathyroïdie ; le complexe de Carney, secondaire à des
mutations perte-de-fonction sur le gène PRKAR1A, associe hyper-
plasie nodulaire pigmentée de la glande surrénale responsable d’un
syndrome de Cushing, tumeur de la thyroïde, hyperparathyroïdie,
myxome cardiaque et myxome cutané ; la maladie de von Hippel-
Lindau (VHL), secondaire à des mutations perte-de-fonction sur
le gène suppresseur de tumeur VHL, associe phéochromo cytome,
paragangliome, hémangioblastome du système nerveux central
et de la rétine, kyste rénal, cancer du rein et tumeur du pancréas ;
la forme familiale d’adénome hypophysaire, secondaire à des
mutations sur le gène AIP, associe acromégalie et adénome à
prolactine chez un même sujet ou chez deux sujets apparentés ;
le syndrome phéochromocytome-paragangliome héréditaire,
Tableau III. Principales néoplasies endocriniennes multiples dont le diagnostic génétique est disponible dans certains laboratoires d’onco-
génétique.
Néoplasies endocriniennes multiples (NEM) Principales tumeurs associées Gènes
NEM 1 Tumeur hypophysaire, hyperparathyroïdie, tumeur endocrine du pancréas MEN1
NEM 2 Carcinome médullaire de la thyroïde, hyperparathyroïdie, phéochromocytome RET
Complexe de Carney Myxome cardiaque, adénome surrénalien, tumeur testiculaire, adénome hypophysaire,
tumeur thyroïdienne, schwannome mélanocytique, kyste et adénome ovarien
PRKAR1A
Maladie de von Hippel-Lindau Phéochromocytome, paragangliome, hémangioblastome rétinien et du système
nerveux central, tumeur du pancréas, cancer du rein
VHL
Adénome hypophysaire familial Adénome hypophysaire sécrétant ou non sécrétant AIP
Paragangliome/phéochromocytome
héréditaire
Paragangliome de la tête et du cou (glomus carotidien, vagal, tympano-jugulaire),
paragangliome thoraco-abdomino-pelvien, phéochromocytome
SDHD,
SDHB
SDHC
1
/
3
100%