U Rétinoblastome bilatéral Cas clinique Bilatérel retinoblastoma

Images en Ophtalmologie
•
Vol. VII
•
n
o
6
•
novembre-décembre 2013
168
Tableau. Classifi cation internationale IRC pour la réponse à la chimiothérapie.
Groupe A Petites tumeurs rétiniennes (≤ 3 mm) ; > 3 mm de la fovéa ; < 1,5 mm du nerf
optique
Groupe B Tumeurs rétiniennes (> 3 mm) quelle que soit leur localisation, avec un
décollement sérieux rétinien localisé (≤ 6 mm du bord de la tumeur)
Groupe C Essaimage vitréen et/ou sous-rétinien localisé (< 6 mm du bord de la tumeur)
S’il existe plusieurs sites, la totalité des sites doit être < 6 mm
Groupe D Essaimage vitréen et/ou sous-rétinien localisé (> 6 mm du bord de la tumeur)
S’il existe plusieurs sites, la totalité des sites doit être ≥ 6 mm
Liquide sous-rétinien > 6 mm du bord de la tumeur
Groupe E Essaimage vitréen et/ou sous-rétinien localisé (> 6 mm du bord de la tumeur)
S’il existe plusieurs sites, la totalité des sites doit être ≥ 6 mm
Liquide sous-rétinien > 6 mm du bord de la tumeur
Pas de potentiel visuel ou présence d’un ou de plusieurs éléments suivants :
– tumeur dans le segment antérieur ;
– tumeur au niveau du corps ciliaire ;
– glaucome néovasculaire ;
– hémorragie intravitréenne massive masquant la tumeur, ou hyphéma important ;
– œil en phtyse ;
– aspect pseudo-infl ammatoire orbitaire
Cas clinique
Rétinoblastome bilatéral
Bilatérel retinoblastoma
C. Bonnet, F. Chaalal, L. Lumbroso-Le Rouic
(Service d’ophtalmologie et d’anatomie pathologique, institut Curie, Paris)
Une enfant âgée de 4 ans, sans antécédents particuliers, née de parents
consanguins, est amenée en consultation pour leucocorie de l’œil droit
depuis 2 mois.
Examen ophtalmologique
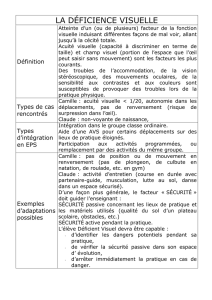
Le fond d’œil retrouve un décollement de rétine total à droite, avec une masse implantée
en antérieur et en nasal, blanche, crayeuse, intrarétinienne, avec calcifi cations intra-
tumorales occupant plus de la moitié de la rétine
(fi gure1)
.
Le fond d’œil à gauche retrouve 4tumeurs blanches, de petite taille, dans la périphérie
des 4quadrants.
L’aspect du fond d’œil, avec présence de tumeurs caractéristiques, est celui d’un
rétino blastome bilatéral, classé groupeVbE à droite, IVaB à gauche (classifi cation
de Reese-Ellsworth et classifi cation internationale).
Bilan d’extension
L’IRM encéphalique et orbitaire avec coupes fi nes sur le nerf optique montre une
absence d’extension extraoculaire
(fi gure2)
.
Conduite à tenir
Compte tenu du décollement de rétine total et de la taille de la tumeur, une énucléation
de l’œil droit est réalisée d’emblée
(1)
[fi gure3]
. Le résultat de l’analyse anatomo-
pathologique confi rme le diagnostic de rétinoblastome moyennement différencié, avec
calcifi cations intratumorales
(fi gure4)
. La sclère ainsi que le nerf optique sur tout son
trajet sont indemnes, de même que les gaines méningées. En revanche, il existe une
atteinte du corps ciliaire antéronasal et une infi ltration focale choroïdienne.
Leucocorie • Rétinoblastome
bilatéral.
Leucokoria • Bilateral retino-
blastoma.
Légendes
Figure 1. Fond d’œil droit montrant une
volumineuse masse crayeuse qui occupe plus
de la moitié inférieure de la rétine (fl èche),
associée à un décollement séreux total (*).
Figure 2. IRM encéphalique montrant un
hypersignal T1 intraoculaire à droite (*), sans
envahissement extrascléral.
Figure 3. Aspect macroscopique retrouvant
une volumineuse masse blanchâtre intra-
rétinienne.
Figure 4. Aspect microscopique retrouvant
des calcifi cations intratumorales (*)
.
Figure 5. Facteurs de mauvais pronostic.
a. Atteinte du corps ciliaire antérieur (fl èche).
b. Atteinte choroïdienne focale (tête de
fl èche). Notez le décollement associé (fl èche).

Images en Ophtalmologie
•
Vol. VII
•
n
o
6
•
novembre-décembre 2013
169
1
3
4
5a
5b
Corps ciliaire
Choroïde
Rétine
2
**
**
**

C. Bonnet et L.Lumbroso-LeRouic déclarent
nepas avoir de liens d’intérêts.
F.Chaalal n’a pas précisé
ses éventuels liens d’intérêts.
Cas clinique
À gauche, on réalise un traitement conservateur par une association de
chimiothérapie et de thermothérapie par laser diode.
Discussion
Le rétinoblastome doit être évoqué devant toute leucocorie, conduisant à
réaliser un fond d’œil en urgence
(2)
.
Le traitement dépend du stade de la tumeur
(3)
. Le premier objectif est la
survie de l’enfant, puis la conservation oculaire et enfi n la vision. La prise
en charge associe actuellement énucléation et chimiothérapie
(4)
, thermo-
thérapie transpupillaire, cryoapplication, radiothérapie externe et disques
radioactifs pour les traitements conservateurs
(5)
. L’infi ltration du nerf
optique en histologie est un facteur de mauvais pronostic, car il existe alors
un risque de dissémination au système nerveux central. L’infi ltration du corps
ciliaire et de la choroïde est également de mauvais pronostic, avec risque
de dissémination hématogène
(fi gure5, p.169)
. Pour cette enfant, nous
avons été amenés à réaliser une chimiothérapie adjuvante
(tableau, p.169)
.
Le rétinoblastome est une tumeur maligne pouvant mettre en jeu le pro-
nostic vital de l’enfant. Le fond d’œil retrouve une masse intrarétinienne
blanche crayeuse, plus ou moins fragmentée, avec calcifi cations intratu-
morales. Le pronostic vital est excellent lorsque la prise en charge n’est
pas retardée (plus de95% des cas dans les pays développés). Le facteur
de risque de mortalité le plus important est l’extension extraoculaire de
la tumeur (surtout trans-sclérale ou par l’atteinte du nerf optique).
IIII
Références bibliographiques
1.
Nagarkatti-Gude N, Wang Y, Ali MJ et al. Gene-
tics of primary intraocular tumors. Ocul Immunol
Infl amm 2012;20(4);244-54.
2.
RosaJr RH. Ophthalmic pathology and intrao-
cular tumors. 2011-2012. Basic and clinical science
course, section4. American Academy of ophthal-
mology 2011:293-308.
3.
Moll AC, Imhof SM, Bouter LM, Tan KE. Second
primary tumors in patients with retinoblas-
toma. A review of literature. Ophatlmic Genet
1997;18(1):27-34.
4.
Aerts I, Sastre-Garau X, Savignoni A et al.
Results of a multicenter prospective study on
the postoperative treatment of unilateral retino-
blastoma after primary enucleation. JClin Oncol
2013;31(11):1458-63.
5.
Lumbroso-Le Rouic L, Aerts I, Lévy-Gabriel C et
al. Conservative treatments of intraocular retino-
blastoma. Ophthalmology 2008;115(8):1405-10.
Lucentis 10 mg/ml Solution injectable (ranibizumab) DONNEES CLINIQUES Indications thérapeutiques Lucentis est indiqué chez les adultes dans : • Le traitement de la forme néovasculaire (humide) de la dégénérescence
maculaire liée à l’âge (DMLA). • Le traitement de la baisse visuelle due à l’œdème maculaire diabétique (OMD). • Le traitement de la baisse visuelle due à l’œdème maculaire secondaire à une occlusion de branche veineuse
rétinienne (OBVR) ou de la veine centrale de la rétine (OVCR). • Le traitement de la baisse visuelle due à une néovascularisation choroïdienne (NVC) secondaire à une myopie forte (MF). Posologie et mode d’administration*
Doit être administré par un ophtalmologiste qualifi é ayant l’expérience des injections intravitréennes (IVT). Posologie dans le traitement de la DMLA néovasculaire : dose recommandée : 0,5 mg (0,05 ml). Le traitement sera
administré 1 fois / mois jusqu’à ce que l’acuité visuelle du patient soit stable lors de 3 évaluations mensuelles consécutives effectuées au cours du traitement. Par la suite, contrôler l’acuité visuelle 1 fois / mois. Si nouvelle baisse
de l’acuité visuelle due à la DMLA néovasculaire, réinstaurer le traitement. Réaliser des injections mensuelles jusqu’à ce que l’acuité visuelle soit à nouveau stable lors de 3 évaluations mensuelles consécutives. L’intervalle entre
2 doses pas ne doit pas être inférieur à 1 mois. Posologie dans le traitement de la baisse visuelle due à l’OMD ou à l’œdème maculaire (OM) secondaire à l’occlusion veineuse rétinienne (OVR) : dose recommandée : 0,5 mg (0,05 ml).
Le traitement sera administré 1 fois / mois jusqu’à ce que l’acuité visuelle du patient soit stable lors de 3 évaluations mensuelles consécutives effectuées au cours du traitement. Si pas d’amélioration d’acuité visuelle à l’issue
d’une 1
ère
série de 3 injections, la poursuite du traitement n’est pas recommandée. Par la suite, contrôler l’acuité visuelle 1 fois / mois. Si nouvelle baisse de l’acuité visuelle due à l’OMD ou à l’OM secondaire à l’OVR, réinstaurer
le traitement. Réaliser des injections mensuelles jusqu’à ce que l’acuité visuelle soit à nouveau stable lors de 3 évaluations mensuelles consécutives. L’intervalle entre 2 doses pas ne doit pas être inférieur à 1 mois. Lucentis et
photocoagulation au laser dans l’OMD et dans l’œdème maculaire secondaire à l’OBVR : cf. RCP complet. Posologie dans le traitement de la baisse visuelle due à une NVC secondaire à une MF Le traitement sera initié avec une injection
unique. Si au cours d’un contrôle, des signes d’activité de la maladie sont constatés, comme par exemple diminution de l’acuité visuelle et/ou des signes d’activité de la lésion, il est recommandé de re-traiter. La surveillance
de l’activité de la maladie peut comprendre un examen clinique, une tomographie à cohérence optique (OCT) ou une angiographie à la fl uorescéine (AF). Surveillance recommandée tous les mois au cours des deux 1
er
mois de
traitement et au moins 1 fois tous les 3 mois par la suite au cours de la 1
ère
année. Après la première année, la fréquence des contrôles doit être déterminée par l’ophtalmologue traitant. L’intervalle entre 2 doses ne doit pas être
inférieur à 1 mois. Lucentis et thérapie photodynamique par Visudyne dans la NVC secondaire à une MF Il n’existe pas de données concernant l’administration concomitante de Lucentis et de Visudyne. Populations particulières
Insuffi sance hépatique : aucune précaution particulière. Insuffi sance rénale : aucune adaptation de dose. Patients âgés : aucune adaptation de dose, expérience limitée en cas d’OMD chez les patients > 75 ans. Population pédiatrique :
pas de données disponibles. Mode d’administration : cf. RCP complet. Contre-indications Hypersensibilité au principe actif ou à l’un des excipients. Patients présentant une infection oculaire ou périoculaire active ou suspectée.
Patients présentant une infl ammation intraoculaire active sévère. Mises en garde spéciales et précautions d’emploi* Réactions liées aux injections intravitréennes ; Elévations de la pression intraoculaire ; Traitement bilatéral ;
Immunogénicité ; Utilisation simultanée avec d’autres médicaments anti-VEGF (facteur de croissance de l’endothélium vasculaire) ; Interruption du traitement par Lucentis ; Déchirure de l’épithélium pigmentaire rétinien ;
Décollement rhegmatogène de la rétine ou trous maculaires ; Populations chez lesquelles les données sont limitées ; Effets systémiques suite à une utilisation intravitréenne ; Antécédents d’OVR, forme ischémique d’OBVR
ou d’OVCR : cf. RCP complet. Interactions avec d’autres médicaments et autres formes d’interactions* ; Fécondité, grossesse et allaitement* ; Effets sur l’aptitude à conduire des véhicules et à utiliser des machines* : cf. RCP
complet. Effets indésirables* Résumé du profi l de tolérance : La majorité des effets indésirables sont liés à la procédure d’injection intravitréenne. Effets indésirables oculaires les plus fréquemment rapportés : douleurs oculaires,
hyperhémies oculaires, augmentations de la pression intraoculaire, hyalites, décollements du vitré, hémorragies rétiniennes, troubles visuels, corps fl ottants vitréens, hémorragies conjonctivales, irritations oculaires, sensations
de corps étranger dans l’œil, sécrétions lacrymales accrues, blépharites, sécheresses oculaires et des prurits oculaires. Effets indésirables non oculaires les plus fréquents : céphalées, rhino-pharyngites et arthralgies. Effets
indésirables moins fréquents mais plus graves comprennent : endophtalmies, cécités, décollements de la rétine, déchirures rétiniennes et cataractes traumatiques iatrogènes. Les patients doivent être informés des symptômes
de ces effets indésirables potentiels et doivent être alertés sur le fait qu’ils doivent informer leur médecin s’ils développent des signes tels que des douleurs oculaires ou une gêne accrue, une rougeur de l’œil s’aggravant, une
vision trouble ou diminuée, une augmentation du nombre de petites taches dans leur champ visuel ou une augmentation de la sensibilité à la lumière. Effets indésirables observés dans les études cliniques : cf. RCP complet.
Effets indésirables liés à la classe : cf. RCP complet. La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfi ce/risque du
médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres
Régionaux de Pharmacovigilance www.ansm.sante.fr. Surdosage* : cf. RCP complet. PROPRIETES PHARMACOLOGIQUES* Propriétés pharmacodynamiques Classe pharmacothérapeutique : Médicaments ophtalmologiques,
médicament contre la néovascularisation, code ATC : S01LA04. Liste I Médicament à prescription réservée aux spécialistes en ophtalmologie. Lucentis 10 mg/ml : EU/1/06/374/001 (2007, révisée 4.07.2013) ; CIP : 34009
378 101.5 9 – boîte de 1. Prix : 895, 57 €. Remboursement Séc. Soc. 100 % selon la procédure des médicaments d’exception.
Prescription en conformité avec la Fiche d’Information Thérapeutique :
•
Traitement de la dégénérescence maculaire liée à l’âge (DMLA) exsudative avec néovascularisation choroïdienne rétrofovéolaire.
•
Traitement de la baisse d’acuité visuelle due à un œdème maculaire diabétique (OMD) chez les patients ayant une baisse d’acuité visuelle inférieure ou égale à 5/10 consécutive à un œdème maculaire diabétique en cas de
forme diffuse ou de fuites proches du centre de la macula et chez lesquels la prise en charge du diabète a été optimisée.
•
Traitement de la baisse visuelle due à l’œdème maculaire secondaire à une occlusion de branche veineuse rétinienne (OBVR) ou de la veine centrale de la rétine (OVCR).
Agréé collect. Non remboursé et non agréé aux collectivités à la date de juillet 2013 (demande d’admission à l’étude) dans l’indication : « traitement de la baisse visuelle due à une néovascularisation choroïdienne (NVC)
secondaire à une myopie forte (MF) ». TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE Novartis Europharm Limited Royaume-Uni Représentant local : Novartis Pharma
S.A.S 2 et 4, rue Lionel Terray 92500 Rueil-Malmaison Tél : 01.55.47.60.00 Information et Communication Médicales : Tél : 01.55.47.66.00 [email protected] FMI0078-17
*Pour une information complète, consulter le texte intégral du résumé des caractéristiques du produit, soit sur le site internet http://www.ema.europa.eu si disponible, soit sur demande
auprès du laboratoire.
B65268 Cahier Ophtalmo 180x120-ML.indd 1 02/09/13 10:20
1
/
3
100%