biodiversité, fonctionnement des écosystèmes et - GIP

BIODIVERSITÉ,
FONCTIONNEMENT DES ÉCOSYSTÈMES
ET GESTION FORESTIÈRE.
PREMIÈRE PARTIE
F.LE TACON -M.-A.SELOSSE -F.GOSSELIN
Rev.For.Fr.LII -6-2000
477
Avertissement
Cet article est tiréd’unessaide synthèseBiodiversitéet gestion forestière,sollicitépar YvesBirot
et OlivierLaroussinie, respectivement,président du Conseil d’administration et directeur du GIP
ECOFOR.Ilest publié en deux parties dans deux numéros successifs de laRevueforestièrefran-
çaise ,le numéro6-2000 et le numéro1-2001. La premièrepartie traitedelabiodiversitéengénéral
et des facteurs anthropiques,autres quelagestion forestière,quipourraient lamodifier.La seconde
traitedu rôle possible des interventions sylvicoles et se termine par une conclusion générale. Cet
article ne peut prétendreàl’exhaustivité. Il reflètela sensibilitéet le champ de compétence,forcé-
ment limité,de chacundes trois auteurs.FrédéricGosselin est l’auteur du planet a rédigé lapartie
sur lamesuredeladiversité spécifique. Ilaégalement effectué une recherche bibliographique
importantequiaaboutià une basededonnées comprenant 8000 références.Ilafourni àFrançois
LeTacon des synthèses sur différents points.Marc-AndréSelosseafourni plusieurs éléments de
réflexion sur labiodiversitéengénéralet rédigé différents documents sur ladiversitéfongique.
François LeTacon a rédigé l’essentiel du texte. Cet article privilégie les sources d’origine française.
Les trois parties, respectivement consacrées àlanotion de biodiversitéet à samesure,aux consé-
quences des actions anthropiques en généralet àl’effet des interventions sylvicoles,constituent
des synthèses aussiobjectives quepossible àpartir de lalittératureexistante. Les éléments de
conclusion n’engagent queles auteurs.
Remarque
Certains termes techniques sont succinctement définis dans unglossaire. Ils sont signalés dans le
textepar unastérisque*.
LA BIODIVERSITÉ
Fondements
La notion de biodiversitéest aussiancienne quel’humanité. Elle ad’abordété strictement utilitaire
et liée aux besoins de l’homme quiaprogressivement tiré sa subsistanced’unnombredeplus en

plus grand d’espèces animales et végétales.Les premiers recensements datent de l’Antiquité. L’ His-
toireNaturelle de Pline l’Ancien est le premier ouvrage décrivant ladiversitédes formes de la vie.
La diversitédela vie est la résultantedelanaturedela vie et de salonguehistoireau terme de
laquelle sont apparues,en nombreconsidérable,des formes adaptées à toutes les situations écolo-
giques (Darwin,1859). L’évolution,depuis l’origine de la vie jusqu’àmaintenant, secaractérisepar
deux processus fondamentaux :lagenèsed’une variabilitécontinuelle par mutation ou recombi-
naison de l’ADN et la“complexification” croissantepar association d’entités différentes.
La recombinaison de l’ADN sous toutes ses formes ne semble pas avoir de limites;pendant la
majeurepartie de l’évolution,les flux de gènes permettant de fairepasser des séquences entières
entreespèces différentes et l’association entregénomes différents ont permis de fairedes avancées
prodigieuses.Ultérieurement et surtout après la sortie des eaux,c’est-à-dire vers moins 420 millions
d’années,ce sont des recombinaisons moins importantes quiont permis àla vie d’évoluer.
La diversité résultedel’action de différents générateurs.L’undes plus importants est l’accumula-
tion de mutations dans les génomes:cegénérateur est interne. Unautregénérateur,externe celui-
là, est constituépar les échanges qu’entretient une population avec ses voisines plus ou moins
éloignées (Nagarajanet Singh,1990). Denouvelles populations arrivent et tentent de s’installer,
alors qued’autres sedisséminent dans de nouveaux milieux.Ces mouvements de population
apportent de nouveaux allèles*.Les nouvelles combinaisons,issues de ces générateurs externes ou
internes, sont soumises àlapression de sélection du milieu.Seules les combinaisons les mieux
adaptées à unmilieu survivent et sont conservées.Des modifications du milieu entraînent la sélec-
tion de nouveaux caractères et la survie d’autres combinaisons.La pression de sélection n’agit pas
simplement sur des gènes déterminés mais sur des systèmes interactifs complexes avecprobable-
ment des phénomènes de compétition entreensembles génomiques assurant différentes fonctions.
Il y aainsiprogressivement divergenceentrepopulations soumises àdes pressions de sélection
différentes lorsqu’il y aisolement géographiqueet en particulier insularité(Darwin,1859). Àpartir
d’uncertain niveau de différenciation,la reproduction sexuée ne peut plus s’effectuer entrepopu-
lations différentes;il y aalors spéciation. Cettedernièreest diteallopatriquelorsqu’elle est la
conséquenced’unisolement géographique. Elle est dite sympatriquelorsquel’isolement n’est pas
physique(MaynardSmith,1966). Dans cecas,elle repose sur tout unensemble de facteurs qui
varient de façon plus ou moins continue. Ces facteurs peuvent êtreliés au milieu ou à une niche
particulièreou à une espèceaccompagnatricequipeut devenir une espècehôte(symbioseou
parasitisme). La spéciation sympatriqueest en généralprogressiveet il existe tous les intermé-
diaires entreespèces au sens strict,définies par labarrièregénétiquequiles isole des autres orga-
nismes vivants,et les espèces définies morphologiquement,mais non encoregénétiquement isolées
des espèces ou sous-espèces voisines.Unexcellent exemple d’une spéciation non encoreachevée
est celle des chênes blancs américains.Les systématiciens distinguent une trentaine d’espèces
morphologiques.Toutes ces espèces peuvent s’hybrider et forment en réalité uncontinuum(Hardin,
1975). La situation des chênes européens est probablement très voisine (Dupouey et Badeau,
1993). Par exemple,en Lorraine,le Chêne sessile et le Chêne pubescent forment uncontinuum. Par
contre,il y apeu d’intermédiaires entreleChêne pédonculé et le Chêne sessile. Lorsquela spécia-
tion est définitive, une nouvelle entitéest née et s’intègreàl’ensemble des communautés*d’êtres
vivants en y jouant un rôle bien précis.Ces processus sont placés sous l’influencedes modifica-
tions naturelles du milieu et,depuis l’avènement de l’humanité, sous l’influencedel’activitéhumaine.
Biodiversitéfonctionnelle et écosystèmes
L’association entregénomes différents entraîne l’apparition de plusieurs niveaux trophiques liés les
uns aux autres et permettant àl’ensemble de fonctionner sous forme de cycles plus ou moins
ouverts.Chaquegrand groupe fonctionnel est indispensable aux autres.Sa disparition ou son
mauvais fonctionnement entraîne undysfonctionnement généralisé. Au sein de cettecoopération
478
F.LE TACON -M.-A.SELOSSE -F.GOSSELIN

générale avecpartage des tâches,existeenpermanence une compétition entre tous les génomes,
cequipermet de conserver toujours les combinaisons les plus adaptées,quelles que soient les
conditions de milieu,qui, rappelons-le,ne sont jamais stables.La plupart du temps,d’ailleurs,ce
sont les conditions de fonctionnement de l’écosystème quigénèrent des modifications du milieu.
Par exemple,l’apparition de laphotosynthèseoxygénique,et doncde l’autotrophie pour le carbone,
aentraîné l’apparition de l’oxygène dans l’atmosphèreet anécessitélepassage de l’anaérobioseà
l’aérobiose. Ilest nécessairequ’il y ait en permanence une possibilitéd’évolution et d’adaptation de
l’ensemble des génomes.Il semble doncindispensable que soit en permanencemaintenuelaplus
grande diversitépossible de façon àcequela vie puisse s’adapter à toutes les modifications d’en-
vironnement susceptibles de seproduire.
Lemaximumdecomplexitéest atteint dans les écosystèmes qui résultent de plusieurs dizaines de
niveaux d’associations.Lefonctionnement de l’écosystème dépend de celuidechaquecompo-
santequigarde ses propriétés et du fonctionnement généralquiobéit à ses propres règles.
Les écosystèmes forestiers sont particulièrement complexes;chaquecomposante y joue un rôle
déterminant.Ils sont caractérisés par laprésencemajoritaired’espèces ligneuses pérennes qui
fonctionnent de manière très particulièreet structurent verticalement l’espaceencréant des strates
aériennes et souterraines qui sont autant de milieux différents favorisant le développement de
communautés très diversifiées.Les structures forestières varient aussihorizontalement par la
densité,l’irrégularitédes peuplements et lacomposition en espèces de la stratearborescente.
La diversitébiologique semble avoir deux rôles majeurs :
—assurer certaines fonctions essentielles,
—permettrel’adaptation aux nouvelles conditions de milieu.
Unécosystème ne peut subsister que si tous les éléments quiconcourent aux différentes étapes
sont présents et fonctionnels.Deux étapes sont indissociables dans unécosystème forestier,
comme dans tout écosystème terrestreou de surfacedes océans:lacaptation de l’énergie solaire
par réduction du gaz carbonique,l’utilisation de l’énergie ainsicaptée par oxydation de lamatière
organique. La premièreétape, sielle est très complexe sur le planbiochimique,ne nécessiteque
l’intervention des chloroplastes des différentes espèces photosynthétiques.Ilfaut cependant y
ajouter l’intervention des espèces hétérotrophes*pour le carbone quiassurent l’essentiel du flux
des éléments minéraux du sol vers les feuilles par l’intermédiairedes symbioses mycorhiziennes.La
deuxième étape est plus complexeet est assurée par une multitude de groupes fonctionnels,micro-
biens et animaux.
D’autrepart,le milieu n’est jamais stable ; les conditions climatiques présentent de fortes variations
annuelles et sont sujettes àdes modifications continuelles de grande amplitude sur des pas de
temps plus ou moins longs.Endehors des accidents ou des variations climatiques,les écosys-
tèmes,et peut-êtreplus particulièrement les écosystèmes forestiers, sont soumis àdes agressions
de grande ampleur :incendies,pullulations de ravageurs,etc.La diversitébiologiquepermet de
répondreàces différentes perturbations et de trouver une solution adaptée àchaque situation
nouvelle. Unécosystème naturel forestier est évolutif et doit êtrecapable de s’adapter àde
nouvelles situations,du moins àl’intérieur de certaines limites.
Traditionnellement,dans les écosystèmes forestiers,labiodiversitéest organisée autour des grands
groupes suivants :
Capteurs d’énergie
Espèces ligneuses
Espèces herbacées et arbustives
Algues,lichens et mousses épiphytes
Rev.For.Fr.LII - 6-2000
479
Biodiversité,fonctionnement des écosystèmes et gestion forestière

Utilisateurs mobiles d’énergie
Insectes et arachnides
Oiseaux
Batraciens et reptiles
Mammifères
Utilisateurs d’énergie peu mobiles
Microfaune du sol
Utilisateurs d’énergie non mobiles
Champignons
Bactéries
Actinomycètes
L’importancedes groupes fonctionnels et de leur diversitédans le fonctionnement des écosys-
tèmes forestiers ne peut être traitée de manièreexhaustive. Différents exemples pourraient êtrepris
comme celuidelachaîne trophiqueet de l’ensemble de ses maillons allant de laproduction de
biomasseaux grands carnivores quiassurent la régulation des herbivores et donclapérennitéde
l’écosystème forestier.Il serait aussipossible de prendrelamême chaîne trophique,mais en se
focalisant cettefois sur les insectes et les oiseaux avecles interactions concernant lapollinisation
des arbres ou ladissémination des semences quiconditionnent les possibilités d’extension de
certaines espèces et doncl’évolution de l’écosystème tout entier (exemple du rôle des geais dans
ladissémination des glands). Nous pouvons illustrer l’importancedes groupes fonctionnels en
prenant unautreaspect de lachaîne trophique:celuideladécomposition de lamatièreorganique
mortequiest assurée àlafois par des micro-organismes,des micro-arthropodes,des insectes et
quelques autres groupes.Les micro-organismes du sol ont un rôle majeur dans le fonctionnement
des écosystèmes forestiers en assurant au moins quatrefonctions essentielles (Dommergues et
Mangenot,1970):
—ladisponibilitéenazoteminéralcombiné dont l’origine est essentiellement d’origine micro-
biologique,
—l’altération des minéraux primaires dont dépend lafertilitédes sols,
—le recyclage du carbone,
—lefonctionnement des cycles biogéochimiques et plus particulièrement laminéralisation de
lamatièreorganique.
Les micro-organismes sont eux-mêmes très diversifiés et appartiennent àdes groupes différents :
bactéries,champignons,protozoaires (algues unicellulaires,amibes,ciliés,etc.).
Dès qu’une feuille, unmorceau de bois ou unfragment d’écorcearriveau sol,ils sont soumis à
l’action coordonnée de lamicrofloreet de lamicrofaune du sol. Sil’humiditéest suffisante,ce sont
les bactéries,les actinomycètes et les champignons quiattaquent en premier cettematièreorga-
niqueprimaire,essentiellement par voie enzymatique. Ils sont ensuite suivis par des insectes,des
mollusques,des crustacés,des vers de terre,des enchytréides,et beaucoupd’autres quiinter-
viennent àlafois mécaniquement et par voie enzymatique. Les bactéries,les champignons et les
algues sont eux-mêmes consommés par des protozoaires unicellulaires et mobiles.
D’autres micro-organismes du sol,les champignons mycorhiziens,assurent l’essentiel de lanutri-
tion minérale et de l’équilibrehormonalde tous les végétaux constituant l’écosystème forestier
(végétation herbacée,arbustiveet arborescente). Ils jouent aussi un rôle non négligeable dans l’ali-
mentation en eau des arbres àectomycorhizes.
Lefonctionnement des écosystèmes en généralet des écosystèmes forestiers en particulier est
assurépar de multiples partenaires quipossèdent souvent des fonctions identiques.Onparle
480
F.LE TACON -M.-A.SELOSSE -F.GOSSELIN

souvent de “redondancefonctionnelle”. Mills,Soulé et Doad(1993)préfèrent substituer àcette
notion de redondancecelles de similarité,d’équivalence,de compensation ou de complémentarité.
Pour les fonctions de décomposition de lalitière,par exemple,les différentes étapes sont assurées
par des micro-organismes,des micro-arthropodes et d’autres organismes dont les modes d’action
semblent très “redondants”. La présenced’une fraction de ces communautés semble suffisante
pour assurer la totalitédes fonctions nécessaires.Une simplification d’une ou plusieurs compo-
santes de l’écosystème ne semble pas avoir de conséquences au moins àcourt terme. C’est la
raison pour laquelle les systèmes artificiels simplifiés fonctionnent de manière satisfaisante,bien
quenon durable. L’intervention de l’homme assureleur pérennitéàpresque tous les stades de la
révolution et en particulier au moment de la régénération. La redondancefonctionnelle peut par
contreavoir beaucoupd’importanceau moment de l’apparition de modifications importantes ou de
perturbations de grande ampleur.Les communautés microbiennes quiassurent des fonctions iden-
tiques sont souvent très différentes sur le plan taxonomique. Leur réactivitéaux changements sera
doncdifférente. La redondancepeut,par conséquent,êtreinterprétée comme une assurancepour
le futur.
Biodiversitéet grands facteurs du milieu
Ilest évident quelemilieu joue un rôle déterminant dans l’établissement de labiodiversité. Plus le
milieu sera variable dans l’espace,plus le nombred’écosystèmes seraimportant et plus labiodi-
versité seragrande. Pour prendrequelques exemples forestiers,comparons le nombrede types de
forêts en Franceet en Scandinavie. EnScandinavie,le nombrede types de forêts est faible et peut
facilement êtredécrit en quelques grands ensembles homogènes répartis sur de grandes surfaces.
EnFrance,il en est tout autrement en raison de lagrande variétédes roches-mères,des sols et des
climats.D’autrepart,en France,les conditions écologiques sont très favorables (sols riches et
climat généralde type tempéré). Or,il est admis,même sicen’est pas toujours le cas,queladiver-
sitéest d’autant plus grande queles conditions de milieu sont plus favorables.C’est ainsiquele
nombred’espèces de plantes ou d’arbres diminueaveclalatitude ou l’altitude (Woodward,1987).
Demême,en milieu forestier tempéré,les espèces herbacées ou arbustives acidiphiles sont moins
nombreuses queles espèces acidoclines,elles-mêmes moins nombreuses queles espèces neutro-
acidoclines ou neutrophiles (Becker et al.,1980). Les milieux neutrophiles présentent par consé-
quent une plus grande diversitéqueles milieux acidiphiles.Mais sicelaest exact pour les arbres
et leurs espèces herbacées accompagnatrices,c’est l’inversepour lamicrofloredes sols et pour les
associés fongiques des arbres forestiers.L’accumulation de matièreorganiqueenmilieu acide
entraîne lamiseenplaced’une chaîne particulièrement complexededécomposeurs.Demême la
nécessitéd’extrairedes éléments nutritifs de lalitièreainduit unchangement profond dans la
natureet ladiversitédes associés symbiotiques mycorhiziens des milieux acides.
Niveau d’expression de labiodiversité
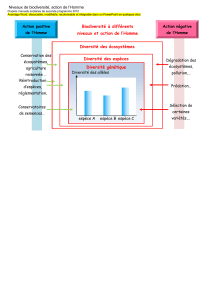
Les organismes vivants sont organisés en différents niveaux de diversité:diversitéallélique,diver-
sitépopulationnelle ou intraspécifique,diversité spécifiqueet diversitédecommunauté. La diversité
allélique s’exprime par l’ensemble des gènes et de leurs allèles générés au cours de l’évolution et
existant encore. Pour l’ensemble des formes de vie,le nombredegènes est estimé à10 9,chaque
gène possédant en moyenne plusieurs dizaines ou centaines d’allèles différents.Sicertains sont
stables en raison du rôle qu’ils jouent dans les processus métaboliques de base,d’autres évoluent
constamment.Ces gènes s’organisent en génomes caractérisant les espèces.La diversité spéci-
fiqueest le moyen le plus fréquent d’exprimer ladiversité. 1,7million d’espèces ont étédécrites à
cejour.Lenombre totald’espèces existant sur l’ensemble de laplanèteest inconnu.Ilpourrait
varier entre5et 80millions d’espèces dont lamajorité sont des insectes et des micro-organismes
(Stork,1988). Àl’intérieur même des espèces,il existe une diversitéintraspécifiqueplus ou moins
Rev.For.Fr.LII - 6-2000
481
Biodiversité,fonctionnement des écosystèmes et gestion forestière
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
1
/
20
100%