Classification moléculaire des tumeurs thyroïdiennes : intérêts et limites de l’approche transcriptomique

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XIV - n° 7 - septembre 2010
216
dossier thématique
Cancers de la thyroïde :
aspects innovants
Classification moléculaire des tumeurs
thyroïdiennes : intérêts et limites
de l’approche transcriptomique
Molecular classification of thyroid tumors: advantages and limitations
of the transcriptomic approach
Frédérique Savagner*
»Le transcriptome permet d’avoir une vision globale des fonctions
dérégulées dans une classe tumorale.
»
L’analyse du transcriptome permet d’identifier les processus
tumoraux initiaux, mais aussi les réactions du tissu environnant
(infiltrats lymphocytaires).
»
Il existe une meilleure corrélation entre le statut mutationnel et
le transcriptome d’une tumeur qu’entre le statut mutationnel et
l’histologie de cette tumeur.
»
L’identification de biomarqueurs spécifiques de classe n’est
pertinente que si le transcriptome de l’ensemble des classes
pathologiques de l’organe est exploré.
»
Le profil d’expression de biomarqueurs ciblés présente un réel
potentiel diagnostique pour les classes intermédiaires de pathologies.
Mots-clés : Transcriptome – Tumeurs thyroïdiennes – Classication –
Biomarqueurs.
Keywords: Transcriptome – Thyroid tumors – Classication – Biomarkers.
Points forts
L’
analyse moléculaire de la physiopathologie
d’un organe ou d’un tissu a été longtemps
limitée à l’étude de quelques gènes candidats.
Depuis le milieu des années 1990, les outils molécu-
laires développés permettent de mesurer l’expression
de plusieurs milliers de gènes en même temps, et ce
de façon maintenant tout à fait able et standardisée.
Appliquée à l’étude des tumeurs, cette technologie a
pour ambition de préciser les mécanismes physiopa-
thologiques et d’identier des marqueurs diagnos-
tiques ou pronostiques ainsi que de potentielles cibles
thérapeutiques. Elle est très peu utilisée dans un but
de reclassication moléculaire en complément de la
classication histologique.
Lorsque l’on examine la classication histologique des
tumeurs thyroïdiennes (OMS, 2004), il apparaît pourtant
que des marqueurs biologiques ayant éventuellement
une valeur pronostique pour les classes intermédiaires
sont encore manquants (1). Ainsi, la nouvelle classe
des tumeurs de potentiel de malignité incertain
(TPMI) entretient le ou quant à l’évolution clinique.
De même, la distinction de certains variants histolo-
giques ne semble pas avoir de valeur pronostique. Mais
la principale diculté de la classication histologique
des tumeurs thyroïdiennes diérenciées provient des
tumeurs folliculaires bénignes (FTA) et malignes (FTC) et
de la grande variabilité interobservateur pour armer
l’invasion capsulaire et vasculaire (2).
L’approche transcriptomique
Les microarrays, ou puces à ADN, servent à détecter et à
quantier plusieurs milliers d’acides nucléiques (ARNm)
extraits d’un échantillon biologique et qui constituent
le transcriptome de l’échantillon. L’analyse bio-infor-
matique des données du transcriptome de plusieurs
échantillons va permettre leur regroupement selon la
similarité des prols d’expression. Selon les méthodes,
les regroupements peuvent être indépendants (classi-
cation non supervisée), ou au contraire contraints par
les classes histologiques (classication supervisée). Ces
2 méthodes sont complémentaires dans leur approche :
d’une part, conrmer la pertinence d’une classe par sa
présence en classication non supervisée ; d’autre part,
apprécier la proximité de diérentes classes par une
approche supervisée. Ces approches permettent égale-
ment d’identier de nouvelles classes ou d’apporter des
éléments de reclassication pour des classes considé-
rées comme atypiques. Elles vont permettre d’identier
des gènes corégulés (cluster de gènes) associés à une
fonction et/ou à une classe histologique donnée. Au
travers de ces fonctions et de ces gènes corégulés, les
* Inserm UMR694,
CHU d’Angers.

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XIV - n° 7 - septembre 2010
217
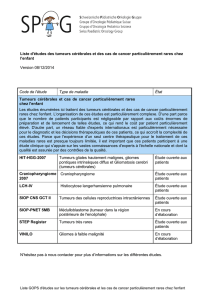
Figure 1. Cibles thérapeutiques identiées par analyse du transcriptome et de l’interactome
des cancers folliculaires (FTC) et papillaires (PTC).
Cible thérapeutique des FTC
PPARγ/Pax8 positifs (interactome
des gènes surexprimés)
Cibles thérapeutiques des PTC
Ret/PTC, BRAF et Ras positifs
BRAF EPHA2
EGFR
NRG1
PTK2 SOS1
Inhibiteurs de la
tyrosine kinases/EGFR
Inhibiteurs de la
tyrosine kinases/EGFR
Inhibiteurs de la
sérine-thréonine kinases
Ret
RAS
BRAF
MAPK
Ret/PTC3
PI3Kinase
Classication moléculaire des tumeurs thyroïdiennes
biomarqueurs de chaque classe sont recherchés. Pour
autant, une même fonction peut être dérégulée dans
plusieurs classes de pathologies.
Transcriptome et anomalies moléculaires
des tumeurs thyroïdiennes
Les cancers papillaires sont fortement associés aux
réarrangements Ret/PTC et aux mutations du gène
B-Raf, alors que les tumeurs folliculaires présentent,
pour partie, des anomalies dans les gènes Ras ou
PPARγ/Pax8. Les études du transcriptome de diérentes
tumeurs thyroïdiennes dont le statut mutationnel est
connu montrent que ce statut est mieux corrélé au
prol d’expression qu’à la morphologie des tumeurs.
Les voies précoces de tumorigenèse peuvent donc être
mieux cernées par une approche transcriptomique. Les
2 études de Giordano et al. sont sur ce point instructives
(3, 4). La première étude portant sur la classication
des cancers papillaires (PTC) avec réarrangements
Ret/PTC1 ou 3, mutations B-Raf ou N-, K- ou H-Ras
montre que, si la plupart des prols transcriptionnels
des cancers papillaires présentent des caractéristiques
moléculaires communes associées à la voie Ret/Ras/
Raf/MAPK, chaque type de mutation est lié à un prol
transcriptionnel spécique. Le réarrangement Ret/PTC3
est quant à lui associé à un prol d’activation de la voie
PI3Kinase et non à celle des MAPK. La deuxième étude
portant sur le transcriptome des cancers folliculaires
avec réarrangement PPARγ/Pax8 montre que la voie
PPARα est activée en parallèle de la voie PPARγ. Cette
voie PPARγ est alors corrélée à la surexpression de gènes
associés à la voie EGFR. Ces 2 approches soulignent
l’intérêt thérapeutique d’une meilleure connaissance
des voies de tumorigenèse thyroïdienne, puisque les
thérapeutiques ciblées seront alors diérentes selon la
mutation dominante retrouvée (gure 1).
Classification moléculaire des tumeurs
différenciées
S’agit-il d’identier le caractère bénin ou malin d’une
tumeur ou de prouver la pertinence de la classe histo-
logique ? La plupart des études explorent 2 classes de
tumeurs (malignes/bénignes) ou une classe tumorale
par rapport au tissu sain environnant. L’objectif de ces
études est soit l’identication d’un ou de plusieurs bio-
marqueurs de la classe pathologique (comparaison au
tissu sain) soit l’identication de marqueurs de malignité
(comparaison de classes bénignes et malignes). Pour
autant, la comparaison de 2 classes, quelle que soit la
question posée, n’est pas susante pour armer la
spécicité de biomarqueurs.
Classes intermédiaires
Si l’on considère la notion de continuum dans les
tumeurs thyroïdiennes folliculaires, l’apport de la tech-
nologie des puces à ADN semble pourtant à même,
de par sa sensibilité, d’identifier les modifications
précoces de l’expression de gènes impliqués dans
un état de prémalignité. Deux études se sont pour le
moment penchées sur la reclassication moléculaire
des TPMI (5, 6). Leur classication par prol d’expres-
sion n’est cependant pertinente que si les classes dié-
rentielles de ces tumeurs sont explorées en parallèle,
comme les FTA, les FTC peu invasifs, mais aussi les
variants folliculaires des cancers papillaires. Dans ces
2 études basées sur des échantillons représentatifs
des 4 classes nodulaires d’intérêt mais aussi de classes
non nodulaires témoins, les auteurs montrent que le
prol d’expression permet d’améliorer la classica-
tion des TPMI. Les prols d’expression sont corrélés à
l’analyse immunohistologique (score), celle-ci restant
malheureusement toujours dépendante du patholo-
giste référent (gure 2, p. 218).
Nombre d’échantillons et taille des classes
Comme toute approche de classication, la recherche
de biomarqueurs pertinents par l’analyse du trans-
criptome nécessite que la spécicité de ces biomar-
queurs soit vériée au travers de l’ensemble des classes
pathologiques d’un organe donné. Si la classication

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XIV - n° 7 - septembre 2010
218
dossier thématique
Cancers de la thyroïde :
aspects innovants
Figure 3. Classication supervisée des échantillons issus de 12 classes de pathologies thyroïdiennes
et de tissus sains selon leur prol d’expression moyen (transcriptome de plusieurs milliers de gènes).
L’arbre, ou dendrogramme, illustre la distance entre les classes de pathologies thyroïdiennes. La
robustesse de la classication est illustrée par les 3 cercles noirs sur les arbres. Deux groupes de
tumeurs se distinguent du groupe bénin: les tumeurs de potentiel de malignité incertain (TPMI)
et les adénomes d’architecture microfolliculaire (FTA microfolliculaires).
Groupe
de pathologies Bénignes
FTA, thyroïdite,
Basedow…
Malignes
FTC, PTC,
TPMI
Riches
en mitochondries
Tumeurs
oncocytaires
– 0,2
0
0,2
0,4
Corrélation
0,6
0,8
1
FTA
microfolliculaires
TPMI
Figure 2. Corrélation entre le prol d’expression moyen des 10 tumeurs de potentiel de malignité
incertain (TPMI) et le score du pathologiste établi par combinaison de marqueurs immunohis-
tologiques (HBME-1, galectine 3, CK-19 et TPO) et de caractéristiques histologiques (nucléaires,
cytoplasmiques, invasions capsulaires et vasculaires). Coecient de corrélation Spearman = 0,71.
Profil Score
0,16 14
12
10
8
6
4
2
0
– 2
– 4
0,14
0,12
0,1
0,08
0,06
0,04
0,02
0
– 0,02
– 0,04
Profil d’expression moyen
Score du pathologiste
1 2 3 4 5 6 7 8 9 10
Numéro des TPMI
moléculaire met en évidence des événements pré-
coces de tumorigenèse, elle n’en demeure pas moins
une technique qui permet aussi de visualiser des évé-
nements annexes de type réaction du tissu environ-
nemental (inltrats), qu’il faudra alors identier pour
extraire la signature spécique du processus tumoral
engagé dans la classe histologiquement dénie. Peu
d’études ont comparé plus de 4 classes de pathologies
thyroïdiennes au cours d’une même analyse (4, 7-10).
À ce jour, une seule étude a dépassé les 10 classes ou
sous-classes histologiques explorées conjointement
(8). Cette unité technique et temporelle a permis d’être
pertinent dans la sélection de biomarqueurs réelle-
ment spéciques de chaque classe. Une méta-analyse
impliquant 5 autres jeux de données de transcriptome
disponibles dans les bases de données publiques et
permettant de “cross-valider” les marqueurs les plus
pertinents pour les classes communes à ces diérentes
études a permis de montrer que plus de 52 % des mar-
queurs sélectionnés par cross-validation étaient com-
muns à au moins 2 des classes ou sous-classes dénies
dans la première étude (12 classes). Elle montre aussi
que l’identication du prol d’expression des variants
oncocytaires des tumeurs folliculaires permet une
meilleure classification des tumeurs (figure 3). En
eet, la signature mitochondriale de ces variants est
parfois présente dans d’autres classes de tumeurs et
peut masquer la signature pertinente de ces classes
au même titre qu’une signature “non spécique” de
type lymphocytaire.
Les méta-analyses regroupant les données de trans-
criptome issues de plusieurs études montrent mal-
heureusement encore un intérêt limité en pathologie
thyroïdienne car, en dehors de la classe PTC, très peu
de variants de tumeurs folliculaires sont explorés et
leurs caractéristiques histologiques restent souvent
imprécises (11, 12).
Validation des biomarqueurs de classe
Si l’identication d’un seul biomarqueur d’une classe
donnée est utopique, plusieurs études proposent un
nombre restreint de marqueurs (3 à 10) qui permet-
tent non pas de réaliser la bonne classication des
tumeurs étudiées mais d’en dénir le potentiel malin
(9, 13-15). Ces marqueurs de malignité sont cependant
toujours dénis en utilisant un nombre restreint de
classes. Une étude plus récente montre la nécessité
de 20 biomarqueurs pour la seule classication des
cancers papillaires (11). Les cancers papillaires repré-
sentent pourtant la classe la mieux caractérisée d’un
point de vue moléculaire. Il est important de consta-
ter que, en dehors des marqueurs identiés pour la
classe des cancers papillaires, les diérentes études
d’expression ne permettent actuellement pas d’iden-
tier des marqueurs communs pour la classication
des tumeurs folliculaires.
Dans tous les cas, le nombre de marqueurs à sélection-
ner ne pourra être déni que si un nombre susant de
classes pathologiques est exploré. L’intérêt des clusters

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XIV - n° 7 - septembre 2010
219
Classication moléculaire des tumeurs thyroïdiennes
de gènes repose sur le fait que la dérégulation de leur
expression est rapportée à une fonction. Il faut alors
plutôt s’orienter vers la recherche des meilleurs mar-
queurs de cette fonction spéciquement dérégulée
dans la classe tumorale d’intérêt. Faut-il à tout prix
valider ces biomarqueurs au niveau protéique ? Tous
les biomarqueurs de la fonction dérégulée ne seront
pas aussi pertinents comme marqueurs protéiques
utilisables en immunohistochimie. Quel que soit le
tissu exploré, les variations du transcriptome et du
prol protéique sont discordantes dans 30 % des cas.
En dehors du problème de la disponibilité en anticorps
commerciaux, il faut donc aussi tenir compte des modi-
cations traductionnelles de ces ARNm dérégulés. En
regard du nombre restreint de cas nécessitant une
classication moléculaire complémentaire à la classi-
cation histologique, il est peut-être plus judicieux de
réaliser une analyse d’expression ciblée plutôt que de
proposer un panel très vite contraignant de marqueurs
en immunohistochimie. L’intérêt du transcriptome
réside vraiment dans sa capacité à identier puis à
explorer un panel de biomarqueurs, sans véritables
contraintes liées à la quantité de matériel biologique
ou au nombre de marqueurs à tester.
Conclusion
Si la sensibilité de l’outil d’analyse du transcriptome
a maintenant fait ses preuves et peut être appliquée
à l’exploration de quelques cellules (microdissection,
cytoponction), la pertinence des biomarqueurs iden-
tiés dépend entièrement de l’échantillonnage des
tumeurs explorées. L’utilisation de nouvelles approches,
telles que l’étude des prols de microARN, sera confron-
tée au même problème d’échantillonnage. En dehors
de la classe des cancers papillaires, pour laquelle il y
a susamment d’études d’expression permettant de
converger vers une vingtaine de biomarqueurs réel-
lement spéciques, peu de marqueurs de classes fol-
liculaires peuvent encore être proposés avec certitude.
Pour autant, l’information est sûrement pour partie déjà
présente, sous les dénominations “nodules chauds/
froids”, “tumeurs bénignes” sans autre précision, qui sont
très généralement les tissus “témoins” des études por-
tant sur les cancers papillaires. L’intérêt de poursuivre
ces études réside dans la pertinence de l’identication
de biomarqueurs de groupes plus marginaux (TPMI,
adénomes microfolliculaires, tumeurs oncocytaires)
et de la révélation de leur valeur pronostique. ■
1. Chan JKC, Hirokawa M, Evans H et al. Tumours of the thyroid
and parathyroid: follicular adenoma. In: DeLellis RA, Lloyd RV,
Heitz PU, Eng C, eds. WHO classification of tumours: pathology,
genetics of tumours of endocrine organs. Lyon, France: IARC
Press 2004:98-103.
2.
Franc B, de la Salmoniere P, Lange F et al. Interobserver and
intraobserver reproducibility in the histopathology of follicular
thyroid carcinoma. Hum Pathol 2003;34:1092-100.
3. Giordano TJ, Kuick R, Thomas DG et al. Molecular classifi-
cation of papillary thyroid carcinoma: distinct BRAF, RAS, and
RET/PTC mutation-specific gene expression profiles discovered
by DNA microarray analysis. Oncogene 2005;24:6646-56.
4. Giordano TJ, Au AY, Kuick R, Thomas DG et al. Delineation,
functional validation, and bioinformatic evaluation of gene
expression in thyroid follicular carcinomas with the PAX8-
PPARG translocation. Clin Cancer Res 2006;12:1983-93.
5. Fontaine JF, Mirebeau-Prunier D, Franc B et al. Microarray
analysis refines classification of non-medullary thyroid tumours
of uncertain malignancy. Oncogene 2008;27:2228-36.
6. Barroeta JE, Baloch ZW, Lal P, Pasha TL, Zhang PJ, LiVolsi VA.
Diagnostic value of differential expression of CK19, Galectin-3,
HBME-1, ERK, RET, and p16 in benign and malignant folli-
cular-derived lesions of the thyroid: an immunohistoche-
mical tissue microarray analysis. Endocr Pathol 2006;17:
225-34.
7. Finley DJ, Zhu B, Fahey TJ, III. Molecular analysis of Hurthle
cell neoplasms by gene profiling. Surgery 2004;136:1160-8.
8. Fontaine JF, Mirebeau-Prunier D, Raharijaona M et al.
Increasing the number of thyroid lesions classes in microarray
analysis improves the relevance of diagnostic markers. PLoS
One 2009;4:e7632.
9. Weber F, Shen L, Aldred MA et al. Genetic classification of
benign and malignant thyroid follicular neoplasia based
on a three-gene combination. J Clin Endocrinol Metab
2005;90:2512-21.
10.
Yukinawa N, Oba S, Kato K et al. A multi-class predictor
based on a probabilistic model: application to gene expression
profiling-based diagnosis of thyroid tumors. BMC Genomics
2006;7:190.
11. Eszlinger M, Wiench M, Jarzab B et al. Meta- and reanalysis
of gene expression profiles of hot and cold thyroid nodules and
papillary thyroid carcinoma for gene groups. J Clin Endocrinol
Metab 2006;91:1934-42.
12. Giordano TJ. Genome-wide studies in thyroid neoplasia.
Endocrinol Metab Clin North Am 2008;37:311-31.
13. Foukakis T, Gusnanto A, Au AY et al. A PCR-based expression
signature of malignancy in follicular thyroid tumors. Endocr
Relat Cancer 2007;14:381-91.
14. Aldred MA, Huang Y, Liyanarachchi S et al. Papillary and
follicular thyroid carcinomas show distinctly different microar-
ray expression profiles and can be distinguished by a minimum
of five genes. J Clin Oncol 2004;22:3531-9.
15.
Mazzanti C, Zeiger MA, Costouros NG et al. Using gene
expression profiling to differentiate benign versus malignant
thyroid tumors. Cancer Res 2004;64:2898-903.
R é f é r e n c e s
1
/
4
100%