L Modalités de la prise en charge chirurgicale des patientes mutées

14 | La Lettre du Sénologue • No 60 - avril-mai-juin 2013
Figure 1. Mastectomie bilatérale prophylactique conservant l’étui cutané avec exérèse
de la plaque aréolomamelonnaire et reconstruction immédiate par prothèse.
DOSSIER
Prise en charge des seins
d’une “femme mutée”
Modalités de la prise
en charge chirurgicale
des patientes mutées
Surgical handling of patients with BRCA1/2 mutations
T. Ihrai*, K. Clough**
* Centre Antoine-Lacassagne, Nice.
** Institut du sein, Paris.
L
es patientes porteuses d’une mutation pré-
disposante présentent un risque majoré de
survenue d’un cancer du sein (risque cumulé à
70 ans de 60 à 70 % en cas de mutation de BRCA1
et de 50 à 60 % en cas de mutation de BRCA2) et
de l’ovaire (risque de 20 à 60 % et de 4 à 47 %,
respectivement) [1]. La prise en charge chirurgicale
des patientes mutées ne se conçoit que dans un
cadre pluridisciplinaire. Une information claire et
exhaustive doit être délivrée aux patientes afi n de
les guider dans leurs décisions quant à la prévention
du risque de cancer.
Les principes de la prise en charge chirurgicale des
patientes mutées reposent sur une abondante litté-
rature scientifi que. Cependant, aucun essai contrôlé,
randomisé ou non, portant sur les patientes mutées
n’a été publié, ce qui doit inciter à considérer avec
précaution les conclusions des diverses publications
disponibles (2).
Les différentes situations cliniques relatives aux
patientes mutées sont développées ci-dessous.
Patientes mutées, indemnes
de tout cancer
La prise en charge de ces patientes repose soit sur
une surveillance rapprochée, soit sur la mise en place
de mesures prophylactiques.
Surveillance rapprochée
La surveillance mammaire comporte, en plus de
l’autopalpation et d’un suivi clinique régulier, la
réalisation d’un bilan d’imagerie annuel. Le recours
à l’IRM est recommandé, en raison de sa plus impor-
tante sensibilité chez les patientes à haut risque de
cancer du sein (3). La surveillance des ovaires est
plus problématique, du fait de l’absence d’une tech-
nique effi cace de dépistage précoce. La surveillance
présente peu de désagréments pour les patientes,
en dehors de l’anxiété inhérente à leur statut de
patientes “à risque”. Cette attitude ne réduit pas
le risque de cancer mais vise à détecter et à traiter
précocement un éventuel cancer.
Mesures prophylactiques
Les mesures prophylactiques disponibles sont de
2 types : l’hormonothérapie préventive, qui ne sera pas
traitée dans ce travail, et la chirurgie prophylactique.

La Lettre du Sénologue • No 60 - avril-mai-juin 2013 | 15
Points forts
»La méthode de prévention primaire la plus efficace est la chirurgie prophylactique.
»
La réduction maximale du risque est obtenue par la combinaison d’une mastectomie bilatérale prophy-
lactique et d’une annexectomie bilatérale prophylactique. L’annexectomie est la seule chirurgie prophy-
lactique qui ait un bénéfice en survie démontré.
»
En cas de diagnostic de cancer du sein chez une femme mutée, le traitement conservateur est une option
valide. Après le traitement d’un cancer du sein, une mastectomie prophylactique controlatérale réduit le
risque de cancer controlatéral mais n’améliore pas la survie.
»
En cas d’antécédent de cancer du sein traité, seule l’annexectomie bilatérale prophylactique semble
apporter un bénéfice en survie.
Mots-clés
BRCA1/2
Cancer du sein
Cancer de l’ovaire
Prévention
Traitement chirurgical
Highlights
»
Patients with BRCA1/2 muta-
tion are at high risk of devel-
oping breast and ovarian
cancer.
»
The best cancer prevention, in
BRCA patients with no personal
history of cancer, relies on
bilateral mastectomy and/or
bilateral salpingo-oophorec-
tomy. Several techniques of
prophylactic mastectomy are
available: total mastectomy,
skin-sparing mastectomy and
nipple-sparing mastectomy.
»
After bilateral mastectomy,
immediate breast reconstruc-
tion with implants is often
performed.
»
In BRCA patients diagnosed
with breast cancer, breast
conservation is a valid option,
as it is equivalent to mastec-
tomy in terms of overall
survival. Contralateral prophy-
lactic mastectomy reduces
contralateral breast cancer risk
but does not improve survival.
In patients with a personal
history of breast cancer, only
bilateral salpingo-oophorec-
tomy seems to enhance overall
survival.
Keywords
BRCA1/2
Breast cancer
Ovarian cancer
Prevention
Surgical treatment
La chirurgie prophylactique repose sur la réalisa-
tion d’une annexectomie bilatérale prophylac-
tique (ABP), associée ou non à une mastectomie
bilatérale prophylactique (MBP). En théorie, cette
chirurgie devrait, pour permettre un gain en survie,
être réalisée précocement dans la vie d’une femme
mutée, le risque de décès par cancer du sein étant
plus élevé chez les femmes jeunes. Le bénéfi ce de la
chirurgie prophylactique, en termes d’espérance de
vie, dépend du type de mutation, des antécédents
cancérologiques personnels et de l’âge auquel est
réalisée cette chirurgie.
◆Mastectomie bilatérale prophylactique
La MBP permettrait de réduire de 85 à 100 % le
risque de survenue d’un cancer du sein (4, 5). Bien
que cela s’associe probablement à une réduction
de la mortalité globale (1), nous ne disposons à ce
jour d’aucune étude qui ait démontré un bénéfi ce
en survie de la MBP par rapport à la surveillance et
au dépistage du cancer à un stade précoce.
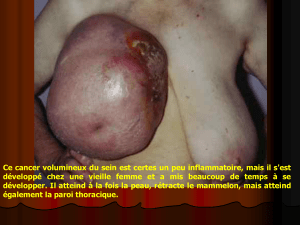
Différentes techniques de MBP ont été décrites :
mastectomie totale, mastectomie conservant l’étui
cutané (skin-sparing mastectomy) et mastectomie
conservant l’étui cutané (fi gure 1) et la plaque aréo-
lomamelonnaire (PAM) [nipple-sparing mastectomy]
(fi gures 2, 3, p. 16), qui est aujourd’hui la technique
la plus souvent proposée. Ces techniques semblent
équivalentes sur le plan de la réduction du risque
de survenue d’un cancer. Les techniques conserva-
trices de l’étui cutané et éventuellement de la PAM
facilitent la reconstruction mammaire et donnent
généralement de meilleurs résultats cosmétiques.
Le choix d’une technique de MBP repose essentiel-
lement sur le souhait de la patiente à qui ont été
expliquées, de manière exhaustive, les différentes
options chirurgicales (6). Avant une MBP, un bilan
d’imagerie avec IRM est recommandé afi n de limiter
le risque de découverte, lors de l’examen histologique
défi nitif, d’un cancer occulte. Après la MBP, la sur-
veillance repose sur un examen clinique annuel (7).
La MBP est le plus souvent associée à une reconstruc-
tion mammaire immédiate. Cette dernière repose sur
la mise en place de prothèses rétromusculaires dans
70 à 95 % des cas (8). L’utilisation de matrices der-
miques acellulaires est de plus en plus répandue, car
celles-ci facilitent la création de la loge prothétique et
limitent le risque de déplacement de l’implant (9). Par
ailleurs, si la patiente le souhaite et que sa morpho-
logie s'y prête et si ses comorbidités ne constituent
pas un obstacle, une reconstruction par 2 lambeaux
de type DIEP (Deep Inferior Epigastric Perforator), voire
2 lambeaux de grand dorsal, peut être envisagée (10).
Le recours au lipofi lling (autogreffe de tissu graisseux)
en complément de la reconstruction est très large-
ment pratiqué, comme chez les patientes non mutées.
Le taux de complications (précoces et tardives) après
une mastectomie et une reconstruction immédiate
varie entre 30 et 50 %. Le taux de reprise chirurgi-
cale, après une complication, varie entre 35 et 70 %.
Ce taux est plus important en cas de reconstruction
par implant (11). Ces chiffres doivent néanmoins
être relativisés, car plus de 1/3 de ces complica-
tions correspondent à des coques périprothétiques
qui peuvent être traitées par capsulotomie simple
(fi gure 4, p. 16).
◆Annexectomie bilatérale prophylactique
Le National Comprehensive Cancer Network amé-
ricain, de même que l’Institut national du cancer
(INCa), recommandent la réalisation, chez les
patientes porteuses d’une mutation prédisposante,
d’une ABP vers l’âge de 40 ans, sous réserve qu’il n’y
ait pas de projet de grossesse (7). En effet, l’ABP est
la seule intervention dont le bénéfi ce sur la survie a
été démontré. Par ailleurs, l’ABP réduit de 80 à 90 %
le risque de cancer de l’ovaire et de 50 % le risque
de cancer du sein (12).
Le geste chirurgical correspond à la réalisation d’une
annexectomie bilatérale (ovaires et trompes) avec
cytologie et biopsies péritonéales. Cette intervention
est réalisée par laparoscopie ; les suites opératoires sont
simples (13). La prescription d’une hormonothérapie
de substitution est le plus souvent associée à l’ABP.
Patientes mutées présentant
un cancer du sein
Traitement conservateur
La prise en charge chirurgicale doit être discutée
avec la patiente. Il est possible de réaliser un traite-
ment conservateur si le rapport du volume tumoral

16 | La Lettre du Sénologue • No 60 - avril-mai-juin 2013
Modalités de la prise en charge chirurgicale des patientes mutées
Figure 3. Patiente BRCA1 : mastectomie totale thérapeutique à gauche et mastectomie
prophylactique conservant la plaque aréolomamelonnaire à droite avec reconstruction
bilatérale par prothèse.
Figure 2. Mastectomie bilatérale prophylactique avec préservation de l’étui cutané et
de la plaque aréolomamelonnaire. Reconstruction par matrice dermique acellullaire et
prothèse. Aspect avant (à gauche) et après l’opération (à droite).
Figure 4. Mastectomie bilatérale prophylactique avec conservation de la plaque aréolo-
mamelonnaire. Coque périprothétique de grade 3 au niveau du sein droit.
DOSSIER
Prise en charge des seins
d’une “femme mutée”
sur le volume du sein l’autorise. Chez les patientes
mutées, les techniques de remodelage glandulaire
sont identiques à celles pratiquées chez les patientes
non mutées. Les différentes études menées ne
montrent pas de différence de survie globale entre
traitement conservateur et mastectomie totale chez
les patientes mutées. Bien que les données de la
littérature soient divergentes, le risque de récidive
locale ne semble pas plus élevé après un traitement
conservateur chez les patientes mutées. Le risque
de récidive locale chez ces patientes serait réduit en
cas de chimiothérapie, de traitement par tamoxifène
ou d’ABP (12).
Mastectomie bilatérale
Cette approche peut être justifi ée par le risque de
survenue d’un cancer du sein controlatéral, estimé
à 30 % à 10 ans (14). Ce risque doit être pondéré à
l’aide des paramètres suivants : âge de la patiente,
type du gène muté, statut hormonal et pronostic
à long terme du premier cancer du sein (7). Néan-
moins, les bénéfices en termes de survie de la
réalisation d’une mastectomie controlatérale pro-
phylactique (MCP), en cas de cancer du sein chez
une patiente mutée, n’ont pas été démontrés (2).
Les modalités de la reconstruction mammaire
dépendent des souhaits de la patiente, mais surtout
de la nécessité de réaliser une radiothérapie post-
opératoire. Si la radiothérapie n’est pas nécessaire,
la reconstruction par prothèses est une option
simple avec une rançon cicatricielle minime. Si
une radiothérapie postopératoire est nécessaire,
la reconstruction doit être réalisée de préférence
par une technique autologue, la reconstruction
par prothèses étant grevée d’un important taux
de complications et de résultats cosmétiques peu
satisfaisants (15).
Annexectomie bilatérale
prophylactique
L’ABP doit être discutée avec les patientes mutées
présentant un cancer du sein. Ce geste ne semble
pas réduire le risque de second cancer chez les
patientes mutées présentant un cancer du sein.
Cependant, l’ABP permettrait de réduire, dans ce
groupe de patientes, la mortalité globale, en rédui-
sant la mortalité spécifi que par cancer du sein et
cancer de l’ovaire. L’ABP semble donc présenter un
intérêt majeur chez les patientes mutées ayant un
cancer du sein (16).
Patientes mutées déjà traitées
pour un cancer du sein
Du fait du bénéfi ce en termes de mortalité globale,
l’ABP doit être discutée et proposée. La prise en
charge de ces patientes dépend des modalités du
traitement initial du cancer.

Chers abonnés, chers lecteurs,
toute l’équipe Edimark vous souhaite
un très bel été d’évasion
et de réflexion et vous donne
rendez-vous dès la rentrée !
La Lettre du Sénologue • No 60 - avril-mai-juin 2013 | 17
DOSSIER
1. Salhab M, Bismohun S, Mokbel K. Risk reducing strategies
for women carrying BRCA1/2 with a focus on prophylactic
surgery. BMC Womens Health 2010;10:28.
2. Lostumbo L, Carbine NE, Wallace J. Prophylactic mastec-
tomy for the prevention of breast cancer. Cochrane Database
Syst Rev 2010;(11):CD002748.
3. Kriege M, Brekelmans CT, Boetes C et al. Efficacy of
MRI and mammography for breast-screening in women
with a familial or genetic predisposition. N Engl J Med
2004;351(5):427-37.
4. Rebbeck TR, Friebel T, Lynch HT et al. Bilateral prophy-
lactic mastectomy reduces breast cancer risk in BRCA1 and
BRCA2 mutation carriers: the PROSE Study Group. J Clin
Oncol 2004;22(6):1055-62.
5. Grann VR, Panageas KS, Whang W, Antman KH, Neugut AI.
Decision analysis of prophylactic mastectomy and oophorec-
tomy in BRCA1-positive or BRCA2-positive patients. J Clin
Oncol 1998;16(3):979-85.
6. Institut national du cancer. Chirurgie prophylactique
des cancers avec prédisposition génétique. 2009. www.e-
cancer.fr
7. Euhus D. Managing the breast in patients who test
positive for hereditary breast cancer. Ann Surg Oncol
2012;19(6):1738:44.
8. Eldor L, Spiegel A. Breast reconstruction after prophylactic
mastectomy in women at high risk for breast cancer. Breast
J 2009;15 Suppl 1:S81-9.
9. Nahabedian MY. Acellular dermal matrices in primary
breast reconstruction: principles, concepts, and indications.
Plast Reconstr Surg 2012;130(5 Suppl 2):44S-53S.
10. Spear S, Carter ME, Schwarz A. Prophylactic mastectomy:
indications, options and reconstructive alternatives. Plast
Reconstr Surg 2005;115(3):891-909.
11. Heemskerk-Gerritsen BA, Brekelmans CT, Menke-Pluy-
mers MB et al. Prophylactic mastectomy in BRCA1/2 muta-
tion carriers and women at risk of hereditary breast cancer:
long-term experiences at the Rotterdam Family Cancer
Clinic. Ann Surg Oncol 2007;14(12):3335-44.
12. Smith KL, Isaacs C. BRCA mutation testing in determining
breast cancer therapy. Cancer J 2011;17(6):492-9.
13. Fatouros M, Baltoyiannis G, Roukos D. The predomi-
nant role of surgery in the prevention and new trends in the
surgical treatment of women with BRCA1/2 mutations. Ann
Surg Oncol 2008;15(1):21-33.
14. Metcalfe K, Lynch HT, Ghadirian P et al. Contralateral
breast cancer in BRCA1 and BRCA2 mutation carriers. J Clin
Oncol 2004;22(12):2328-35.
15. Lam TC, Hsieh F, Boyages J. The effects of post-mastec-
tomy adjuvant radiotherapy on immediate two-staged
prosthetic breast reconstruction: a systematic review. Plast
Reconstr Surg 2013. [Epub ahead of print.]
16. Domchek SM, Friebel TM, Singer CF et al. Association of
risk-reducing surgery in BRCA1 or BRCA2 mutation carriers
with cancer risk and mortality. JAMA 2010;304(9):967-75.
Références bibliographiques
Patientes mutées traitées
initialement par mastectomie :
le sein controlatéral
La simple surveillance ou la mastectomie contro-
latérale prophylactique avec ou sans reconstruction
mammaire immédiate doivent être discutées avec ces
patientes. Les critères permettant d’évaluer le bénéfi ce
de la MCP ont été énumérés plus haut. Le choix de la
technique chirurgicale utilisée lors de la MCP dépend
du type de la mastectomie et de la reconstruction
réalisées lors de la prise en charge du cancer, l’objectif
étant d’obtenir la meilleure symétrie possible.
Patiente mutée traitée initialement
par traitement conservateur
Cette situation est fréquente, du fait des délais
nécessaires à l’obtention des résultats des tests
génétiques. Cependant, l’amélioration de ces tests
devrait permettre, dans un avenir proche, un diag-
nostic rapide. Ainsi, le paramètre génétique pourra
être pris en compte lors de la prise en charge ini-
tiale de patientes présentant un cancer et suspectes
d’être porteuses d’une mutation (12).
La simple surveillance ou la MBP avec ou sans
reconstruction mammaire immédiate doivent être
discutées avec les patientes mutées initialement
traitées par traitement conservateur.
Néanmoins, la prise en charge de ces patientes
est compliquée, du fait de l’antécédent de radio-
thérapie au niveau du sein traité. En effet, l’irradia-
tion contre-indique la conservation cutanée dans
le cas où la patiente souhaite une mastectomie
bilatérale. Le choix des techniques chirurgicales
est donc limité à la mastectomie associée à une
reconstruction par lambeau. La reconstruction par
implant reste possible mais expose à un risque
élevé de complications. ■
T. Ihrai déclare ne pas avoir
de liens d’intérêts.
1
/
4
100%