Lire l'article complet

26 | La Lettre du Cardiologue • N° 506 - juin 2017
MISE AU POINT
L’essentiel de la cardiologie
du sport en 2017
Sport’s cardiology, the main points in 2017
F. Carré*, F. Schnell*
* Service de médecine du sport,
hôpital Pontchaillou, CHU de Rennes,
Inserm U I099.
A
lors que notre société est submergée par une
vague d’inactivité physique et de sédentarité
qui fait le lit des maladies chroniques, en
particulier de l’athérosclérose, et que les bienfaits
− préventifs et curatifs − de l’activité physique et
sportive sont formellement prouvés, proposer une
mise au point sur la cardiologie du sport peut sur-
prendre. Pourquoi cet article ? Les cardiologues qui
témoignent d’un intérêt croissant pour la cardiologie
du sport rencontrent de plus en plus de sportifs lors
de leurs consultations, et ils peuvent être interpellés
par leurs adaptations cardiaques. Bien que rare, le
risque d’un accident cardiovasculaire (CV) plane, et
sa prévention préoccupe le praticien. Les accidents
CV liés à la pratique sportive et leur prévention sont
l’objet de cette mise au point.
Caractéristiques de la mort
subite liée au sport
La mort subite liée au sport (MSS) est un événement
dramatique, toujours mal compris par les médias
et la population, qui comprennent mal comment
un sujet a priori en “bonne santé” peut mourir en
pratiquant une activité elle-même décrite comme
bénéfique.
Si les bienfaits à long terme du sport sont prouvés,
il est aussi vrai que pendant une pratique sportive
intense, le risque d’accident CV est transitoirement
majoré. Dans la population générale française, l’in-
cidence des accidents CV est estimée à 6,5/100 000,
pour un âge moyen de 45 ans (1). Dans la population
sportive, la collecte médiocre des données, pour
le numérateur (nombre de MSS) et le dénomina-
teur (nombre de sportifs, en particulier de loisir),
et l’oubli de la prise en compte des MSS réanimées
expliquent la variabilité et l’imprécision de l’in-
cidence de la MSS selon les études (1-3). Dans la
population générale française, deux études pros-
pectives estiment que son incidence est comprise
entre 1,5 et 1,9/100 000 (1, 2). Dans la population
sportive, les incidences proposées sont de 1/50 000
et de 1/25 000 pratiquants, respectivement avant
et après 35 ans (3, 4). La MSS est donc un événe-
ment exceptionnel et, rapporté au nombre global de
MS, le rapport bénéfice/risque de la pratique d’une
activité sportive, en particulier après 35 ans, est
très favorable à la poursuite de cette pratique (5,
6). La MSS, qui est classiquement attribuée au
jeune compétiteur, touche en réalité surtout les
pratiquants masculins de sports de loisir de plus
de 45 ans (selon les études, il y a 5 à 9 hommes
qui meurent pour 1 femme) [1-3]. L’intensité de
la pratique, et surtout le niveau d’entraînement
semblent corrélés au risque de MSS, en particulier
après 35 ans (6). Chez le jeune compétiteur, elle
serait plus fréquente chez l’Afro-Caribéen et dans
certains sports comme le basket-ball (4), mais le
rôle aggravant de la compétition est discuté (2). La
MSS, qui survient dans plus de 50 % des cas dans une
enceinte sportive (2), révèle le plus souvent une car-
diopathie méconnue mais précédée dans plus d’un
tiers des cas de symptômes minimisés, quelques
jours avant l’accident (5, 6). Après 35 ans, la cause
principale de la MSS est la maladie coronaire (6), et
avant 35 ans, les maladies CV héréditaires ou congé-
nitales prédominent devant les hypertrophies ventri-
culaires gauches idiopathiques, les myocardites, la
maladie coronaire − dont la prévalence augmente
chez les jeunes − et le rare commotio cordis (3, 4). La
variabilité méthodologique des autopsies explique
que l’ordre hiérarchique de ces pathologies reste
discuté (3). La réalisation des autopsies par un car-
diologue anatomopathologiste suit un protocole
incluant une description macroscopique, l’analyse
histologique des cavités, des coronaires et du tissu
de conduction ; la réalisation de tests toxicologiques
a été recommandée (3). Des tests génétiques, à la
recherche des syndromes les mieux connus, réalisés
systématiquement au moins avant 35 ans, devraient
donner une réponse étiologique dans au moins 20
à 30 % des MSS inexpliquées, avec tout le béné-
fice secondaire qui en résulterait pour la famille (3).

La Lettre du Cardiologue • N° 506 - juin 2017 | 27
Points forts
»Le sport est globalement bénéfique pour la santé et sa pratique doit être recommandée.
»Les accidents cardiaques liés au sport sont rares et touchent surtout les hommes d’âge moyen, prati-
quants de loisir.
»Une pratique d’endurance très intense peut chez de rares sportifs favoriser l’apparition de signes d’in-
tolérance cardiaque et essentiellement des arythmies supraventriculaires.
»
La prévention de ces accidents repose sur une bonne éducation des pratiquants, un bilan cardiovasculaire
efficace avec une interprétation adaptée aux signes du cœur de sportif et une formation de la population
aux gestes de réanimation.
Mots-clés
Cardiologie du sport
Mort subite
Visite de non-contre-
indication au sport
Highlights
»
Sport is good for health and
its practice should be recom-
mended.
»
Sport-related cardiac events
are rare and concern mostly
middle-aged men during lei-
sure-time sport practice.
»
In few athletes, a very intense
endurance practice can favor
the occurrence of cardiac
abnormalities and mainly
supraventricular arrhythmias.
»
The prevention of these
events and deleterious effects
is based on a good education
of the athletes, on an effective
cardiovascular assessment with
a specific interpretation of the
athlete’s heart signs, and on a
training of the general popu-
lation for cardiopulmonary
resuscitation.
Keywords
Sport’s cardiology
Sudden death
Pre-participation evaluation
for sport
Les inconnues et imprécisions qui persistent sur la
MSS retentissent sur la qualité de sa prévention et
méritent des études ciblées spécifiques.
Prévention des accidents
cardiovasculaires liés au sport
De nouvelles recommandations en Amérique du
Nord pour les sujets porteurs de pathologies CV
désireux de pratiquer un sport en compétition
viennent d’être proposées (7). Leur but est de
prévenir l’aggravation d’une pathologie CV et/ou
d’un accident grave, sans interdire injustement la
pratique sportive par crainte médicolégale. Elles
reposent encore principalement sur des consensus
d’experts, mais sont globalement plus permissives
que celles de 2005. La nécessité d’impliquer le
sportif et son entourage dans la décision finale est
fortement soulignée (7). Les recommandations prin-
cipales sont proposées dans le tableau, pp. 28-29.
D’un point de vue éthique, social et médical, il paraît
justifié pour les sujets a priori sains de proposer aussi
une prévention des accidents CV liés au sport. Elle
repose sur 3 actions principales : la visite médicale de
non contre-indication (VNCI) à la pratique sportive,
l’éducation du pratiquant, et la formation aux gestes
de premier secours.
La nécessité de la VNCI et le contenu de son bilan
CV font l’objet d’un débat animé. La plupart des pays
qui recommandent ou imposent légalement une
VNCI la limitent aux compétiteurs. Dans le cadre
des recommandations, les compétiteurs se limitent
aux sujets qui s’entraînent de manière structurée
pour réaliser la meilleure performance possible. En
France, depuis 2017, la loi impose une VNCI tous les
3 ans avec délivrance d’un certificat médical valable
pendant 1 an et obligation pour le sportif de remplir
de manière annuelle un questionnaire comprenant 9
items les 2 années suivantes. Toute réponse positive
à une question impose une nouvelle VNCI.
Un groupe international d’experts s’est récemment
réuni pour proposer un consensus raisonnable sur les
examens CV à inclure dans la VNCI pour le sport en
compétition (8). L’association interrogatoire, examen
physique et ECG de repos a une potentialité diagnos-
tique indéniablement supérieure à l’examen clinique
seul. Le principal reproche fait à l’ECG réside dans le
nombre de faux positifs observés chez l’athlète. Une
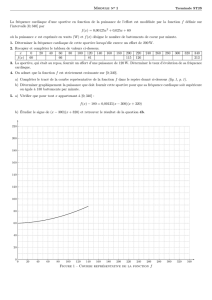
nouvelle classification internationale de l’ECG adaptée
à l’athlète a très récemment été proposée (figure, p.
30) [9]. Elle se fonde sur le risque potentiel d’aggra-
vation ou d’accident induit par la pratique sportive
intense sur une possible pathologie cardiovasculaire.
L’absence de risque des particularités ECG classées
comme ne nécessitant pas de bilan CV a été confirmée
par des études menées chez des athlètes (9). La néces-
sité d’une formation adaptée des praticiens concernés
par la VNCI pour l’analyse de l’ECG doit aussi être souli-
gnée (8). L’ajout systématique d’examens d’imagerie ne
représente pas un apport diagnostique substantiel (8).
De même, la réalisation d’une épreuve d’effort (EE), en
particulier après 35 ans, ne doit pas être systématique
mais ciblée (6), en se fondant sur la symptomatologie
éventuelle, le niveau d’entraînement et celui du risque
CV du demandeur, estimé surtout en fonction de l’âge,
du bilan lipidique et du tabagisme, et sur les caractéris-
tiques du sport désiré (10). L’EE est toujours justifiée
pour les sujets symptomatiques, porteurs d’une car-
diopathie connue, présentant au moins 2 facteurs de
risque, désireux de reprendre un sport intense après une
longue interruption (6, 10). Cette EE doit être épuisante
et non limitée à l’obtention de la fréquence cardiaque
maximale théorique, souvent dépassée par les sportifs
qui sont peu limités mus culairement. La détection de
la maladie coronaire est la cause principale de l’indi-
cation préventive de l’EE chez le sportif. Sa limite est
une faible détection du risque de rupture de plaque
malgré une bonne détection de l’angor ; cette limite
doit être connue des praticiens et clairement expliquée
au sportif, qui peut à tort considérer une EE normale
comme une “assurance tous risques”.
In fine, la décision d’une VNCI obligatoire au niveau
d’une population reste une décision gouvernemen-
tale. Les désaccords sur son contenu CV, essentiel-
lement pour l’ECG, s’expliquent par des différences
culturelles et sociales et par des contraintes juri-
diques spécifiques aux pays. Hors de ces contraintes
légales, une VNCI devrait être proposée aux prati-
quants d’activités sportives intenses et régulières
avec information sur ses avantages et ses limites (8).
Les circonstances de survenue des accidents − symp-
tômes non pris en compte et non-prise en compte
des facteurs favorisants −, et la population (âge,

28 | La Lettre du Cardiologue • N° 506 - juin 2017
MISE AU POINT L’essentiel de la cardiologie du sport en 2017
Tableau. Résumé des nouvelles recommandations américaines concernant la pratique sportive en compétition des sujets présentant une pathologie cardio-
vasculaire. Les pathologies cardiovasculaires congénitales ne sont pas abordées (D’après B.J. Maron et al. [7]).
Pathologie cardiovasculaire Pratique sportive
Classification de Mitchell Conservée avec ses limites :
– Tenir compte du niveau maximal de l’effort si variable entraînement/per-compétition
– Rôle de l’environnement et du niveau d’acclimatation
– Impact psychologique de la compétition
– En cas de traitement anticoagulant, les sports avec chocs sont contre-indiqués, quelle que soit la pathologie en cause.
Le cas des antiagrégants n’est pas traité
Après récupération d’un
commotio cordis
Un bilan cardiologique, en particulier rythmologique, est justifié. S’il est normal, aucune restriction sportive
Hypertension artérielle – Aucune restriction sportive si pré-hypertension ou HTA de grade 1 sans atteinte d’organe
– Si HTA de grade 2, attendre contrôle tensionnel, surtout si sports statiques (classés III)
Maladie coronaire – Après accident, bilan classique avec échographie de repos et EE sous traitement (capacité physique, ischémie,
arythmies)
– Traitement et équilibre des facteurs de risque, surtout hypercholestérolémie
– Discussion avec le patient sur la balance bénéfices/risques du sport intense
– Aucune restriction sportive si coronarien asymptomatique avec FEVG > 50 %, sans ischémie ni TDR
– Autres cas : restriction aux sports IA et IIA. Interdiction de compétition au moins 3 mois après revascularisation
ou si aggravation des symptômes et/ou ischémie
Cardiomyopathies CMH probable ou certifiée : quels que soient les critères de gravité et le traitement, autorisation pour sports IA
– CMH génotype+ phénotype– sans antécédent MS familial par CMH : aucune restriction sportive
– Pas de traitement anti-arythmique ni DCI pour autoriser sport intense
– NCVG asymptomatique et FEVG normale, sans TDR ventriculaires complexes : aucune restriction sportive
– Autres cas NCVG : autorisation pour la pratique des sports IA
– Cardiomyopathie dilatée, restrictive primaire ou infiltrative : parfois autorisation pour la pratique sports IA
– MAVD certifiée, probable ou possible : parfois autorisation pour la pratique sports IA
Myocardites Arrêt de tout sport intense 3 à 6 mois. Normalisation totale : aucune restriction sportive, sinon pas de sport en
compétition. Si rehaussement tardif persistant asymptomatique : pas de restriction sportive et surveillance
Péricardites – Aiguës ou chroniques : aucun sport
– Si récupération complète : aucune restriction
TDC – BAV complet congénital asymptomatique : aucune restriction
– Si symptomatique : QRS > 120 ms, FC repos < 40 bpm. PM indiqué et sport adapté. Restriction adaptée après EE.
TDRSV – FA faible risque bien tolérée et arrêt spontané : aucune restriction sportive. Ablation traitement de choix.
– Flutter ablation.
– TSV ablation recommandée.
– Pré-excitation asymptomatique, EEP avec ablation si nécessaire.
– Après ablation efficace, pas de restriction

La Lettre du Cardiologue • N° 506 - juin 2017 | 29
MISE AU POINT
Pathologie cardiovasculaire Pratique sportive
TDRV – ESV isolées ou complexes asymptomatiques sur cœur sain, pas de restriction
– Si symptôme : traitement et ablation si traitement inefficace
– Si cardiopathie, sport IA ou aucun sport.
– TVNS sur cœur sain disparaissant à l’EE : pas de restriction, discussion ablation
– TVNS effort sur cœur sain : limitation sports IA. Après traitement, EE et EEP : discussion autres sports.
– TVNS et cardiopathie : limitation aux sports IA
– TVS monomorphes et cœur sain : traitement et/ou essai ablation. Si EE et EEP normal : pas de restriction
– TVS monomorphes et cardiopathie : limitation aux sports IA
– ACR sur TV ou FV et cardiopathie : DCI, si cardiopathie réversible, reprise sport après 3 mois
Syncope, PM, DCI – Syncope neurologique : aucune restriction
– PM permanent sans cardiopathie : sport sans collision, sauf si protection adaptée
– PM et cardiopathie : sport selon cardiopathie
– DCI: pas de sport pendant 3 mois, limitation aux sports IA ou selon cardiopathie, discussion avec patient
etautorisation autre sport possible au cas par cas
Canalopathies – Avis spécialisé
– Canalopathie génotype+ phénotype– : aucune restriction sportive. Respect règles de sécurité et si possible DEA
personnel et entourage formé
– Brugada : aucune restriction sauf si port de DCI
– QT long traité asymptomatique > 3 mois : pas restriction sportive sauf natation pour LQT1 et sauf si DCI–
– TV polymorphe catécholergique : aucun sport, exception possible après avis spécialisé
Valvulopathies – Toujours EE au mieux avec VO2 : adaptations, capacité physique, arythmies, segment ST. Suivi annuel.
– Sténose aortique : minime, pas de restriction ; modérée : limitation sports IA, IB, IIA ; serrée : aucun sport.
– Fuite aortique : minime-modérée ou sévère, dilatation VG absente ou modérée, FEVG normale : pas de restriction.
Sévère et symptôme et/ou EE anormale et/ou dilatation marquée : aucun sport. Si dilatation aorte minime à modérée,
pas de sport avec collision.
– Sténose mitrale, si minime : pas de restriction ; si sévère : aucun sport ou limitation aux sports IA.
– Fuite mitrale : si minime-modérée et rythme sinusal, VG non ou peu dilaté, FEVG normale sans HTAP, pas de
restriction ; si sévère, sinusal, FEVG normale, et dilatation VG : restriction IA, IIA, IB ; si sévère, VG dilaté, HTAP, FEVG
anormale : aucun sport ou IA.
– Valvulaire opéré : bioprothèses aorte ou mitrale, fonctions valves et VG normales, restriction aux sports IA, IB, IC,
IIA. Dilatation percutanée ou commissurotomie mitrale, sport selon sévérité résiduelle. Chirurgie sténose mitrale ou
valvulopathie aortique sans fuite résiduelle et fonction VG normale, restriction aux sports IA, IB, IIA avec faible risque
collision cas par cas.
– Valves mécaniques. Fonctions valves et VG normales : restriction aux sports IA, IB, IIA et pas sport avec risque collision
Pathologies de l’aorte – Bicuspidie : non compliquée, pas de restriction. Aorte 40-42 mm hommes (H) et 36-39 mm femmes (F) , Z-score2-3,5
sans sténose ni fuite : sports IA, IB, IC, IIA, IIB, IIC sans collision. Aorte 43-45 mm, Z score > 3,5 : sports IA sans
collision. Aorte > 45mm : aucun sport.
– Aorte saine : Z-score2-2,5, 40-41mm H, 35-37 mm F: pas de restriction. Dilatation plus marquée, bilan complet ±
génétique, autorisation sportive au cas par cas, attention aux sports à contrainte statique élevée
– Dissection aortique chronique ou anévrisme ou dissection autre artère : aucun sport. Anévrisme ou dissection opérés
avec succès : sport IA.
Trait drépanocytaire Pas de restriction sportive. Respect hydratation et des contraintes environnementales (chaleur et haute altitude).
Information entourage sportif
ACR : arrêt cardiorespiratoire, BAV : bloc atrioventriculaire, CMH : cardiomyopathie hypertrophique, DCI : défibrillateur cardiaque implantable, DEA : défibrillateur automatique, EE : épreuve d’effort, EEP :
exploration électrophysiologique, ESV : extrasystole ventriculaire, FA : fibrillation atriale, FEVG : fraction d’éjection du VG, FV : fibrillation ventriculaire, HTA : hypertension artérielle, HTAP : hypertension
artérielle pulmonaire, LQT1 : syndrome du QT long type 1, MAVD : maladie arythmogène du ventricule droit, NCVG : non-compaction du VG, PM : pacemaker, TDC : troubles de la conduction, TDR :
troubles du rythme, TDC : troubles de la conduction, TDRSV : troubles du rythme supraventiculaire, TSV : tachycardie supraventriculaire, TVS et TVNS : tachycardies ventriculaires soutenues et non
soutenues, VG : ventricule gauche.

30 | La Lettre du Cardiologue • N° 506 - juin 2017
MISE AU POINT L’essentiel de la cardiologie du sport en 2017
Limite chez l’athlète
– Axe QRS anormal
– Hypertrophie atriale
électrique
– BBD complet
Normal chez l’athlète Aspects anormaux
– Bradycardie sinusale et/ou
arythmie respiratoire
– Rythme jonctionnel ou ectopique
– BAV degré 1
BAV degré 2 Mobitz 1
– Amplitude de QRS avec critères
d’HVG ou HVD
– BBD incomplet
– RP ou élévation ST
– ST surélevé en dôme avec ondes
– T négatives V1-V4 chez athlètes A-C
– T négatives V1-V3 avant 16 ans
Pas de bilan CV complémentaire
si athlète asymptomatique sans
antécédent familial de cardiopathie
héréditaire ni de mort subite cardiaque
avant 50 ans
≥ 2 signes 1 signe
Bilan CV complémentaire justifié
pour détecter une pathologie CV
à risque d’accident grave lors du sport
– Bradycardie majeure < 30 bpm
– ≥ 2 extrasystoles
– Tachyarythmies supraventriculaires
– PR ≥ 400 ms
– BAV degré 2 Mobitz 2
– BAV degré 3
– Pré-excitation ventriculaire
– Ondes Q pathologiques
– BBG complet
– QRS ≥ 140 ms
– Sous-décalage ST
– T négatives sauf avR, D3, V1
– QTc prolongé (> 470 ms H, 480 ms F)
– Aspect Brugada type 1
– Onde epsilon
Figure. Critères d’interprétation de l’ECG de repos de l’athlète (≥ 4 h/sem. de sport)
[d’après Sharma S et al. (9)].
A-C : Afro-Caribéens ; BAV : bloc atrioventriculaire ; BBD, BBG : bloc de branche droit
ou gauche ; CV : cardiovasculaire ; F : femmes ; H : hommes ; HVG ou HVD : hypertrophie
électrique ventriculaire gauche ou droite ; QTc : durée QT corrigée par la formule de Bazett ;
RP : repolarisation précoce.
niveau de préparation) concernée (3, 6) montrent
qu’une éducation sur la bonne pratique des acti-
vités sportives pourrait diminuer significativement
l’incidence des MSS dans la population générale.
Soulignons l’absolue nécessité de consulter en cas
de symptômes évocateurs, de s’abstenir de pratiquer
un sport intense en cas de fièvre et/ou de syndrome
viral et, pour les fumeurs invétérés, de s’abstenir
de fumer dans les 2 heures précédant et suivant la
pratique sportive. La simplicité et le faible coût de
cette action éducative plaident pour sa diffusion
et son utilisation.
Dans plus de 90 % des cas, l’accident CV survient en
présence de témoins ; des gestes de premiers secours
efficaces et la présence d’un trouble du rythme cho-
quable représentent les 2 principaux facteurs pro-
nostiques en cas d’arrêt cardiorespiratoire (3). Une
éducation aux gestes de réanimation la plus large
possible dans le monde sportif doit donc être réalisée.
Le sport intense peut-il devenir
délétère pour un cœur sain ?
En 2011, la Haute Autorité de santé (HAS) a reconnu
l’activité physique et sportive comme une théra
-
peutique non médicamenteuse. Mais cette poly-
pill pourrait-elle avoir des effets délétères en cas
d’excès ?
On sait que la pratique sportive intense, par les
modifications environnementales cellulaires qu’elle
induit, peut déclencher des arythmies graves en cas
de foyer arythmogène sous-jacent. L’endurance
intense peut aussi aggraver des cardiopathies
arythmogènes héréditaires comme la maladie aryth-
mogéne du ventricule droit (7, 11). Le sport intense
pratiqué en période infectieuse, surtout virale, aug-
mente le risque d’arythmies en cas de localisation
myocardique inflammatoire.
La question de savoir si la pratique effrénée d’un
sport d’endurance peut à long terme créer un foyer
arythmogène reste très débattue (11, 12).
La notion de fatigue cardiaque est ancienne. Dès les
années 1970, des études rapportaient une baisse de
la fonction systolique, une dilatation cavitaire et
des signes radiologiques de surcharge pulmonaire
transitoires chez des athlètes asymptomatiques
à l’arrivée d’un marathon. Les moyens d’explora-
tion actuels ont affiné ces observations. En bref,
après un effort intense d’endurance, 50 % des par-
ticipants environ présentent des signes de fatigue
myocardique avec, à l’échographie, une dilatation
et une baisse des fonctions diastolique et systolique
plus nettes sur le ventricule droit et, à l’analyse
biologique, une élévation de la troponine et du
BNP. Ces anomalies très transitoires (normalisa-
tion ≤ 24 heures) concernent des athlètes toujours
cliniquement asymptomatiques et sans anomalie
ECG ou tissulaire à l’IRM associée. Ces adaptations
sont donc actuellement considérées comme physio-
logiques. De plus, le très faible nombre d’accidents
CV (0,54 MSS/100 000) lors des semi-marathons
et marathons et la longévité prolongée de 4 à 6 ans
des athlètes, surtout endurants, de haut niveau par
rapport à la population générale, sont des éléments
rassurants.
Il est néanmoins justifié d’étudier le retentissement
potentiel à long terme des effets myocardiques de
ces épreuves, surtout si elles sont répétées et pra-
tiquées par des sportifs d’âge moyen (de plus de
40-45 ans).
Le risque de fibrillation atriale (FA), favorisée par une
longue pratique de l’endurance, reste le mieux docu-
menté. Les caractéristiques cliniques et physiopatho-
logiques de la FA de l’athlète ont été très récemment
revues (13). La FA concerne les vétérans (45-65 ans)
masculins pratiquant un sport d’endurance à haute
intensité depuis plusieurs années, et exempts des
facteurs de risque classique de la FA. Les femmes
semblent protégées. La FA est surtout paroxystique
 6
6
1
/
6
100%