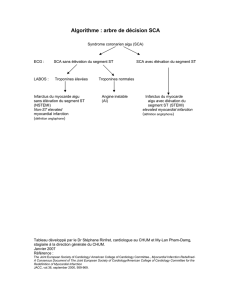
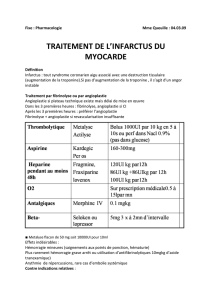
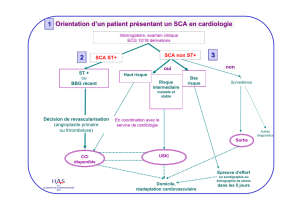
Urgences valvulaires critiques

8 | La Lettre du Cardiologue • n° 445 - mai 2011
CONGRÈS
RÉUNION
TUC 2011
23-25 mars 2011
Paris
Urgences valvulaires critiques
B. Iung*
* Département de cardiologie, hôpital
Bichat-Claude-Bernard, Paris.
U
ne des sessions du congrès Thromboses
et urgences coronaires (TUC) 2011 était
consacrée aux situations d’urgence dans
les cardiopathies valvulaires, très hétérogènes, qui
ont en commun de poser la question des difficultés
d’indication d’intervention en urgence.
Décompensation aiguë
des valvulopathies chroniques
D’après une communication du Pr Bernard Iung, Paris
Le diagnostic de valvulopathie est parfois difficile à
poser car, dans des conditions de bas débit, le souffle
cardiaque peut être de faible intensité, ce qui souligne
l’importance d’une échocardiographie précoce en
cas d’insuffisance cardiaque aiguë, sachant que les
conditions hémodynamiques peuvent rendre difficile
la quantification de la sévérité des sténoses, comme
des régurgitations.
Rétrécissement aortique calcifié
L’utilisation des vasodilatateurs et des inotropes ne doit
pas être restreinte en cas de rétrécissement aortique
calcifié (RAC) décompensé. Même si le traitement
médical permet souvent une amélioration immédiate,
le pronostic à court terme est mauvais – avec une
médiane de survie entre 1 et 2 ans –, d’autant plus
qu’une dysfonction ventriculaire gauche est presque
toujours associée. La mortalité opératoire est accrue
chez ces patients : supérieure à 10 % dans la plupart des
séries. Les études comparatives montrent cependant
que les patients présentant un RAC très symptoma-
tique avec dysfonction ventriculaire gauche sont ceux
pour lesquels, par rapport à leur histoire naturelle, le
traitement chirurgical est le plus bénéfique.
L’analyse du rapport bénéfice-risque doit être indivi-
dualisée, car les patients présentant un RAC décom-
pensé avec dysfonction ventriculaire gauche sont
plus âgés et présentent davantage de comorbidités
que ceux ayant une fraction d’éjection conservée,
ce qui contribue à augmenter le risque opératoire
indépendamment de l’état hémodynamique.
La dilatation aortique percutanée permet une amélio-
ration transitoire en cas de RAC compliqué d’un choc
cardiogénique, mais elle n’est justifiée que lorsqu’une
chirurgie est possible secondairement. L’implanta-
tion d’une prothèse aortique par voie percutanée
est attractive bien qu’elle n’ait fait l’objet d’aucune
étude spécifique dans le RAC en cas d’insuffisance
cardiaque aiguë.
Insuffisance aortique
L’insuffisance aortique chronique est bien tolérée
longtemps en raison de la dilatation progressive du
ventricule gauche. Au stade tardif de dysfonction
ventriculaire gauche sévère, les résultats de la chirurgie
sont moins bons, mais, désormais, des données
montrent un bénéfice par rapport à l’histoire naturelle.
Insuffisance mitrale organique
Dans l’insuffisance mitrale (IM) organique sévère avec
dysfonction ventriculaire gauche, la chirurgie, surtout
lorsqu’elle est conservatrice, peut être effectuée avec
une mortalité opératoire acceptable. En revanche, le
résultat à moyen terme est compromis par la persis-
tance d’une dysfonction ventriculaire gauche rési-
duelle. Ce résultat explique que les recommandations
d’intervention sont plus restrictives lorsqu’une IM
organique s’accompagne d’un retentissement ventri-
culaire gauche sévère (fraction d’éjection < 30 % ou
diamètre télésystolique > 55 mm).
Insuffisance mitrale fonctionnelle
L’IM fonctionnelle étant la conséquence, et non la
cause, d’une dysfonction ventriculaire gauche, son
traitement est avant tout le traitement de l’insuffi-
sance cardiaque par dysfonction systolique, incluant
la resynchronisation si indiquée. La correction chirur-
gicale de l’IM fonctionnelle peut avoir un effet béné-
fique sur le remodelage ventriculaire gauche, mais son
impact sur les symptômes demeure controversé et
aucun bénéfice sur la survie n’a été mis en évidence.
Les indications de correction chirurgicale de l’IM fonc-
tionnelle sont surtout envisagées lorsqu’une revascu-
larisation myocardique est par ailleurs indiquée. Les
techniques de traitement percutané de l’IM ont fait
la preuve de leur faisabilité bien que leur évaluation
dans cette indication soit encore préliminaire.
Rétrécissement mitral
Le principal facteur de risque de décompensation
aiguë du rétrécissement mitral n’est pas la dysfonc-

La Lettre du Cardiologue • n° 445 - mai 2011 | 9
CONGRÈS
RÉUNION
tion ventriculaire gauche mais les troubles du rythme
rapide. Sur le plan interventionnel, la commissuro-
tomie mitrale percutanée doit être favorisée dans
ces circonstances lorsque les conditions cliniques et
anatomiques sont propices.
Indications chirurgicales
dans l’endocardite aiguë
D’après une communication du Pr Pascal Leprince,
Paris
Comme en témoignent les résultats parfois contradic-
toires d’études observationnelles récentes, le béné-
fice de la chirurgie précoce est difficile à évaluer. Ce
bénéfice est principalement mis en évidence en cas de
complication hémodynamique, infectieuse ou embo-
lique. Les indications sont désormais plus clairement
codifiées dans les recommandations de la Société
européenne de cardiologie, qui incluent notamment
le délai dans lequel l’intervention est souhaitable.
L’indication opératoire est formelle et urgente en cas
d’insuffisance cardiaque réfractaire en rapport avec
une régurgitation volumineuse ou une fistule. Elle
est moins urgente en cas d’insuffisance cardiaque
contrôlée. La chirurgie peut également être envi-
sagée en cas de régurgitation volumineuse, surtout
aortique, sans signe d’insuffisance cardiaque, en
particulier lorsque le risque opératoire est modéré.
Les indications opératoires pour des raisons infec-
tieuses sont principalement justifiées par la présence
de lésions périvalvulaires (abcès périvalvulaire ou
périprothétique), plus rarement par la persistance
d’un sepsis avec hémocultures positives ou en raison
de germes résistant au traitement médical.
Les indications justifiées par le risque embolique sont
formelles en cas de végétation résiduelle mesurant
plus de 10 mm et associée à un épisode embolique. En
l’absence d’embolie, les indications reposant unique-
ment sur la taille de la végétation sont plus controver-
sées et ne sont envisagées que pour des végétations
mesurant plus de 15 mm. Les indications d’ordre
embolique doivent être envisagées précocement,
durant les 2 premières semaines suivant le début de
l’antibiothérapie, période durant laquelle le risque
de récidive embolique est le plus élevé. La présence
d’un accident vasculaire cérébral ne contre-indique la
chirurgie que lorsqu’il s’agit d’un accident vasculaire
cérébral hémorragique ou d’un accident vasculaire
cérébral ischémique très étendu, notamment chez
un patient comateux.
D’une façon générale, les indications de chirurgie
précoce sont d’autant plus larges que le patient
est jeune et que le micro-organisme en cause est
virulent, en particulier s’il s’agit d’un staphylocoque
doré. Le caractère particulièrement polymorphe
de l’endocardite infectieuse souligne l’importance
d’une évaluation multidisciplinaire précoce afin d’en
optimiser la prise en charge médico-chirurgicale.
Thromboses de prothèses
D’après une communication du
Pr Raymond Roudaut, Bordeaux
Les thromboses de prothèses concernent princi-
palement les prothèses mécaniques. Il s’agit d’une
complication rare (< 1 pour 100 années-patients)
mais grave, avec une mortalité dépassant 10 %. Les
facteurs favorisants sont la position mitrale de la
prothèse, le bas débit et surtout une anticoagulation
insuffisante.
Le diagnostic repose sur l’échocardiographie trans-
thoracique et transœsophagienne et le radio-cinéma
de la prothèse, qui apportent des informations
complémentaires et doivent donc être tous effec-
tués en cas de suspicion de thrombose de prothèse.
Les 2 options thérapeutiques sont principalement la
chirurgie et la thrombolyse. La chirurgie comporte
un risque relativement élevé, car il s’agit d’une réin-
tervention souvent effectuée dans des conditions
hémodynamiques instables. Cependant, la thrombo-
lyse est grevée de mortalité (5 à 10 % des cas), d’un
risque thrombo-embolique (5 à 15 % des cas) et
d’un risque hémorragique (autour de 8 % des cas).
Le risque d’échec de la thrombolyse est augmenté
lorsque le thrombus mesure plus de 10 mm.
Bien qu’il existe peu de séries comparatives, celles-ci
favorisent le recours à la chirurgie comme traitement
de première intention. Les indications de la thrombo-
lyse selon les recommandations actuelles concernent
principalement les thromboses prothétiques du cœur
droit et les thromboses prothétiques du cœur gauche
lorsqu’il existe une instabilité hémodynamique et
qu’une chirurgie ne peut être effectuée en urgence
pour des raisons d’éloignement. Certaines équipes
favorisent la thrombolyse en première intention
sur les thromboses obstructives du cœur gauche de
petite taille, mais cette attitude demeure contro-
versée et n’est pas reprise dans les recommandations
actuelles.
Les thromboses prothétiques non obstructives sont
diagnostiquées par l’échocardiographie transœso-
phagienne. Le risque, essentiellement embolique,
est relativement faible, et ces thromboses justifient
donc un traitement médical de première intention,
associant généralement anticoagulant et antiagré-
gant plaquettaire. ■
Pour en savoir plus…
##
#Vahanian A, Baumgartner H,
Bax J et al. Guidelines on the
management of valvular heart
disease: The Task Force on the
Management of Valvular Heart
Disease of the European Society
of Cardiology. Eur Heart J
2007;28(2):230-68.
##
#Habib G, Hoen B, Tornos P
et al. Guidelines on the preven-
tion, diagnosis, and treatment
of infective endocarditis (new
version 2009): the Task Force on
the Prevention, Diagnosis, and
Treatment of Infective Endo-
carditis of the European Society
of Cardiology (ESC). Eur Heart J
2009;30(19):2369-413.
##
#Delahaye F. Is early surgery
beneficial in infective endocar-
ditis? A systematic review. Arch
Cardiovasc Dis 2011;104(1):
35-44.
##
#Roudaut R, Lafitte S, Roudaut MF
et al. Management of prosthetic
heart valve obstruction: fibrino-
lysis versus surgery. Early results
and long-term follow-up in
a single-centre study of 263
cases. Arch Cardiovasc Dis 2009;
102(4):269-77.
Conflit d’intérêts. L’auteur
déclare avoir un conflit d’intérêts
avec Servier, Boehringer Ingelheim,
Valtech, St Jude Medical, Edwards
Life sciences, Sanofi-Aventis.

10 | La Lettre du Cardiologue • n° 445 - mai 2011
CONGRÈS
RÉUNION
TUC 2011
23-25 mars 2011
Paris
Accident ischémique transitoire
expliqué aux non-neurologues
L. Krapf*
* Service de cardiologie, hôpital
Bichat-Claude-Bernard, Paris. C
ette thématique a été l’objet d’une présenta-
tion de P. Lavallée (Paris) lors du congrès TUC.
L’accident ischémique transitoire (AIT) se
définit comme une dysfonction neurologique tran-
sitoire causée par une ischémie focale cérébrale,
rétinienne ou médullaire, sans qu’un infarctus puisse
être mis en évidence. Les symptômes doivent être
focaux (c’est-à-dire correspondre à un territoire vas-
culaire), de survenue brutale et négatifs (perte de
fonction). L’examen neurologique est normal. Les
symptômes concernent le territoire carotidien dans
75 % des cas, vertébrobasilaire dans 25 % des cas.
Le diagnostic est difficile : selon les études, il est
confirmé dans uniquement 38 % des cas adressés,
et la variabilité interobservateur entre 2 neurologues
est moyenne. Il est important de connaître et de
rechercher les diagnostics différentiels, surtout en
cas de symptômes atypiques (migraines, vertiges,
troubles de la mémoire, diplopie).
Le risque est celui d’un AVC, évalué à 5 % dans les
48 heures qui suivent un AIT et à 10 % dans les 3 mois
suivants. Ce risque diffère en fonction de l’étiologie ou
selon l’atteinte à l’imagerie ; il peut aussi être évalué au
moyen du score ABCD2 (Age, Blood pressure, Clinical
features, Duration of symptom, Diabetes) [1]. Mais l'éva-
luation doit cependant être globale et tenir compte de
tous ces éléments cliniques et paracliniques (même
chez des patients avec un score bas, le risque d’AVC
reste de 20 % [2]). Les recommandations du NICE
de 2008 codifient la prise en charge selon le risque.
Les étiologies principales sont l’athérosclérose
intra- et exocrânienne, l’atteinte des petits vaisseaux
(lacunes) et l’accident cardioembolique.
L’imagerie cérébrale en urgence permet :
➤➤
d’éliminer une cause non ischémique (hémor-
ragie, tumeur, hématome sous-dural) ;
➤➤de confirmer le diagnostic (IRM en diffusion) ;
➤➤
d’obtenir une investigation artérielle dans le
même temps.
L’IRM avec séquences en diffusion a une meilleure
sensibilité que le scanner pour la détection de lésions
précoces souvent réversibles, et pour éliminer un
diagnostic différentiel ; le choix dépendra surtout
de l’accessibilité et d’éventuelles contre-indications.
Le bilan étiologique comprendra systématiquement :
➤➤
une imagerie artérielle sans délai (indication
d’endartériectomie en urgence ?) ;
➤➤
un électrocardiogramme (à la recherche d’une
arythmie complète avec fibrillation auriculaire) ;
➤➤une échocardiographie ;
➤➤
un bilan biologique : troubles métaboliques,
glycémie, polyglobulie, bilan des facteurs de risque
cardiovasculaires.
La priorité est guidée par la clinique : l’échocardio-
graphie est rapidement demandée en cas de prothèse
valvulaire ou de symptômes dans différents territoires
artériels ; le doppler des troncs supra-aortiques en cas de
souffle carotidien ; des AIT répétés dans le même terri-
toire évoquent une atteinte artérielle ; un syndrome de
Claude Bernard-Horner évoque une dissection carotide.
Le traitement est à débuter immédiatement par de
l’AAS 300 mg en i.v. puis 75 mg/j avant toute imagerie
(pas d’effet délétère démontré). Une endartériectomie
devra être réalisée dans les 2 semaines si la sténose
carotidienne est supérieure à 70 % (norme ECST).
Les facteurs de risque cardiovasculaire devront être
traités et l’examen devra rechercher d’autres atteintes
artérielles.
Un traitement anticoagulant pourra être prescrit
(il n’existe pas de recommandations actuellement
dans le cadre d’AIT. Le risque hémorragique paraît
plus faible que dans le cas d’un AVC mais le risque
de récidive embolique également).
Les indications d’hospitalisation ne sont pas scien-
tifiquement établies : sténose artérielle très serrée,
maladie cardioembolique, présentation clinique “cres-
cendo”. L’hospitalisation est intéressante sur le plan de
la surveillance (risque de récidive), de l’instauration de
traitements spécifiques, de la réalisation plus rapide
des examens, de la surveillance télémétrée.
Les cliniques spécialisées dans les AIT (SOS AIT)
permettent la réception d’appels 24 h/24 par une
infirmière formée ou un neurologue de garde, qui
orientent éventuellement le patient en hospitalisa-
tion. La mise en place de ces structures a permis une
diminution du risque d’AVC en 3 mois de 10 à 3 % (3).
L’éducation du patient est primordiale : explications sur
la pathologie, reconnaissance des symptômes, conduite
à tenir en cas de récidive, risque cardiovasculaire.
En conclusion, l’AIT est un signe d’alerte dont le
diagnostic peut être difficile, nécessitant une évalua-
tion et une prise en charge rapides et spécialisées
pour permettre une diminution de 80 % du risque
d’AVC. ■
Références
bibliographiques
1.#Rothwell PM, Giles MF, Floss-
mann E et al. A simple score
(ABCD) to identify individuals
at high early risk of stroke after
transient ischaemic attack.
Lancet 2005;366(9479):29-36.
2.#Amarenco P, Labreuche J,
Lavallée PC et al. Does ABCD2
score below 4 allow more time
to evaluate patients with a tran-
sient ischemic attack? Stroke
2009;40(9):3091-5.
3.#Rothwell PM, Giles MF, Chan-
dratheva A et al. Effect of urgent
treatment of transient ischaemic
attack and minor stroke on early
recurrent stroke (EXPRESS study):
a prospective population-based
sequential comparison. Lancet
2007;370(9596):1432-42.

La Lettre du Cardiologue • n° 445 - mai 2011 | 11
CONGRÈS
RÉUNION
TUC 2011
23-25 mars 2011
Paris
Références
bibliographiques
1.#Wallace TW, Abdullah SM,
Drazner MH et al. Prevalence and
determinants of troponin T eleva-
tion in the general population.
Circulation 2006;113:1958-65.
2.# Brekke PH, Omland T,
Holmedal SH, Smith P, Søyseth V.
Troponin T elevation and long-term
mortality after chronic obstructive
pulmonary disease exacerbation.
Eur Respir J 2008;31:563-70.
3.# Sundström J, Ingelsson E,
Berglund L et al. Cardiac
troponin- I and risk of heart
failure: a community-based
cohort study. Eur Heart J
2009;30:773-81.
4.#Miller WL, Hartman KA,
Burritt MF et al. Serial biomarker
measurements in ambulatory
patients with chronic heart
failure: the importance of
change over time. Circulation
2007;116;249-57.
5.# Thygesen K, Alpert JS,
White HD; Joint ESC/ACCF/
AHA/WHF Task Force for the
Redefinition of Myocardial
Infarction. Universal definition of
myocardial infarction. Eur Heart
J 2007;28:2525-38.
6.#Agewall S, Giannitsis E,
Jernberg T, Katus H. Troponin
elevation in coronary vs. non-
coronary disease. Eur Heart
J 2011;32:404-11.
7.#Jeremias A, Gibson CM. Narra-
tive review: alternative causes for
elevated cardiac troponin levels
when acute coronary syndromes
are excluded. Ann Intern Med
2005;142(9):786-91.
Troponine non coronaire
L. Krapf*
* Service de cardiologie, hôpital
Bichat-CLaude-Bernard, Paris.
L
a troponine non coronaire a été le sujet des
communications présentées par les Prs P. Jour-
dain (Pontoise), E. Bonnefoy (Lyon) et P. Ray
(Paris) lors du congrès TUC.
Élévation chronique
de la troponine
L’élévation de la troponine circulante est un marqueur
de dommages myocardiques, principalement de l’in-
farctus du myocarde (IDM). Elle peut cependant être
détectée en dehors de ce contexte. Dans une étude
sur une population générale, 0,7 % des dosages de
troponine étaient positifs et étaient corrélés à la
présence d’insuffisance cardiaque, d’hyper trophie
ventriculaire gauche, d’insuffisance rénale chronique
et de diabète (1). Dans une population de BPCO en
décompensation, 43 % des dosages de troponine
étaient positifs et associés à un pronostic défavo-
rable (2). La troponine est donc souvent élevée dans
des situations diverses, en particulier dans l’insuffi-
sance cardiaque, même stable.
L’identification par la troponine circulante du dégât
myocardique peut avoir une valeur pronostique,
même en l’absence de syndrome coronarien aigu
(SCA). L’augmentation de la troponine de plus de 20 %
d’un prélèvement à l’autre serait un marqueur pronos-
tique péjoratif, le taux de 0,03 ng/ml paraissant plus
fiable pour prédire la mortalité (3). La variabilité de
la troponine au cours du temps est faible, présentant
peu d’intérêt pour le suivi, mais sa valeur pronostique
en association avec le BNP est augmentée (4).
Troponine non coronaire
avec infarctus
Dans la définition universelle de l’IDM (5), l’IDM de
type 2 correspond au déséquilibre entre apports et
besoins en oxygène du myocarde sans occlusion
coronaire (mismatch).
Quatre-vingt-quinze pour cent des SCA avec sus-
décalage du segment ST sont de type 1 (avec événe-
ment aigu coronaire) ; en l’absence de sus-décalage
du segment ST (NSTEMI), 40 à 60 % sont de type 1
et 40 à 60 % de type 2.
En faveur d’un IDM de type 2 on recherchera un
terrain avec coronaropathie et les éléments pour
un mismatch : diminution des apports (hypotension,
anémie, hypoxie, tachycardie) et/ou augmentation
des besoins (tachycardie, fièvre).
En pratique, devant des symptômes sans sus-décalage
du segment ST et avec élévation de la troponine :
➤➤
Si le SCA est peu probable : l’élévation de la tropo-
nine peut être non coronaire ;
➤➤Si le SCA est probable :
➤#
avec mismatch : corriger “vigoureusement” ce
mismatch ;
➤#
sans mismatch : NSTEMI à traiter selon les recom-
mandations.
Troponine non coronaire
Outre les IDM de types 1 et 2, il existe de nombreuses
causes de libération de la troponine non clairement
reliées à un événement thrombotique coronaire :
insuffisance cardiaque aiguë, AVC, embolie pulmo-
naire, rhabdomyolyse, exacerbation de BPCO, exer-
cice, chimiothérapie (6). Le mécanisme peut être le
mismatch, mais celui-ci n’est pas le seul et certains
restent méconnus (tableau) [7].
En conclusion, l’augmentation de la troponine est
fréquemment retrouvée en dehors des SCA, et ses
mécanismes ne sont pas tous appréhendés. Il faut
reconnaître le SCA et le mismatch pour les traiter
de façon adaptée. Hors du contexte de SCA chez un
patient âgé, insuffisant cardiaque, insuffisant rénal,
l’augmentation de la troponine peut être un élément
pronostique. ■
Tableau. Causes non thrombotiques et mécanismes
présumés de l’élévation de la troponine.
Diagnostic Mécanisme
Sepsis, tachycardie,
choc/hypotension
Mismatch
AVC Déséquilibre du système
nerveux autonome
Contusion myocardique Traumatisme direct
Chimiothérapie Toxicité myocardique directe
Embolie pulmonaire Dilatation du ventricule droit
Insuffisance cardiaque,
exercice prolongé
Contrainte pariétale
ventriculaire
Tako-tsubo,
sympathomimétiques
Effets adrénergiques directs
Insuffisance rénale
chronique
Inconnu

12 | La Lettre du Cardiologue • n° 445 - mai 2011
CONGRÈS
RÉUNION
TUC 2011
23-25 mars 2011
Paris
Physiopathologie et prise
en charge de la fibrillation
atriale chez les patients
avec une dysfonction
ventriculaire gauche
L. Mimoun*
* Service de cardiologie, hôpital
Bichat-Claude-Bernard, Paris.
Fibrillation atriale,
cause ou conséquence
de la dysfonction ventriculaire
gauche ?
D’après une communication de B. Gersh, États-Unis
Les deux ! Il existe un cercle vicieux entre la fibrilla-
tion atriale (FA) et la dysfonction du ventricule
gauche (VG), la FA étant à la fois cause et consé-
quence. Ainsi, chez les patients avec une insuf-
fisance cardiaque (IC) chronique, systolique ou
diastolique, l’incidence de la FA augmente avec le
stade NYHA. En parallèle, la FA altère le pronostic
des patients, avec une augmentation de la morta-
lité et d’hospita lisations d’origine cardiovasculaire.
L’orateur a souligné le cas particulier de la cardio-
myopathie induite par la FA dite rythmique, dont
l’incidence est probablement sous-estimée : 5 %
des cas de survenue de FA sur cœur sain s’accompa-
gnent d’une dysfonction sévère du VG et, de façon
probablement plus fréquente, d’une dysfonction
modérée à moyenne. La plupart des études montrent
une normalisation de la fonction du VG après
réduction ou simple ralentissement de la fonction
cardiaque (FC).
Facteurs prédictifs
de la survenue d’une FA
et remodelage cardiaque
D’après une communication de S. Edery, Paris
S. Edery est allé dans le sens de B. Gersh. La FA est
le reflet d’une atteinte structurelle du myocarde
et de l’oreillette gauche (OG). Ainsi, des facteurs
prédictifs du remodelage myocardique et de l’OG
– et donc prédictifs de la survenue d’une FA – ont
pu être établis à partir d’études épidémiologiques.
Ces facteurs sont cliniques (présence d’une cardio-
pathie, âge, HTA, diabète, consommation d’alcool,
obésité), échocardiographiques (diamètre et surface
de l’OG, fraction de raccourcissement du VG, somme
de l’épaisseur de la paroi postérieure du VG et du
septum interventriculaire, dysfonction diastolique)
et biologiques (taux de BNP).
Le remodelage de l’OG pourrait également être
étudié grâce à de nouvelles techniques comme
la quantification de la fibrose de l’OG par IRM ou
de l’anomalie du strain de l’OG. Plusieurs études
ont suggéré un rôle pronostique de ces nouveaux
marqueurs de remodelage de l’OG et une bonne
corrélation entre l’importance de la fibrose de l’OG
détectée à l’IRM (avec score de CHADS), le risque
de survenue d’un AVC et le risque de récurrence de
la FA après réduction.
Prise en charge
du risque embolique
D’après une communication de B. Gersh, États-Unis
L’orateur a insisté sur la faiblesse des différents scores
de risque embolique : mauvaise performance pour
les patients à faible risque et manque de données
pour les patients à haut risque.
De nouveaux anticoagulants sont en cours d’évalua-
tion dans la FA. Dans l’étude RE-LY, le dabigatran
(anti-IIa oral), comparé à la warfarine, est apparu
supérieur à la dose de 150 mg et n’a pas été infé-
rieur à la dose de 110 mg en termes de réduction
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
1
/
11
100%