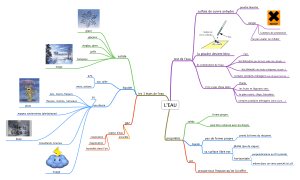
Electrosynthèses sur matériaux divisés

ELECTROSYNTHESE SUR MATERIAUX DIVISES
Christine CACHET-VIVIER, Rachid BARHDADI, Jean-Yves NEDELEC
Equipe Electrochimie et Synthèse Organique, Institut de Chimie des Matériaux Paris Est
UMR 7182 CNRS Université Paris 12 – Val de Marne, 2 rue H. Dunant 94320 Thiais-01 49 78 11 37 – [email protected]
Extraction : CH2Cl2/HCl / Identification des produits : Chromatographie en phase gazeuse couplée Spectrométrie de masse.
(1) Electrode de travail; (2) Electrode de référence (Calomel ou Ag/AgCl, KCl sat.); (3) Electrode auxiliaire
(A)Cavité ( h = 0,3 mm, ∅= 13 mm ) remplie avec poudre de graphite Lonza KS44 (0,15g pressé avec 2.5 Kg/10 min); (B) Cylindre de graphite;
(C) Papier filtre; (D) Bouchon en Teflon®
Suivi de l’électrolyse
Cathode: mélange bromoester/benzaldéhyde + 20 µL MeOH/ TBABF4
+O
O
R1R2
H
0,2 mmol
0,4 mmol
R3
CHO
+
O
O
Br
R1R2poudre de graphite
e-
0,1 M KBr/H2O
0,1 M TBABF4/MeOH O
R3
O
R1R2
OH H
12 3 4
Mettre au point des procédés d’électrosynthèse organique:
Simples, sélectives, efficaces, propres, transposables à l’échelle préparative.
Trouver des alternatives à certaines méthodes chimiques peu efficaces ou peu sélectives.
OBJECTIFS
Réduction des halogénures organiques:
→à des fins synthétiques (Couplage de dérivés halogénés avec divers électrophiles:
Cibles visées : produits ou des intermédiaires de synthèse pour la pharmacie, l’agrochimie ou
la parfumerie.
→en électrodépollution (élimination des PCB, HOV…)
EXPERIENCE DU LABORATOIRE
- Catalyse homogène avec des complexes de métaux de transition (Ni, Fe, Co).
-Analyse des processus par des méthodes électrochimiques.
- Développement de la MicroElectrode à Cavité.
-Nouveaux solvants: Remplacer les solvants moléculaires
→Solvant protiques (eau, alcool)
→Liquides ioniques
-Nouveaux matériaux d’électrode:
Remplacer les électrodes surfaciques par des électrodes volumiques
DEVELOPPEMENTS RECENTS
- (i) un état divisé (poudre, feutre)
→bénéficier de la plus grande interface matériau/substrats
⇒réduire les quantités de solvant ;
-(ii) Nature des matériaux
→Graphite, métaux supportés ou non:
Alternative à une réduction indirecte impliquant des catalyses par des métaux de
transition
Par exemple: l’argent présente une affinité particulière pour les composés organiques
halogénés: surtension plus faible.
→Matériaux modifiés: greffage de complexes de métaux de transition
à la surface de poudre ou de feutres de carbones:
Augmenter l’efficacité du catalyseur et faciliter sa récupération.
NOUVEAUX MATERIAUX D’ELECTRODE:NOUVELLE CELLULE A ELECTRODE A POUDRE:
APPLICATION 1 : REDUCTION DIRECTE DE PhCH2Cl: APPLICATION 2 : REACTION DE REFORMATSKI:
POUDRE: graphite
PHASE ORGANIQUE: Réactifs + solvant
PHASE AQUEUSE:
KBr 0,1 mol.L-1 /
H2O
1
3
2
ABC
D
0 20406080100
0
10
20
30
40
50
60
70
80
90
100
Qexpérimental (%)
% Ag
-3,0 -2,5 -2,0 -1,5 -1,0 -0,5 0,0
-30
-25
-20
-15
-10
-5
0
PhCH2Cl pur
5% DMF + 95% PhCH2Cl
20% DMF + 80% PhCH2Cl
50% DMF + 50% PhCH2Cl
100% DMF
intensité (mA)
Potentiel (V/ECS)
mélange 50%argent / 50% graphite
0 20406080100
0
10
20
30
40
50
60
70
80
90
100 chlorure de benzyle
toluène
dimère
%
% argent
- Conversion jusqu’à 90%
- Excellent rendement faradique
- Meilleur rendement pour 10%
d’argent : Effet combiné de la
grande surface de graphite
(Sgraphite = 9 m2.g-1/Sargent = 0,2 m2.g-1) et
du potentiel de réduction plus
élevé sur argent ⇒matériaux
nanométriques (argent nano sur
graphite).
Electrolyses à potentiel contrôlé -2 V/ECS (20% DMF)
0 20406080100
0
10
20
30
40
50
60
70
80
90
100
110
120
rendement faradique
%
% argent
PhCH2Cl + e-→½PhCH
2-CH2Ph + Cl-
-1,5 -1,4 -1,3 -1,2 -1,1 -1,0 -0,9 -0,8 -0,7 -0,6 -0,5 -0,4 -0,3 -0,2
16
14
12
10
8
6
4
2
0
-2
c = (1)+(2)
a
b = (2*)
Ep(2) = -1.35 V
Ep(2*) = -1.32 V
Ep(1) = -0.98 V
c
a = (1*)
- i / mA
E / V
b
Ep(1*) = -0.91 V
(*) = alone
ConditionaRendement / %
(1): (2) / mmol 1b2b3c4
1 (0.6) : (0.2) 11 10 45 34
2(0.4) : (0.2) 0 8 70 22
3 (0.2) : (0.2) 0 36 53 11
4 (0.2) : (0.4) 0 62 34 4
Entrée
Influence de la teneur en poudre d’argent
Influence de la teneur en solvant
-De 0 à 50% en Ag, Epic augmente:
affinité de l’argent pour PhCH2Cl.
- Pour % Ag > 50: Epic stable mais
plus faible que pour 50%:
Résistance plus grande.
- Si la teneur en DMF
augmente, Epic diminue mais la
charge augmente.
- Pour 50% de DMF, réduction
du solvant.
0204060
0
20
40
60
80
100
120
140
160
180
200
Q (%)
% DMF
Réduction du bromoster
Réduction du benzaldehyde
Electrolyses -0,98 V/Ag/AgCl, potentiel de
réduction du bromoester
Mécanisme:
1) RX + 2e-→R-+ X-
2) Attaque nucléophile du C=O de l’aldéhyde
R1 = R2 = CH3
R3 = H
Influence de la proportion des réactifs
bromoester/benzaldéhyde = 2:1
- Réduction du bromoester efficace (rendement faradique 77%)
- Réaction entre R-et le benzaldéhyde lente (rendement faradique ~30%) ⇒Améliorer l’efficacité du couplage
Volume de la cavité = profondeur x Surface ~265 ±25 µL
Volume de graphite = m/ρ = 67 µL (masse = 150 mg, ρgraphite = 2,25 g.cm-3)
Volume interstitiel = Vcavité -V
graphite ~200 ±25 µL
Sur graphite / argent / mélanges argent-graphite (poudre d’argent commerciale: grains de diamètre 2 à 3,5 µm)
-20 0 20 40 60 80 100 120 140 160 180
0
20
40
60
80
100
reagents and produits / %
charge / C
(3)
(4)
(2)
(1)
Collaboration avec Eric leonel (ESO – ICMPE), Madalena C. C. AREIAS, Marcelo NAVARRO, Lothar W. BIEBER,
Flamarion B. DINIZ (Université de Récife, Brésil)
¾Perspectives:
- Cellule à circulation de fluides à faible débit.
- Utilisation de feutres de carbone modifié ou non suivant les applications
(dépôt de nano-particules, greffage...).
- Application à d’autres réactions.
-3,5 -3,0 -2,5 -2,0 -1,5 -1,0 -0,5 0,0
-20
-15
-10
-5
0
PhCH2Cl pur
100% graphite
50% Ag / 50% graphite
100% argent
intensité (mA)
Potentiel (V/ECS)
CONCLUSION GENERALE et PERSPECTIVES
¾Nouveau procédé simple à mettre en œuvre, sélectif, efficace pour la réduction
des halogénures organiques.
0,1 mL/1mmol
0-20 % DMF + 20-80% RX
2,5 à 5 mL/1mmol
95-98 % DMF + 2-5% RX
vsolvant/nréactif
% volume
~1,3.105cm2/mL*
3.103cm2/mL**
~1 cm2/mLAelectrode/Vsolution
Cellule à poudreCellule classiqueRapport
25 à 50 fois moins de solvant qu’en cellule classique
Pas de sel organique
* Sgraphite = 9 m2.g-1
** Sargent = 0,2 m2.g-1
1
/
1
100%