Chap18 Piles et oxydoréductions

THÈME : AGIR/CONVERTIR L’ÉNERGIE ÉCONOMISER LES RESSOURCES
LES REACTIONS D’OXYDOREDUCTION
I Exemples de réaction d’oxydoréduction
1. Réaction entre le métal fer Fe et les ions métallique cuivre Cu 2+
! Expérience :
Versez dans un tube à essais environ 4 mL d’une solution de sulfate de cuivre, puis plongez dans la solution un
petit morceau de paille de fer.
Faites le schéma de l’expérience et notez l’aspect de la paille de fer et de la solution au bout de quelques minutes.
! Identification des produits formés au cours de la transformation chimique
Rem : Les ions sulfate sont des ions spectateurs.
o Quelle(s) espèce(s) chimique(s) vos observations permettent-elles d’identifier ?
o Afin d’identifier la seconde espèce chimique formée, ajoutez dans le tube quelques gouttes de soude. Concluez.
! Equation équilibrée de la réaction.
! Complétez le tableau suivant :
L’ion cuivre Cu 2+ :
L’atome de fer Fe :
a gagné
1
proton
a gagné
1
proton
a perdu
2
électron
a perdu
2
électron

3
neutron
3
neutron
2. Réaction entre le métal cuivre Cu et les ions métallique argent Ag+
! Expérience :
Versez dans un tube à essais environ 4 mL d’une solution de nitrate d’argent, puis plongez dans la solution un petit
morceau de tournure de cuivre.
Faites le schéma de l’expérience. notez l’aspect du morceau de cuivre et de la solution au bout de quelques
minutes. (agiter si nécessaire.)
! Identification des produits formés au cours de la transformation chimique
Rem : Les ions nitrate sont des ions spectateurs.
o Quelle(s) espèce(s) chimique(s) vos observations permettent-elles d’identifier ?
o Par analogie avec l’expérience précédente, quelle est selon vous la seconde espèce chimique formée? Comment
pourrait-on mettre en évidence ce produit ?
! Equation équilibrée de la réaction.
! Complétez le tableau suivant :
L’atome de cuivre Cu :
L’ion argent Ag+ :
a gagné
1
proton
a gagné
1
proton
a perdu
2
électron
a perdu
2
électron
3
neutron
3
neutron

II Les réactions d’oxydo-réduction.
1. Oxydants et réducteurs : définitions
Sachant que les ions métalliques sont des oydants, et les métaux des réducteurs, complétez les phrases suivantes :
Un oxydant est une espèce chimique
Un réducteur est une espèce chimique
Une réaction d’oxydoréduction est une réaction au cours de laquelle
2. Couples Oxydant / Réducteur.
a- Couple Cu2+ / Cu
! Quelle équation peut-on écrire pour rendre compte de la transformation qu’a subit Cu 2+ dans la première
expérience ?
! Quelle équation peut-on écrire pour rendre compte de la transformation qu’a subit Cu dans la deuxième
expérience ?
! Cu 2+ et Cu constitue un couple oxydo-réducteur noté : Cu 2+(aq) / Cu . Comment peut-on définir un couple
oxydo-réducteur?
Deux entités chimiques constituent un couple oxydant/réducteur s’il est possible de
b- Autres couples
! Ecrivez les demi-équations équations chimiques correspondants aux transformations subies par le fer et
l’argent. Donnez la notation des couples oxydo-réducteurs auxquels appartiennent ces espèces chimiques.

3. Ecriture d’une équation d’oxydoréduction.
Principe: Une réaction d’oxydoréduction a lieu entre l’oxydant d’un couple et le réducteur d’un autre couple.
Tous les électrons cédés par le réducteur sont captés par l’oxydant; aucun n’électron n’apparaît dans
l’équation de la réaction.
Méthode d’écriture:
1. On écrit les deux ½ équations correspondant
aux deux couples mis en jeu.
2. On ’’combine’’ ces deux ½ équations de
manière à égaliser le nombre d’électrons cédés
et gagnés

III Les piles
Cf activité documentaire 1 p 328 et activité expérimentale.
1. Définition
Une pile est un générateur électrochimique qui transforme l’énergie chimique en énergie électrique.
Une pile est constituée de l'assemblage de deux
compartiments:
L’un constitue le pôle + de la pile, l'autre le pôle -.
La plupart du temps chaque compartiment contient
une électrode métallique et un électrolyte (milieux
ionique).
Les compartiments sont liés par un séparateur
permettant le transport des ions (paroi poreuse ou
pont salin).
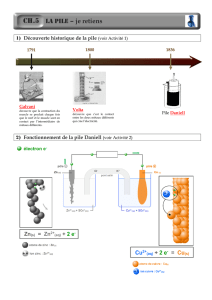
2. Exemple d’une pile cuivre/Fer
Il s’y produit une réaction d’oxydoréduction.
Au pôle négatif de la pile (anode) se produit une oxydation. Des électrons sont libérés :
𝐹𝑒 →𝐹𝑒!!+2𝑒!
Les électrons qui arrivent au pôle positif (cathode) sont captés. Il s’y produit une réduction :
𝐶𝑢!!+2𝑒!→𝐶𝑢
A l’intérieur de la pile, le passage du courant est assuré par des ions. Le pont salin constitue une jonction électrolytique
entre les deux compartiments de la pile.
La réaction est : 𝑭𝒆(𝒔)+𝑪𝒖(𝒂𝒒)
𝟐!→𝑭𝒆(𝒂𝒒)
𝟐!+𝑪𝒖(𝒔)
!
Pont
salin
I
I
Zoom
Zoom
Electrode
de cuivre
Electrode
de fer
Solution
électrolytique de
sulfate de cuivre II
Solution
électrolytique de
sulfate de fer II
 6
6
1
/
6
100%