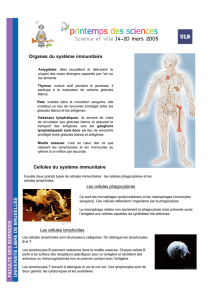
Diapositive 1 - Master Pathologie Humaine

Notions générales sur les
mécanismes de tolérance
immunitaire et de contrôle de la
réponse immune et d’échappement
conduisant aux processus
pathologiques : autoimmuns,
allergiques,….
Dr José Boucraut
jose.boucraut@univ-amu.fr

Définitions et notions générales sur
la tolérance

a. Tolérance et spécificité antigénique
•On relie la tolérance immunologique à la notion de réponse dirigée
contre un antigène ou un déterminant antigénique.
• Elle est donc en ce sens spécifique d’un antigène :
–antigènes du soi
–antigènes du non-soi ou du soi modifié
•Allergènes, antigènes infectieux, antigènes tumoraux,
antigènes de greffe
•On est tolérant vis-à-vis d’un antigène quand l’organisme ne
développe pas de réponse contre cet antigène
•La tolérance est un état de non-réponse (et pas un échappement)
– Soit par absence d’effecteurs
–Soit par anergie de ces effecteurs
–Soit par contrôle de ces effecteurs
•Rôles de populations régulatrices

b . Différence entre tolérance et échappement à la
réponse immune
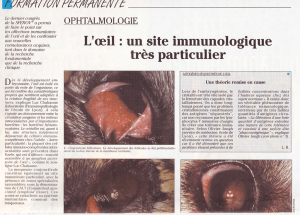
•Sites non accessibles du fait de la présence de barrières
anatomiques :
– Œil, SNC, Placenta
•Expression par les cellules cibles de ligands inducteurs de la mort des
effecteurs, exemples :
–membre de la famille du TNF, ex. FasL, TRAIL qui induisent la mort des LyT
activés
•Libération de cytokines immunosuppressives,
–ex : TGF-béta
• Inhibition de l’expression des molécules du CMH de classe I,
« masquage de l’information »
–Certaines protéines virales codent pour des protéines qui bloquent la transcription,
la biosynthèse ou le transport des molécules du CMH-I
– Les tumeurs sont caractérisées par l’expression de méthyltransférase qui
induisent une inhibition de la transcription des gènes des molécules du CMH-I
–Le syncytiiotrophoblaste n’exprime pas de molécule du CMH-I classiques

c. La tolérance à un antigène n’est pas transmise
mais acquise par une éducation
• Mise en place d’un répertoire de réponse immune
•Sélection positive et survie par engagement minimal du
récepteur
•Sélection négative et mort par engagement maximal du
récepteur
•Délétion clonale, Anergie
•Emigration périphérique de cellules faiblement
autoréactives
•Contrôles de ces populations autoréactives
–Mécanismes de tolérance dits « périphériques »
T B
CMH Ligands endogènes (incluant des Ig)
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
1
/
22
100%