Guide sanitaire

Manuel d’identification
des principales lésions
anatomo-morphologiques
et des principaux parasites
externes des anguilles
Patrick Girard et Pierre Elie
Janvier 2007
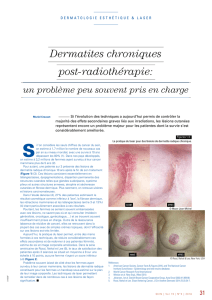
Anguillette stade VII dont les branchies sont
entièrement envahies par des kystes parasitaires (P. Elie)
Etude Cemagref n°110

Manuel d’identification des principales lésions
anatomo-morphologiques et des principaux parasites
externes des anguilles
Par
Patrick GIRARD
*
Docteur Vétérinaire Consultant
en Environnement Aquatique
Pierre ELIE
*
Directeur de Recherche
Cemagref de Bordeaux
Remerciements :
Ce travail a été réalisé grâce au soutien financier du programme européen
« Interreg » dans le cadre du programme Indicang.
Avec tous nos remerciements aux Collègues et Organismes suivants qui ont
mis gracieusement à notre disposition les clichés photographiques qui
illustrent ce manuel :
P. BOURY, D. BUCKE, CEMAGREF, G. CSABA, EAFP, G. FAZIO, S. FEIST,
GDSAA, G. GIORGETTI, J.P. GISLARD, INRA, L. ITBISSEM
,
N. KECK, T.
POPPE, H.J. SCHLOTFELDT, N. SUSPERREGUI.
Ainsi qu’à madame Patricia MARTIN qui a mis en forme ce document de
travail.
Référence de document :
Girard P. et Elie P. 2007 : Manuel d’identification des principales lésions
anatomo-morphologiques et des principaux parasites externes des anguilles
(81 pages) - CEMAGREF / Association « Santé Poissons Sauvages ». Etude
Cemagref n°110 - Groupement de Bordeaux
* Association « Santé Poissons Sauvages »

SOMMAIRE
I Présentation du manuel
5
II Grille de description des anomalies et parasites
Comment utiliser la grille de description 8
Grille de description des anomalies et parasites 10
III Les principales lésions anatomo-pathologiques rencontrées
Absence d’organes (AO) 12
Altération de la couleur (AC) 14
Anus rouge ou saillant (US) 15
Bulle de gaz (BG) 16
Déformation, difformité et malformation (AD) 18
Erosion (ER) 20
Etat pathologique multiforme (ZO) 22
Hémorragie (HE) 23
Hypersécrétion de mucus (SM) 25
Lésions branchiales (LB)
Nécrose, érosion branchiale (NE) 26
Kystes branchiaux (KY) 27
Hyperplasie et congestion branchiale (CH) 28
Lésions oculaires (LB)
Hémorragie oculaire (HE) 29
Gros yeux ou Exophtalmie (EX) 30
Ulcère cornéen (UL) 31
Perte d’œil ou énucléation (AO) 32
Parasitisme oculaire (PA) 33
Opacité (CO) 34
Maigreur (AM) 35
Masse et « grosseur » (AG) 36
Nécrose (NE) 38
Ulcère hémorragique (UH) 39

IV Les principaux parasites externes
Crustacés (PC) 41
Hirudinés ou sangsues (Piscicola geometra) (PH) 45
Mycose ou « mousse » (PM) 47
Point blanc (PB) 49
V Quelques conseils pour les examens des poissons
et la description des anomalies
52
VI Conseils pour le conditionnement des échantillons à analyser
54
VII Modèles de fiches de saisie des informations
Comment renseigner les fiches de saisie « pathologie » 56
Les fiches de saisies
Fiche de renseignements généraux 59
Fiche de saisie « Pathologie » individuelle 60
Fiche de saisie « Pathologie » générale 61
Exemple de saisie 63
VIII Conservation et conditionnement des échantillons
66
IX Evaluation de l’état de fraîcheur initiale avant analyse
69
X Expédition des échantillons
71
XI Glossaire - sigles - abréviations
73
XII Adresses utiles
81

I. PRESENTATION DU MANUEL
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
 53
53
 54
54
 55
55
 56
56
 57
57
 58
58
 59
59
 60
60
 61
61
 62
62
 63
63
 64
64
 65
65
 66
66
 67
67
 68
68
 69
69
 70
70
 71
71
 72
72
 73
73
 74
74
 75
75
 76
76
 77
77
 78
78
 79
79
 80
80
 81
81
 82
82
 83
83
1
/
83
100%