3°EtudeATB 2017

18/02/17
1
Méthodes d’étude de
l’activité des antibiotiques
Pr Hélène MARCHANDIN
DFGSP3 – 2016/2017
Introduction
Etude
in vitro
de l’activité des ATB
sur bactéries pathogènes
=
Etape nécessaire au choix d’une
antibiothérapie adaptée
• Sensibilité (S) et résistance (R) naturelles des
espèces bactériennes à certains antibiotiques (ATB)
• Nombreux mécanismes de R acquise aux antibiotiques
2!

18/02/17
2
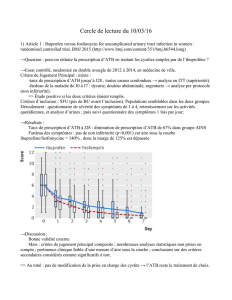
Interactions bactérie-antibiotique
CMB
CMI
Nombre de bactéries/ml
Bactériostase!
Ralentissement !
de la croissance!
Bactéricidie
Effet létal de!
l’antibiotique!
3!
En milieu solide
Dilution en milieu gélosé (réf)
Diffusion en milieu gélosé*
- Disques
- Bandelettes
Etude de la bactériostase
= détermination de la CMI
(concentration minimale inhibitrice)
plus faible concentration d'antibiotique capable
d'inhiber toute croissance visible de la bactérie
in vitro
En milieu liquide
Dilution en milieu liquide
- Méthodes manuelles (réf)
- Méthodes automatisées*
(réf) : méthodes de référence * méthodes utilisées en routine 4!

18/02/17
3
Détermination CMI / DILUTION en milieu liquide
Méthodes manuelles
Gamme de
concentration d’ATB
de raison 2
(sans ATB)!
Inoculum bactérien
standardisé
5!
Croissance!
bactérienne!
Exemple
+
+ +
+ + - - - - - - - -
6!

18/02/17
4
Microméthodes
- en microplaques T!Gamme d’ATB(s)
Exemple
Souche d
’E. coli
et amoxicilline
T 2 4 8 16 32 64 µg/ml!
CMI 64µg/ml
Etude d’un ou plusieurs :
- ATB
- isolats bactériens
par plaque
7!
- méthodes automatisées
• cartes / micro-puits : ≠ antibiotiques
à ≠ concentrations
• incubation, lecture de la croissance bactérienne
et interprétation automatisées
méthodes plus rapides : environ 6-7h
8!

18/02/17
5
Détermination CMI / DILUTION en milieu gélosé
Gamme de
concentration
d’ATB
+
inoculum
bactérien
standardisé
(spot)
T 0,5 1 2 µg/ml
Souches 1 et 4 : CMI = > 2 µg/ml
Souche 2 : CMI = 2 µg/ml ; souche 3 : CMI = 1 µg/ml
9!
Détermination CMI / DIFFUSION en milieu gélosé
Méthode des disques
Lecture d’un diamètre d’inhibition (en mm) 10!
Inoculum standardisé
0,5 McFarland ≈ 108 UFC/ml
Milieu de Mueller-Hinton
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
1
/
20
100%