Exercice I Aspirine et prévention cardiovasculaire (8,5 points)

Correction du DST n°4
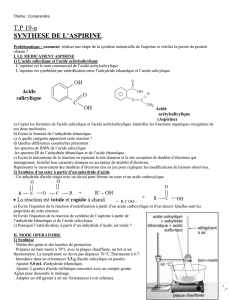
1.1. Obtention de l’aspirine :
1.1.1. Quantité de matière d’anhydride éthanoïque introduite :
On a introduit un volume V = 14,0 mL d’anhydride éthanoïque.
D'après la relation :
m
= V
µ
, on a: m = .V
<=>
m
n = M
donc
.V
n = M
(avec µ convertie en g.L-1 et V en L)
33
1,082 10 ×14,0 10
n = 102
= 0,149 mol d’anhydride éthanoïque
Quantité de matière d’acide salicylique introduite :
On a introduit une masse m’ = 10,0 g d’acide salicylique.
Soit :
m'
n' = M'
<=>
10,0
n' = 138
= 7,25×10-2 mol d’acide salicylique
Déterminons le réactif limitant : 3 méthodes au choix
Méthode 1
:
à privilégier quand les coefficients stœchiométriques sont égaux à 1
n’ < n et comme une mole d’anhydride éthanoïque réagit avec une mole d’acide salicylique, le réactif limitant est
alors l’acide salicylique. L’anhydride éthanoïque est introduit en excès.
Méthode 2
:
On peut aussi utiliser un tableau d’avancement.
équation chimique
acide salicylique + anhydride aspirine + …
éthanoïque
État du
système
Avancement
(mol)
Quantités de matière (mol)
État initial
x = 0
n’
n
0
En cours de
transformation
x
n’ – x
n – x
x
État final
x = xmax
n’ – xmax
n – xmax
xmax
Si l’acide salicylique est limitant, alors n’ – xmax = 0, donc n’ = xmax.
Si l’anhydride éthanoïque est limitant alors n – xmax = 0 donc n = xmax.
Le réactif limitant est celui qui conduit à la valeur de l’avancement maximal la plus faible ; n’ < n donc il s’agit de
l’acide salicylique et l’anhydride éthanoïque est en excès.
Méthode 3 : Méthode des inéquations :
Les quantités de matière sont des grandeurs positives ou nulles
n(acide) ≥0 et n(anhydride) ≥0
<=> n’ – x ≥0 et n – x ≥ 0
<=> x ≤ n’ et x ≤ n soit : x ≤ 7,25×10-2 mol et x ≤ 0,149 mol
Ces deux inéquations sont simultanément vérifiées lorsque : x ≤ 7,25×10-2 mol
Par conséquent : xmax = 7,25×10-2 mol , l'acide salycilique est le réactif limitant et l'anhydride éthanoïque est
bien en excès.
1.1.2. D’après l’équation de la réaction, une mole d’acide salicylique fournit une mole d’aspirine, or on dispose de
n’ mole d’acide salicylique, il se formera n’ mole d’aspirine.
m(aspirine) = n’.M(aspirine)
<=> m(aspirine) = 7,25×10-2180 = 13,0 g
Autre méthode : d’après le tableau d’avancement n(aspirine) = xmax = n’

1.2 Suivi par chromatographie :
1.2.1. Sur une plaque pour CCM il faut déposer différents prélèvements afin de s’assurer de la formation de
l’aspirine.
On trace sur la plaque, un trait à 1 cm du bord inférieur afin d’y effectuer les dépôts.
On dépose deux témoins à l’aide d’un capillaire : l’acide salicylique pur et l’aspirine du commerce.
On effectue ensuite les cinq dépôts correspondants aux prélèvements effectués dans le mélange réactionnel
aux différents instants.
On dépose la plaque pour CCM dans la cuve à chromatographie avec l’éluant. On attend que le front du solvant
monte suffisamment.
On révèle ensuite sous UV ou dans le permanganate de potassium.
1.2.2. Si le système réactionnel est dans son état final, tout l’acide salicylique doit être consommé. Sur le
chromatogramme, il n’y aura plus de tâche correspondant à celle de l’acide salicylique, par contre on aura formé
de l’aspirine. On doit obtenir une tache à la même hauteur que celle obtenue avec l’aspirine du commerce.
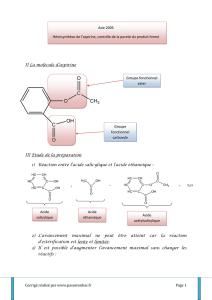
2. Analyse spectrale des espèces chimiques intervenant dans la synthèse de l’aspirine
2.1. Spectre RMN de la molécule d’aspirine.
2.1.1.
Groupe ester
Groupe carboxyle
2.1.2. Carbone « a »
Le carbone voisin du carbone « a » ne
possède pas d’atomes d’hydrogène,
donc les atomes d’hydrogène liés au carbone « a »
correspondent à un singulet.
Carbone « b »
Le carbone « b » a deux carbone voisins, l’un porteur d’un atome
d’hydrogène, l’autre n’en portant pas donc l’hydrogène du carbone « b » correspond à un doublet.
2.2. Spectre IR de la molécule d’acide éthanoïque.
2.2.1.
Il s’agit d’un ester.
Acide éthanoïque méthanoate de méthyle
OH
O
C
O
C
CH3
O
CH3
C
O
OH
CH
O
O
CH3
Carbone « a »
Carbone « b »
OH
O
C
O
C
C
CH3
CH3
O
O
O
OH

2.2.2.
Le spectre IR1 correspond à celui de l’acide éthanoïque et le spectre IR2 à celui du méthanoate de méthyle.
3. Dosage d’un sachet d’aspirine
3.1. HA(aq) + HO-(aq) A(aq) + H2O(
l
)
3.2. À l’équivalence d’un titrage, les réactifs sont introduits dans les proportions stœchiométriques :
Ainsi : n(HA)i = n(HO)versée
<=> n(HA)i = cB.VE dans dans VA = 100,0 mL de solution
Soit n(HA) la quantité d’aspirine présente dans le sachet donc dans 500 mL de solution,
ainsi : n(HA) = 5. n(HA)i
On en déduit la masse correspondante : mexp = n(HA).Maspirine
<=>mexp = 5. cB.VE.Maspirine
<=>mexp = 5 × 1,00102 × 10,7×103 180 = 9,63×10-2 g = 96,3 mg
3.3.
222
exp EB
exp E B
Δm ΔV Δc
= +
m V c
<=>
22
exp EB
exp E B
Δm ΔV Δc
= +
m V c
<=>
2
2-2
exp -2
exp
Δm 0,1 0,02×10
= +
m 10,7 1,00×10
= 210-2 = 2 %
<=> Δmexp = 2102 9,63102= 2103 g = 2 mg
Encadrement : mexp Δmexp < mexp < mexp + Δmexp
94 mg < mexp < 98 mg ou mexp = 96 ± 2 mg
3.4. L’encadrement obtenu ne comprend pas la valeur de 100 mg mentionnée sur le sachet d’aspirine.
L’écart observé peut être dû :
- l’élève aurait dû rincer le sachet avec de l’eau distillée afin d’être certain de récupérer toute l’aspirine
solide ;
Bande à 2500 – 3200 cm-1
Caractéristique de la liaison OH
de l’acide carboxylique
Bande à 1740 – 1800 cm-1
Caractéristique de la liaison C = O
de l’acide carboxylique
Bande à 1730 – 1750 cm-1
Caractéristique de la liaison
C =0 de l’ester

- à la non dissolution totale de l’aspirine dans la solution ;
- à une mauvaise lecture du volume de 500,0 mL sur la fiole jaugée ;
- à une mauvaise détermination du volume équivalent VE (changement de coloration difficile à repérer,
mauvaise lecture sur la burette) ;
- erreur dans le prélèvement du volume VA à doser.
4. Autre forme de l’aspirine, moins agressive pour l’estomac
4.1. Établissons le diagramme de prédominance de l’aspirine :
Dans l’estomac, à pH = 2, l’aspirine prédomine.
4.2.1. Formule semi-développée de l’ion acétylsalicylate :
4.2.2. La catalgine est soluble dans l’eau car elle ne contient pas d’acide acétylsalicylique (aspirine) mais des
ions acétylsalicylate.
4.2.3. A(aq) + H3O+(aq) HA(s) + H2O(l)
Ion acétylsalicylate Aspirine
EXERCICE I : Partie B : SUIVI D'UNE TRANSFORMATION CHIMIQUE (2,5 points)
Étude de la transformation chimique
1. Soient les couples et les demi-équations correspondantes
Couple H+(aq) / H2(g) 2H+(aq) + 2 e–H2(g) (1)
Couple Mg2+(aq) / Mg(s) Mg2+(aq) + 2 e– Mg(s) (2)
2. Déterminons les quantités de matière initiale des réactifs :
n0(Mg) =
Mg
m
M
<=> n0(Mg) =
2
0 12 12 10
24 24
,
= 0,5010–2 = 5,010–3 mol
Et n0(H+) = C V
<=> n0(H+) = 0,50 4010–3 = 2010-3 mol = 2,010–2 mol
Dressons un tableau d'avancement :
Avancement
en mol
Mg (s) + 2 H+ (aq) Mg2+ (aq) + H2 (g)
État initial
x
= 0
5,010–3
2,010–2
0
0
En cours de
transformation
x
5,010–3 – x
2,010
–2 – 2 x
x
x
État final
x = xmax
5,010–3 – xmax
2,010
–2 – 2 xmax
xmax
xmax
Les quantités de matière sont des grandeurs positives ou nulles
n(Mg) ≥0 et n(H+) ≥0
<=> n(Mg)i – x ≥0 et n(H+)i – 2x ≥ 0
<=> x ≤ n(Mg)i et x ≤ n(H+)i/2 soit : x ≤ 5,010–3 mol et x
2
2 0 10
2
,
= 1,010–2 mol
Ces deux inéquations sont simultanément vérifiées lorsque : x ≤ 5,010–3 mol
Par conséquent : xmax = 5,010–3 mol
O
A-
pr
éd
o
mi
ne
Io
n
ac
éty
lsa
lic
yla
te
C
C
O
C
CH3
O
O
C
C
HC
HC
HC
HC
pH
pKA = 3,5
HA prédomine
Aspirine

Graphiquement, dans l'état final : Vf(H2) = 1,2102 mL = 1,210210–3 L = 1,210–1 L
Or la quantité finale de dihydrogène est nf(H2) = xf =
f2
m
V (H )
V
donc xf =
12
12 10 12 10
24 24
,
= 0,5010–2 = 5,010–3 mol
4. On a xf = xmax donc la transformation est totale.
5. Le temps de demi-réaction t1/2 est la durée pour laquelle l'avancement atteint la moitié de sa valeur finale :
x(t1/2) =
f
x
2
.
Ici, l'avancement est proportionnel au volume de dihydrogène , x =
2
m
V(H )
V
,
donc on peut écrire : V(H2)(t1/2) =
f2
V (H )
2
Méthode: on trace la droite horizontale
2
V(H )
2
= 60 mL . Cette droite coupe la courbe V(H2) = f(t) en un point
d'abscisse égale à t1/2. Graphiquement on détermine : t1/2 = 1,2102 s
6. La température est un facteur cinétique. On peut placer le ballon, contenant les réactifs, dans un bain d'eau
glacée. L'état final sera atteint moins rapidement ce qui augmentera le temps de demi-réaction t1/2.
Remarque : la concentration en réactif est aussi un facteur cinétique. On peut augmenter le temps de demi-réaction
t1/2 en diminuant la concentration initiale de la solution d'acide chlorhydrique mais en conservant le métal
magnésium comme réactif limitant afin d'avoir le même état final.
EXERCICE II : DIFFRACTION DE LA LUMIERE A TRAVERS UN TAMIS (4 points)
1.1 Une onde correspond à la propagation d’une perturbation sans transport de matière mais avec transport
d’énergie.
1.2 Une onde peut être transversale. C’est le cas d’une vague qui se propage à la surface d’un liquide.
Une onde peut être longitudinale. C’est le cas du son.
 6
6
 7
7
 8
8
1
/
8
100%