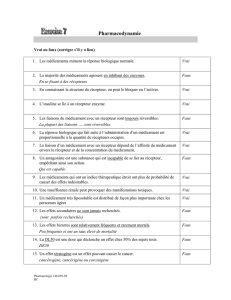
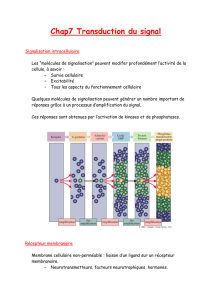
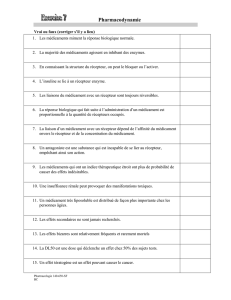
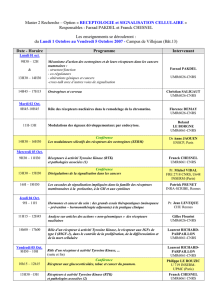
Mécanismes d`action des médicaments

François Etcheverrigaray,
Interne pharmacie hospitalière, PUI Hôpital St Jacques, Nantes.
1

Sommaire :
I) Les effets d'un médicament
A. Effets non spécifiques
B. Effets spécifiques
II) Le mécanisme d'action des médicaments
A. Action indépendante de la notion de récepteur
B. Dépendant de la notion de récepteur
1. Définition du récepteur
2. Les divers types de récepteurs
C. L'interaction médicament-récepteur
1. Saturabilité et affinité
2. Spécificité
3. Sélectivité
III) Conséquences et facteurs influant sur la pharmacodynamie d’un principe actif.
2

Généralités :
Médicament (drug, medicine, medication)
“ Toute substance ou composition, présentée comme possédant des propriétés
curatives ou préventives à l’égard des maladies humaines ou animales, ainsi
que tout produit administré à l’homme ou à l’animal en vue d’établir un
diagnostic médical, de restaurer, corriger ou modifier leurs fonctions
organiques ” (Article L.511 du Code de la Santé Publique).
Mécanismes d’action
Actions non spécifiques
Actions spécifiques
3

Les effets d'un médicament
• Actions non-spécifiques : propriétés physico-chimiques
–Pansements gastriques, intestinaux SMECTA®, alginates…
–Modificateurs de l’équilibre acido-basique (soluté NaCl…)
–Modificateurs de l’équilibre osmotique (mannitol)
4

Les effets d'un médicament
•Actions spécifiques : interactions avec des macromolécules
–Lipides :
•Amphotéricine B : agent surfactant à propriété antifongique
interagissant avec les lipides de la paroi fongique (ergostérol)
–Acides nucléiques :
•Agents anticancéreux : CisPt (ENDOXAN), agents
intercalants…
–Protéines : récepteurs, canaux ioniques, enzymes, transporteurs
5
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
1
/
44
100%