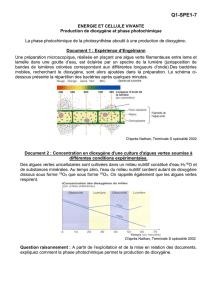
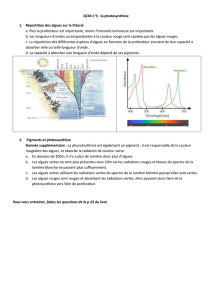
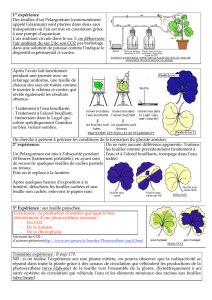
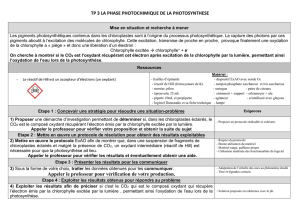
1 6CO2 + 12H2O → C6H12O6 + 6O2 + 6H2O

Diversité et complémentarité des métabolismes – Tale S – Spé SVT B.BOCK – Lycée Rotrou – Dreux (28)
1
TP 6 : La photosynthèse un processus en 2 étapes - la phase photochimique de la photosynthèse
Objectifs méthodologiques :
- réaliser une expérience en suivant un protocole
- observer une électronographie
- faire un dessin légendé
- calculer une taille et représenter une échelle
- mesurez un spectre d’absorption
La mesure de l’intensité photosynthétique peut être réalisée soit en mesurant la quantité de carbone fixé par unité de surface
de feuille et par unité de temps, ou bien plus simplement en mesurant la quantité de dioxygène produit par masse de végétal
et par unité de temps. Certains facteurs modifie l’intensité photosynthétique : l’intensité lumineuse, la qualité (longueurs
d’onde) de la lumière reçue.
Une expérience historique remarquable a permis de mettre en évidence ces variations de l’intensité photosynthétique :
d'après 2002. Terminale S spécialité. Nathan.
Rappel : On peut globalement résumer la création de matière organique par la réaction suivante :
6CO2 + 12H2O C6H12O6 + 6O2 + 6H2O
Problématique : Comment l’absorption de l’énergie lumineuse par la chlorophylle peut-elle aboutir à la production de
matière organique ?
Activité 1 : Mise en évidence des 2 phases de la photosynthèse
Expérience
Milieu de culture contenant
Résultats
Dioxyde de carbone avec du
carbone 14 radioactif
Glucose radioactif
Dioxyde de carbone avec de
l’oxygène 18
Glucose lourd
On cultive des chlorelles, algues
vertes unicellulaires, dans des
milieux différents. Au bout de
quelques heures, on recherche
quels sont les éléments
chimiques devenus radioactifs ou
lourds selon l’isotope incorporé.
Eau avec de l’oxygène 18
Dioxygène lourd
Interprétez ces expériences. Caractérisez les deux processus mis en évidence (réduction, oxydation, carboxylation ou
fixation de CO2, photolyse de l’eau).

Diversité et complémentarité des métabolismes – Tale S – Spé SVT B.BOCK – Lycée Rotrou – Dreux (28)
2
Activité 2 : La phase photochimique de la photosynthèse : conversion de l’énergie lumineuse en énergie
chimique.
On se propose de mesurer l’activité photosynthétique par EXAO (par mesure de la concentration en O
2 avec une sonde à
oxygène) d’une solution de chloroplastes isolés dans trois conditions différentes (réaction de Hill) pendant 10 minutes
Avant de lancez l’expérimentation, précisez les résultats que vous pourriez d’après vous attendre.
Temps
Conditions
t = 0 min
Obscurité
t = 1 min
Lumière
t = 3 min
Lumière + réactif de Hill (0,5 mL)
t = 5 min
Lumière + réactif de Hill (0,4 mL)
t = 6 min
Obscurité
t = 8 min
Réactif de Hill (0,3 mL)
PROTOCOLE EXPERIMENTAL de l’extraction des chloroplastes
1. Peser 10 g de limbes feuilles propres et fraîches d’épinard puis découper les limbes en morceaux dans un mortier
préalablement placé au réfrigérateur et maintenu dans la glace (on évite ainsi une dégradation des enzymes nécessaires aux
réactions). Remarque : Lors du broyage, les thylakoïdes restent intacts mais les constituants du stroma se trouvent dilués
dans le milieu d'extraction et ne peuvent plus intervenir dans les réactions.
2. Ajouter 2,5 mL de solution tampon A et broyer pendant au moins 2 minutes.
3. Ajouter 20 ml de solution tampon B et broyer pendant 1 minute.
4. Filtrer le broyat obtenu sur gaze et coton hydrophile afin de recueillir une quantité suffisante de filtrat (presser si
nécessaire).
5. Contrôler au microscope optique la présence de chloroplastes libres et l'absence de cellules foliaires intactes
Qu’est ce que le réactif de Hill :
Il s’agit d'une solution de potassium hexacyanoferrate de concentration 0,2 M (64.5 g/L). Ce réactif à la propriété d’accepter
très facilement un électron suivant l’équation suivante :
Mesurez le dégagement d’O2 grâce au montage proposé dans les conditions demandées. Légendez, titrez et imprimez votre
courbe. Décrivez et interprétez les résultats obtenus à l’aide du livre page 200.
Bilan :
Résumez ce qui ce passe pendant la phase photochimique de la photosynthèse.
Mots clés : oxydoréduction, oxydation, réduction, photolyse
Travail à la maison : interprétez ce document issu d’un sujet de bac.
Concentration en dioxygène d'une culture d'algues vertes soumise à différentes conditions expérimentales
d'après 2002. Terminale S spécialité. Nathan.
Des algues vertes unicellulaires sont cultivées dans un milieu
nutritif constitué d'eau H218O et de substances minérales. Au
temps zéro, l'eau du milieu nutritif contient autant de
dioxygène dissous sous forme 18O2 que sous forme 16O2.
On rappelle que les algues vertes respirent.
16O2
18O2
1
/
2
100%