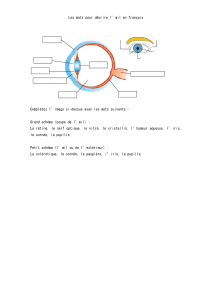
Dysgénésies du segment antérieur et greffes de cornée chez l`enfant

Dysgénésies du segment antérieur
et greffes de cornée chez l’enfant
Réunion d’automne de l’AFSOP
10 et 11 octobre 2014
Dr Emmanuel BUI QUOC, MD PhD
Hôpital Universitaire Robert Debré, Paris

Classifications…
• Pathologies multiples
• Définitions phénotypiques
• Définitions génotypiques
• Glaucome congénital : Diagnostic
différentiel en cas de glaucome congénital
primitif AR CYP1B1…/ Diagnostic associé
dans le cadre du glaucome congénital
secondaire dysgénésique AD PAX 6,
PITX2, FOXC...

Développement normal et
pathologique de l’œil
• Développement du SNC à partir de
l’ectoblaste au 18e jour = plaque neurale
• Invagination au 20e jour : gouttière
neurale puis tube neural
• 2 vésicules optiques
• « Neurocristopathies »
• Migration/Différenciation
• Développement du segment antérieur de
l’œil/ de l’angle très précoce…
Problématique d’un éventuel diagnostic
prénatal sur des critères anatomiques…
alors que la patiente ne connaît pas
forcément encore sa grossesse et que
l’échographie n’a pas une résolution
suffisante
Martine Santallier. Anatomie Ed A&J Péchereau
Barishak YR. Embryology of the Eye and Its Adnexa.
2nd, revised edition KARGER 2001.

• « Les malformations du segment antérieur de
l’œil sont la conséquences d’anomalies du
développement et de la maturation, les différents
phénotypes dépendant du moment où ces
perturbations surviennent dans l’embryogénèse
et le développement fœtal ; bien entendu la
génétique et les caractérisations génotypiques
récentes permettent de mieux comprendre les
processus pathologiques et de repenser la
nosologie des dysgénésies du segment
antérieur »
Glaucomes congénitaux, E Bui Quoc & E Costantini, EMC OPH 2011

• Travaux princeps d’excision graduée des
cellules de la crête neurale céphalique chez
l’embryon de poulet
• Classification des anomalies malformatives du
segment antérieur
– Anomalies de formation,
– Anomalies de migration
– Anomalies de prolifération
– Anomalies de différenciation
des cellules dérivés des crêtes neurales.
Johnston MC, Noden DM, Hazelton RD, Coulombre JL, Coulombre AJ. Origins of avian ocular and periocular tissues. Exp Eye Res.
1979;29:27-43.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
1
/
47
100%