Diagnostic biologique

La thyroïde
(4e année de Pharma 2011-2012)
Les maladies thyroïdiennes(MT) sont les maladies endocrines les +
fréquentes.
Le diagnostic biologique est devenu aisé depuis avènement méthodes
immunométriques et leur automatisation.
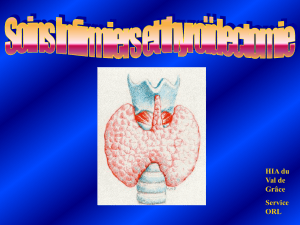
1- Structure de la thyroïde + hormonogenèse:
Glande endocrine du cou (20- 30gr), constituée 2 lobes reliées par 1
isthme. Elle est Constituée de follicules formés d’1 seule couche de
cellules épithéliales. La partie centrale est remplie par la substance
colloïde.
La fonction de la thyroïde est double:
Capter l’iode, fixer en iodotyrosine et HT dans la thyroglobuline (tg)
Secréter HT après protéolyse de la thyroglobuline.
2-Synthèse des HT:
• Besoins en iode: 100 à 200 gr/j (sel iodé, produits de la mer)
• I- capté par un transporteur spécifique situé dans les MBL des
thyrocytes: Symporteur Iodure /Na (NIS)
TYROCYTE T3
20% T4 100%
CELLULE C
CALCITONINE

• La biosynthèse fait intervenir 2 protéines :
*thyroglobuline (protéine volumineuse, riche en tyrosines) dans
colloïde, synthétisée par thyrocytes.
* thyroperoxydase(TPO) enzyme de la membrane apicale des
thyrocytes assure l’iodation et le couplage des iodotyrosines.
Réaction: TPO+ H2O2 +I- + Tg iodation : MIT - Tg et DIT-Tg
Couplage des MIT + DIT HT MIT +DIT= T3; DIT+DIT=T4;
DIT+MIT= rT3
*Les antithyroïdiens de synthèse inhibent iodation et couplage.
• Sécrétion des H :
HT liées à la Tg pénètrent dans les thyrocytes par endocytose après
protéolyse des Tg les HT sont libérées dans le sang (T4100%, T3 20%)
Un petit pourcentage des Tg passe dans le sang.
L’endocytose et la protéolyse sont inhibées par L i et I 2 à forte dose
• Conversion périphérique de T4 enT3
Par les 5’desiodases (type 1:tissu périphérique et type2: SNC,
hypophyse et thyroïde) inhibées par cordarone.
La T3, forme 8 à 10 fois + active, fixe le récepteur, la T4 est une «
forme de réserve »

Régulation de l’hormono-synthèse
Au niveau de la glande
• La Biosynthèses des H T est stimulée par TSH. Ces hormones exercent à
leur tour un feed back (-) sur l’HP et l’ HT.
• La TRH contrôle TSH (TRH est sécrétion par pulse, durant la nuit),
* Les corticoïdes ont une action secondaire sur la thyroïde (la
TSH↑ s’il y a insuffisance surrénalienne et ↓ s’il ya
hypercorticisme)
*L’excès d’I2 inhibe les HT, c’est l’effet Wolff Chaikoff par contre des
doses modérées stimulent la synthèse de la T3 au dépend de la T4
*L’HCG stimule la synthèse des HT (analogie structurale TSH/HCG)
Au niveau périphérique
Par les 5’ desiodases : la T 4 est desiodée en T3. la T3 est davantage le
reflet du MB cellulaire périphérique alors que la T4 celui de la
synthèse thyroïdienne.
* Syndrome T3 basse inhibition ou déficit en desiodases.
TSH et HT dans le sang
• TSH a un rythme circadien minime.

• Les HT circulent liées à des protéines de transport (T3 liée 95%, T4 liée
99,9%) : TBG, TBPA (thyroxin binding prealbumin), albumine.
• L’augmentation des taux des protéines de transport augmentent les
taux de T 4 et T3 totales sans modifier les taux des formes libres : T3L et
T4L.
Catabolisme des HT:
Se fait par desiodation, désamination puis conjugaison hépatique.
Effets biologiques des hormones thyroïdiennes :
Effet stimulateur sur l’ensemble du MB intermédiaire:
↑ Absorption et dégradation du glucose
↑Mobilisation des lipides
↑Production de chaleur
↑Consommation d’O2
Dégradation des protéines à forte dose
↑Croissance et fonctionnement de tous les tissus. Assure vivacité
du cerveau et une grande motilité du tube digestif.
Exploration biologique de la thyroïde
1- TSH
Dosée par méthodes ultrasensibles de 3e et 4e génération:
immunométrie type sandwich anticorps monoclonaux anti sous
unitéβ,
Seuil de sensibilité <0,01mU/L
Permettant le D c des hyperthyroïdies primaires.
Le résultat est exprimé en m U / L de plasma intervalle de référence
varie en fonction de la méthode.
(0,2 – 5 m U /L à titre indicatif)
Enfant: 1e j < 70
2e – 3e j < 30
3e -7e j >10
> 7e j >0,2- 5

Le Dosage n’est affecté ni par le sexe, ni par le caractère pulsatile
ou les variations nycthémérales
« Test de première intention! » :
Paramètre le + discriminant de dépistage d’une dysthyroïdie
Périphérique
Diagnostic des hyper Thyroidie et des hypo Thyroidie 1aires
= hyperthyroïdie = hypothyroïdie
2- Dosage des H T libres :
délicat en raison des faibles concentrations de la fraction libre:
• Dosage immunométrique par compétition:
T4L ou T3L extraite par1 Ac un fixe sur un support solide, puis +de
T 3*ou T4*; T4L ou T3L à doser est inversement proportionnelle à
l’intensité du marquage
(V.N≈ 10- 20pmol/l)
« Dosage de T4l ou FT4 = « Test de 2e intention »:
1. définit la profondeur de l’atteinte fonctionnelle périphérique:
– T4L N (+ TSH perturbée ou )= dysthyroïdie fruste
– T4L + TSH = hyperthyroïdie patente
T4L +TSH = hypothyroïdie patente
2. oriente vers une dysthyroïdie atypique
– TSH N ou basse + T4l basse:
Hypothyroïdie centrale = insuffisance thyréotrope ?
– TSH élevée + T4l élevée:
adénome thyréotrope ? … À confirmer !
résistance aux HT ?… À confirmer
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
1
/
22
100%