formules si -l

SNC2DF - Mots-clés
Définitions, diagrammes, exemples, concepts reliés
« concept map »
Acide
Acidité
Alcalinité
Amer
Anion
Atome
Base
Binaire
Catalyseur
Cation
Changement chimique
Changement physique
Charge
Coéfficient
Combustion
Composé
Composé binaires ioniques
Composé d'ions polyatomiques
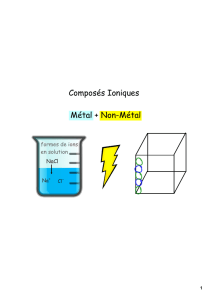
Composé ionique
Composé moléculaire
Concentration
Couches/orbites
Dé = 2- Di = 2-Bi = 2
Déca = 10
Décomposition
Déplacement double
Déplacement simple
diagramme Bohr-Rutherford
diagramme Lewis
Echelle pH
Électrolyte
Électron
Electrons a valence
Élément
Energie
Équation balancée
Equation chimique
Équation nominative
Equation squelette
Famille
Formule chimique
Groupe
Hepta = 7
Hexa = 6
Hydrocarbure= H+C
Ion hydroxyde (OH-)
Ion polyatomique
Ions
Ions polyatomiques
Isotopes
Liaison covalente
Liaison ionique
Loi de la conservation de la
masse
métal
Métaloide
Molécules
Mono = 1
Neutralisation
Neutre
Neutron
Nitrure (exception)
Nomenclature
Nona = 9
Non-métaux
Noyau
Numéro Atomique
Numéro de masse atomique
Octa = 8
Orbite
Oxyde (exception)
papier pH
Papier Tournesol
Penta = 5
Période
pH
Phosphure (exception)
Polyatomique
Potentiel d'hydrogène(pH)
Produit
propriété chimique
propriété physique
proton
réactifs
Réaction chimique
solution
substance pure
Sulfure (exception)
Symbole chimique
Synthese
Tableau périodique (période,
familles)
taux de réaction (et les facteurs)
température
Tétra = 4
Tri = 3
-ure (suffixe)
Valence
Tu devrais savoir :
- au moins une méthode pour
balancer les équations
chimiques
- comment vérifier si une
substance est acide ou base
- comment nommer les
composés si on te donne la
formule
- comment écrire les formules
d’un composé si on te donne
le nom
-
1
/
1
100%