Application de Immunothérapie au Cancer de l`Ovaire

!""#$%&'$()*+,*-../)('012&"$,*
&/*3&)%,2*+,*#456&$2,
72*8$)%,)'*9!85:;
<0$=&/#'*+,*#&*>('',*?(/@,A*7&'2$%B*9,@,.=2,A*812()$C/,*3&'2(DA*E,&)*9,6FC/,
G,26$%,*+,*HI)1%(#(@$,
-JG;?>*:KLML

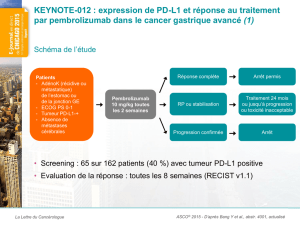
Le Cancer de l’Ovaire
• 30% de Survie à 5 ans
• Traitement :
– Chirurgie Lourde
– Chimiothérapie (Carboplatine / Taxol)
– New : Bevacizumab…
• Réponse au traitement :
– 80% : Réponse Initiale
• 70% récidive dans les 18 mois
• Récidive = Chimiorésistance
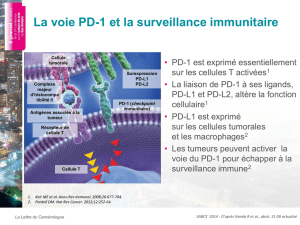
Introduction

Macro
Anatomo-Pathologie des CEO!
4 Histotypes : 98% des CEO!
Micro
Séreux (75%)
•Haut grade : 71%
•Bas Grade : 4,1%
Mucineuses (3,2%)
Endométrioïdes (8,3%)
A Cellules Claires (9,5%)
Gilks B and Concklin C 2013 (série de Vancouver)

Tumeurs de Type I
Tumeurs de Type II
Fréquence
25% des CEO
75% des CEO
Décès
10%
90%
Diagnostic
Stade Précoce
Stade Avancé (Carcinose)
Evolution
Lente
Rapide
Types
Histologiques
•Séreux de Bas grade
•Endométrioïde de Bas grade
•Cellules claires
•Mucineux
•Séreux de Haut grade
•Endométrioïde de Haut grade
•Carcinomes indifférenciés
•Carcinosarcomes
Mutations
•KRAS, BRAF, HER2 (Séreux)
•CTTNNB1, PTEN, PI3KCA
(Endométrioïde)
•KRAS (Mucineux)
•PI3KCA (Cellules Claires)
•ARID1A, PPP2R1A
•P53 (96% des Séreux de Haut Grade)
•BRCA (40-50% des cas)
Génomique
Stabilité Génomique
Instabilité Génomique
Précurseurs
Continuum Lésionnel : kyste Bénin
➔ Borderline ➔ Malin
Précurseurs : de novo, STIC
Anatomo-Pathologie des CEO!
Classification Dualiste (2 voies de Cancérogénèse)

CEO Séreux de Haut Grade !
Profil d’Expression: 4 sous types
Cancer Genome Atlas Research Network, Nature, 2011 (474) 609-615
fct° expression 1500 gènes
4 Sous-Types
Expression élevée
Expression faible
Mésenchymateux
Gènes de la composante stromale
(fibroblaste, péricyte vasculaire …)
Prolifératif
Facteurs de Transcription et de
Prolifération
Marqueurs de différenciation
(MUC16 et MUC1)
Différencié
Marqueurs de différenciation
(MUC16 et MUC1 )
-
Immunoréactif
Chemokines des lymphocytes T
CMH classe I et II
Programmed cell death ligand 1 (PD-L1)
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
1
/
26
100%