Comment Shigella trouve-t-elle son Gap ?

Bases fondamentales
Comment Shigella
trouve-t-elle son Gap ?
Gianfranco Grompone, Philippe Sansonetti,
Guy Tran Van Nhieu
Unité de Pathogénie Microbienne Moléculaire, Inserm U389 – Institut Pasteur,
28, rue du docteur Roux, 75015 Paris
<grompone@pasteur.fr>
Shigella, l’agent responsable de la dysenterie bacillaire, envahit
l’épithélium colique en utilisant un système de sécrétion de type III
lui permettant d’injecter des effecteurs bactériens, les protéines Ipa,
au sein de la membrane et du cytosol de la cellule épithéliale. Une
signalisation complexe faisant intervenir des petites GTPases de la
famille Rho ainsi que la tyrosine kinase Src provoque des profonds
remaniements du cytosquelette d’actine aboutissant à l’internalisa-
tion de la bactérie dans une poche de macropinocytose. Après
l’entrée, Shigella se déplace de cellule en cellule grâce à la
polymérisation de l’actine à l’un de ses pôles, ce qui assure sa
dissémination dans le tissu. L’invasion est suivie par un processus
inflammatoire aigu, recrutant des polynucléaires qui détruisent la
barrière épithéliale. Les jonctions intercellulaires communicantes
GAP potentialisent l’invasion et la colonisation de la bactérie dans
les cellules épithéliales. Les processus d’entrée et de dissémination
de Shigella sont favorisés par une communication intercellulaire
induite par la bactérie et dépendante des connexines. L’entrée de
Shigella dans la cellule induit la libération d’ATP dans le milieu
extracellulaire, ce qui, par un effet paracrin, favorise l’entrée
d’autres bactéries dans les cellules voisines.
Mots clés : shigellose, dysenterie bacillaire, Shigella
Le genre Shigella représente des entérobactéries responsables d’un
certain nombre de pathologies entériques chez l’homme, allant de
la diarrhée sporadique à l’infection aiguë de l’intestin caractérisée
par de la fièvre, des crampes intestinales et par la présence de sang dans
les selles (syndrome dysentérique) [1]. Quatre espèces différentes consti-
tuent le genre Shigella :S. flexneri (comprenant 6 sérotypes) majoritaire-
ment présente dans les pays en voie de développement, S. sonnei
(comprenant 1 sérotype) surtout présente dans les pays industrialisés,
S. dysenteriae (comprenant 16 sérotypes) et S. boydii (comprenant 8
sérotypes). Les deux premières espèces sont responsables de la forme
endémique de la maladie. S. dysenteriae inclut le sérotype 1 ou « bacille
de Shiga » capable de produire une puissante cytotoxine (« shigatoxin »),
à l’origine d’épidémies meurtrières dans les régions les plus pauvres de la
planète. S. boydii demeure une espèce confinée à l’Asie, responsable
d’un certain nombre de cas sporadiques de la maladie. En termes de
santé publique, la shigellose est présente majoritairement dans les pays
en voie de développement avec environ 160 millions de cas par an contre
Hépato-Gastro, vol. 13, n° 2, mars-avril 2006
Tirés à part : G. Grompone
139
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 26/05/2017.

1,5 millions seulement dans les pays industrialisés et
affecte principalement les enfants entre 1 et 5 ans. Le
nombre de décès peut aller de 740 000 à 1 million
par an [2].
Parmi les facteurs qui contribuent au développement de
la shigellose, le manque d’hygiène joue un rôle capital
puisque la maladie se transmet par le contact entre
personnes et l’ingestion d’aliments contaminés. Une
fois ingérée par l’hôte, la bactérie envahit la muqueuse
colique où elle entraîne une réaction inflammatoire
intense, principale responsable de la destruction tissu-
laire.
Schéma physiopathologique
de l’infection par S. flexneri
L’invasion et la colonisation de l’épithélium intestinal
par Shigella sont une étape clé pour l’établissement de
la maladie et le déclenchement du processus d’inflam-
mation. À l’instar d’autres germes entéroinvasifs, Shi-
gella envahit la muqueuse colique au niveau de l’épi-
thélium folliculaire à travers les cellules M. [3].
Contrairement aux entérocytes, les cellules M. sont
dépourvues de mucus, de glycocalyx et de microvillo-
sités et sont donc accessibles aux micro-organismes
CC
Shigella
Shigella
Arp2/3
Cdc42 Rac Src
cortactine
Abl
Crk
BB
Arp2/3
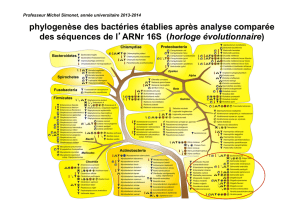
Figure 1.Cascade de signalisation induite après contact entre Shigella et la cellule épithéliale aboutissant à la formation d’une poche de
macropinocytose. L’appareil de sécrétion de type III permet l’activation des tyrosines kinases de la famille Abl, ce qui entraîne la
phosphorylation de la protéine Crk, et l’activation ultérieure des petites GTPases Cdc42 et Rac. Le complexe Arp2/3 est recruté comme
conséquence de cette activation, ce qui assure la nucléation de l’actine (représentée par les ronds verts) au niveau du foyer d’entrée. La
signalisation induite par l’appareil de sécrétion de type III permet aussi le recrutement local de la protéine Src et l’amplification de l’action des
GTPases par l’activation de la cortactine.
Bases fondamentales
Hépato-Gastro, vol. 13, n° 2, mars-avril 2006
140
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 26/05/2017.

présents au niveau du lumen. De plus, elles possèdent
une activité phagocytaire inhérente leur permettant
d’échantillonner les antigènes de la face luminale et de
les présenter aux macrophages associés aux cellules
M. Shigella tire partie de cette route d’entrée en indui-
sant l’apoptose des macrophages par l’activation de la
caspase 1. Ceci établit une véritable stratégie de
groupe pour l’agent pathogène : les premières bacté-
ries en contact avec les macrophages sont sacrifiées
afin d’induire l’inflammation par la sécrétion d’IL-1bet
IL-18. En réponse à cette sécrétion de cytokines, un
efflux massif de polynucléaires se produit, entraînant la
destruction de la barrière épithéliale et l’invasion massive
de nouvelles bactéries à partir des lésions tissulaires.
Shigella possède un plasmide de virulence qui code
pour les déterminants de son invasion et de sa dissémi-
nation dans les cellules épithéliales. L’invasion de Shi-
gella est déterminée par l’activité d’un appareil de
sécrétion de type III, codé par un ou deux opérons, mxi
et spa, au sein d’un îlot de pathogénicité de 30 kb
présent dans le plasmide de virulence. Cet appareil de
sécrétion forme une structure en aiguille qui permet
l’injection d’effecteurs bactériens dans la membrane et
le cytosol de la cellule cible. Avant l’interaction avec la
cellule eucaryote, ces effecteurs sont associés à des
protéines chaperones afin d’éviter leur dégradation
protéolytique, et assurer ainsi le contrôle de leur trans-
location. L’interaction entre Shigella et la cellule épithé-
liale induit des réarrangements massifs du cytosque-
lette d’actine aboutissant à l’internalisation de la
bactérie par la formation d’une poche de macropino-
cytose. Dans les étapes précoces de l’interaction,
l’association entre l’effecteur IpaB et le récepteur à
l’acide hyaluronique, CD44, permet le ciblage de
microdomaines lipidiques intervenant dans la mise en
place d’une plateforme de signalisation conduisant à
des remaniements du cytosquelette. La formation de la
poche de macropinocytose permettant l’entrée de Shi-
gella dans la cellule épithéliale obéit à une signalisa-
tion multifactorielle, médiée par les effecteurs IpaB,
IpaC, IpaA et IpgD [4]. D’une part, la partie carboxy-
terminale d’IpaC induit la nucléation et la polymérisa-
tion de l’actine par l’activation des petites GTPases de
la famille Rho (Cdc42 et Rac). D’autre part, le recrute-
ment et l’engagement du proto-oncogène c-src qui
phosphoryle la cortactine (une protéine de liaison à
5 min
D R/Ro = 20 %
HeLa
5 min
D R/Ro = 20 %
HCx26
IP3Ca2+
PLC
P2
Shigella Shigella
Hémicanal
fermé
ATP
Hémicanal
ouvert
BA
IP3Ca2+
PLC
Figure 2.Modèle représentant l’effet paracrin de l’ATP dans l’entrée de Shigella dans les cellules épithéliales. A) dans les cellules non
communicantes HeLa, Shigella induit des réponses calciques isolées après une première signalisation via la PLC et l’IP3 ; B) dans les cellules
exprimant la connexine 26 de façon stable (Hcx26), l’effet paracrin médié par l’ATP via les récepteurs purinergiques (P2) amplifie la fréquence
des réponses calciques et favorise l’entrée d’autres bactéries au niveau des cellules adjacentes.
Hépato-Gastro, vol. 13, n° 2, mars-avril 2006 141
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 26/05/2017.

l’actine) et régule négativement l’activation de Rho,
assurent une amplification de cette réponse membra-
naire (figure 1). Finalement, la complétion du proces-
sus d’entrée dépend de la fermeture de la poche de
macropinocytose, ce qui est assuré par la dépolyméri-
sation de l’actine grâce à la liaison de l’effecteur IpaA
au domaine amino-terminal de la vinculine (une pro-
téine associée au cytosquelette qui coordonne la for-
mation de plaques d’adhérence cellulaire).
Une fois internalisée, Shigella lyse la vacuole de pha-
gocytose et se multiplie librement dans le cytosol. Lors
de cette phase de multiplication, elle se déplace de
manière intracellulaire grâce à l’assemblage et à la
polymérisation de l’actine via l’action de la protéine
IcsA, située à un pôle de la bactérie. Shigella peut ainsi
induire la formation d’extensions cellulaires vers les
cellules voisines, qui permettent sa dissémination après
lyse des membranes des cellules donneuses et receveu-
ses. L’appareil de sécrétion de type III, de même que les
protéines IpaB et IpaC sont nécessaires à la dissémina-
tion de la bactérie, ce qui suggère que les processus
d’invasion et de colonisation de l’épithélium intestinal
utilisent des voies communes [5]. De plus, il a été
observé que les cadhérines, des récepteurs des jonc-
tions adhérentes dépendantes du Ca
2+
dans les cellu-
les épithéliales, sont requises pour la dissémination de
Shigella [6].
L’invasion des cellules épithéliales par la bactérie
induit une réponse inflammatoire liée à la sécrétion
d’IL8 après activation du facteur transcriptionnel
NF-jB. Récemment, un système d’alarme via des récep-
teurs cytosoliques de la famille Nod capables d’induire
NF-jB en réponse à une présence bactérienne intracel-
lulaire a été identifié [7]. Nod1 est prévalent au niveau
des cellules épithéliales intestinales et reconnaît spéci-
fiquement des muropeptides appartenant aux peptido-
glicanes de bactéries à Gram-négatif exclusivement,
tandis que Nod2 reconnaît le muramyl-dipeptide, struc-
ture commune à tous les peptidoglicanes [8, 9].
Rôle de la communication
intercellulaire dépendante
des connexines dans l’entrée
et la dissémination de Shigella
dans les cellules épithéliales
Les cellules qui composent l’épithélium intestinal com-
muniquent par l’intermédiaire de jonctions intercellulai-
res communicantes GAP, constituées de protéines trans-
membranaires comme les connexines. Elles
s’oligomérisent en hexamères afin de constituer un
hémicanal ou connexon. Lorsque ces structures rentrent
en contact avec un connexon présent dans une cellule
adjacente, elles forment un canal ouvert, à travers
lequel diffusent des seconds messagers comme l’AMPc,
le Ca
2+
ou l’inositol 1,4,5-triphosphate (IP3), impliqué
dans le relargage du Ca
2+
stocké dans le réticulum
endoplasmique [10].
Ces connexons peuvent se retrouver sans partenaire
dans la cellule adjacente et constituer ainsi des hémi-
canaux constitutivement fermés. La plupart des don-
nées existantes concernant le rôle des connexines
proviennent d’études réalisées sur les astrocytes et les
cellules nerveuses, même si leur existence a été décrite
dans plusieurs tissus épithéliaux, comme par exemple
pour la connexine 26 et 43. Il a été montré récemment
que les hémicanaux répondent à des inhibitions méta-
boliques ou à des augmentations du taux local d’IP3,
entraînant leur ouverture [10]. Le rôle de ces hémica-
naux demeure mal caractérisé dans les entérocytes.
Récemment, il a été montré que la dissémination de
Shigella dans les cellules épithéliales non communican-
tes de type HeLa était significativement favorisée lors-
que la connexine 26 est exprimée de façon stable dans
cette lignée. De même, la dissémination de Shigella au
sein des cellules polarisées de type Caco-2 se voit
significativement réduite par un traitement à l’AGA
(acide a-glycyrrhétinique), un inhibiteur des jonctions
communicantes GAP. Ces résultats suggèrent qu’un
second messager diffuse à travers les canaux à
connexines et favorise la dissémination de Shigella
dans les cellules épithéliales [11].
Shigella induit des réponses
calciques dans la cellule épithéliale
Il a été montré que Shigella induisait des réponses
calciques dans les cellules HeLa et dans des transfec-
tants exprimant la connexine 26. Dans les cellules
HeLa, la bactérie induit des réponses calciques lentes
et isolées (figure 2A). Ces réponses sont dépendantes
du système de sécrétion de type III, puisqu’un mutant
non invasif ne produit pas d’effet significatif. Dans les
cellules couplées, on observe aussi ce type de réponse,
sur lesquelles se « surajoutent » des oscillations rapides
du Ca
2+
intracellulaire, rappelant les réponses induites
par des agonistes dépendant du calcium (figure 2B).
Ces réponses sont inhibées par l’AGA (acide
a-glycyrrhétinique) ou le carbénoxolone, des inhibi-
teurs des jonctions gap et des hémicanaux, indiquant
qu’elles sont dépendantes de canaux formés par la
connexine 26.
L’ATP, sécrété par les hémicanaux
à connexine 26, favorise les réponses
calciques ainsi que l’invasion
et la dissémination de Shigella
dans les cellules couplées
L’invasion de Shigella dans les cellules exprimant la
connexine 26 induit la libération d’ATP dans le milieu
Bases fondamentales
Hépato-Gastro, vol. 13, n° 2, mars-avril 2006
142
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 26/05/2017.

extracellulaire. Par ailleurs, l’addition d’ATP dans le
milieu de culture à une concentration agoniste indui-
sant une réponse calcique maximale dans les cellules
HeLa (10 lM) stimule à la fois l’invasion et la dissémi-
nation de Shigella, dans des cellules non connectées.
Enfin, la suramine, un inhibiteur des récepteurs puriner-
giques, inhibe les oscillations rapides et oscillantes
observées dans des cellules exprimant la connexine
26, ainsi que l’invasion de Shigella dans ces cellules.
Ces résultats étaient inattendus, car la connexine 26
n’avait pas été décrite comme pouvant former des
hémicanaux. Afin de conforter ces résultats, il a été
montré que les cellules exprimant la connexine 26
peuvent incorporer un marqueur fluorescent, le Jaune
de Lucifer, en absence de calcium extracellulaire, un
traitement décrit comme provoquant l’ouverture des
hémicanaux. De manière cohérente avec l’existence
d’hémicanaux à connexine 26, cette incorporation est
inhibée par l’AGA ou le carbénoxolone et n’est pas
observée dans les cellules HeLa. En utilisant des tests
similaires, il a été montré que Shigella induit l’ouverture
des hémicanaux à connexine 26. De manière remar-
quable, l’ouverture des hémicanaux induite par Shi-
gella se fait à des concentrations de calcium physiolo-
giques. Cette ouverture est inhibée par l’U73122, un
inhibiteur de la PLC, ainsi qu’avec des concentrations
de Fura-2 interférant avec les réponses calciques : ceci
suggère que l’ouverture des hémicanaux dépend de
l’IP3 et de l’augmentation du calcium intracellulaire
induite durant l’invasion des cellules par Shigella.
Cependant, des agonistes du calcium tels l’ATP ou
l’histamine n’induisent pas l’ouverture des hémicanaux
à connexine 26, ce qui suggère un mécanisme spéci-
fique de la bactérie.
L’ATP constitue un second messager à action paracrine
rapide car : 1) il possède un gradient de sécrétion
positif (environ 10mM dans le milieu intracellulaire
contre 10nM à l’extérieur de la cellule) ; 2) il est le
ligand de récepteurs purinergiques membranaires spé-
cifiques, de type ionotropes (P2X) ou métabotropes
(P2Y), ces derniers induisent une transduction du signal
via les protéines G hétérotrimériques ; 3) il est rapide-
ment dégradé car il est la cible d’ectonucléotidases
présentes dans le milieu extracellulaire.
Nous proposons donc le modèle suivant dans lequel
l’invasion des cellules exprimant la connexine 26
conduit à une augmentation de l’IP3 et du calcium
intracellulaire. Cette augmentation permet l’ouverture
des hémicanaux et la sécrétion d’ATP dans le milieu
extracellulaire, qui stimule les réponses calciques ainsi
que l’invasion dans les cellules adjacentes par voie
paracrine (figure 2).
Conclusion
Le dialogue moléculaire conduisant au détournement
des fonctions cellulaires de la cellule épithéliale en
faveur des bactéries pathogènes entéro-invasives
comme Shigella demeure un champ d’investigations
riche et qui s’ouvre aujourd’hui à de nouvelles perspec-
tives. Le rôle des jonctions intercellulaires communican-
tes GAP dans l’entrée et la dissémination de Shigella
est un clair exemple du caractère dynamique de ce
phénomène et du besoin de la mise en place d’appro-
ches pluridisciplinaires permettant l’analyse molécu-
laire et tissulaire des processus inflammatoires.
Références
1
. Hale TL. Bacillary dysentery. Topley and Wilson’s microbiology and
microbial infections. B. Infections. Vol. 3. London. In : Hausler WJ,
Sussman M, eds, 1998.
2
. Kotloff KL, Winickoff J-P, Ivanoff B, Clemens JD, Swerdlow DL,
Sansonetti PJ, et al. Global burden of Shigella infections : implications for
vaccine development and implementation of control strategies. Bull
World Health Organ 1999 ; 77 : 651-66.
3
. Sansonetti PJ. Rupture, invasion and inflammatory destruction of the
intestinal barrier by Shigella, making sense of prokaryote-eukaryote
cross-talks. FEMS Microbiology Reviews 2001 ; 25 : 3-14.
4
. Tran Van Nhieu G, Bourdet-Sicard R, Dumenil G, Blocker A,
Sansonetti PH. Bacterial signals and cell responses during Shigella entry
into epithelial cells. Cell Microbiol 2000;2:187-93.
5
. Schuch R, Sandlin RC, Maurelli AT. A system for identifying post-
invasion functions of invasion genes : requirements for the Mxi-Spa type
III secretion pathway of Shigella flexneri in intercellular dissemination.
Mol Microbiol 1999 ; 34 : 675-89.
6
. Sansonetti PJ, Mounier J, Prevost MC, Mege RM. Cadherin expres-
sion is required for the spread of Shigella flexneri between epithelial cells.
Cell 1994 ; 76 : 829-39.
7
. Girardin SE, Philpott DJ, Lemaitre B. Sensing microbes by diverse
hosts. Workshop on pattern recognition proteins and receptors. EMBO
Rep 2003;4:932-6.
8
. Girardin SE, Boneca IG, Carneiro LA, Antignac A, Jehanno M,
Viala J, et al. Nod1 detects a unique muropeptide from gram-negative
bacterial peptidoglycan. Science 2003 ; 300 : 1584-7.
9
. Girardin SE, Boneca IG, Viala J, Chamaillard M, Labigne A,
Thomas G, et al. Nod2 is a general sensor of peptidoglycan through
muramyl dipeptide (MDP) detection. J Biol Chem 2003 ; 278 : 8869-72.
10
. Willecke K, Eiberger J, Degen J, Eckardt D, Romualdi A,
Guldenagel M, et al. Structural and functional diversity of connexin
genes in the mouse and human genome. Biol Chem 2002 ; 383 :
725-37.
11
. Tran Van Nhieu G, Clair C, Bruzzone R, Mesnil M, Sansonetti P,
Combettes L. Connexin-dependent inter-cellular communication increases
invasion and dissemination of Shigella in epithelial cells. Nat Cell Biol
2003;5:720-6.
Hépato-Gastro, vol. 13, n° 2, mars-avril 2006 143
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 26/05/2017.
1
/
5
100%





![Télécharger la fiche technique [120.43 Ko PDF]](http://s1.studylibfr.com/store/data/000674177_1-17ee923c1234f9f2353ebcf5ad682c82-300x300.png)