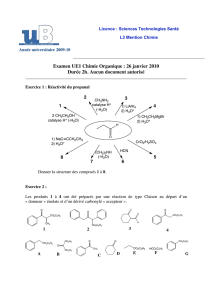
Corrigé DS5 (Partie Chimie Organique) - PCSI

Corrigé DS5 (Partie Chimie Organique)
1. Ecrire pour chaque composé une autre forme limite (illustrant une délocalisation électronique maximale).
2. Une des formules suivantes présente une anomalie, l’entourer Il faut avoir un DI ∈ Ν. .
C8H14
C6H14O3
C3H11N2
C7H12O3
3. Le pH d’une solution molaire d’acide chlorhydrique (acide fort) vaut :
0 - 1 - 2 - 3 (entourer la valeur correcte) pH= -log [H3O+] = -log 1 = 0
4. A une solution molaire d’acide formique dans l’eau à l’équilibre on ajoute 100 mL d’acide chlorhydrique
molaire. La concentration d’ion formiate va :
Rester constante
NON
[HCOOO-] x [H3O+]
KA = = Constante
[HCOOOH]
Diminuer
OUI
[HCOOO-] = Constante ([HCOOOH] initiale)
[HCOOOH] +
Augmenter
NON
Si [H3O+] alors [HCOOOH] et [HCOOO-]
5. Les deux composés suivants sont-ils des :
énantiomères
NON
conformères
NON
diastéréoisomères
OUI
Répondre par Oui ou par Non
isomères géométriques
NON

6. Dessinez ci-dessous un isomère de fonction, un isomère de position ou de squelette et un isomère géométrique
du composé suivant :
ISOMERE = MEME Formule brute soit C8H15ClO (DI = 1)
Isomère de fonction
(exemple possible)
Isomère de position ou de squelette
(exemple possible)
Isomère géométrique
(le seul exemple possible)
7. Dessinez ci-dessous en représentation de Fischer mais Cram le (2R,3S)-butane-2,3-diamine. Ce composé est-il
chiral ?
CH3
H NH2
CH3
H NH2
σ
Achirale car il y a un
centre d’inversion (ou
plan de symétrie selon la
représentation de Cram)
8. Complétez le schéma de Lewis ci-dessous en faisant figurer les doubles liaisons et les doublets non liants (pas
d’atomes supplémentaires et pas de charge).
C
C
C
C
C
C
C
C
C
C
O
C
C
C
I
C
O
F
Cl
HH
H H
N
HH
H
H
-
-
-
-
-
-
-
-
-
-
-
-
-
-
1
/
2
100%