Cours Cohésion des solides ioniques et moléculaires

1
Cours
Blocs : Comprendre
Ref :
Cohésion_des_solides_eleves.docx
Cohésion des solides ioniques et
moléculaires
1S ………..- Chap …10…..
NOM : ………………………….
……………
I. Cohésion des solides ioniques. ................................................................................................................................. 2
Interactions électrostatiques et cohésion .............................................................................................. 2
Formule d'un composé solide ionique ........................................................................................................ 2
Dissolution / Titre massique et concentration molaire du soluté ...................................................... 2
Protocoles de dissolution et de dilution (TP) ........................................................................................... 2
Rappel concentrations massique et molaire / lien .................................................................................. 2
Concentration du soluté lors d'une dissolution ou d'une dilution ...................................................... 2
Concentrations des ions dans une solution ionique ................................................................................ 3
Exercices ……………………………………………….…………………………………………………………………………………………………………… ……3
II. Molécules polaires et apolaires. ............................................................................................................................ 3
1 Electronégativité d'un élément .................................................................................................... 3
2 Polarité d'une liaison et moment dipolaire ................................................................................ 4
3 Polarité d'une molécule .................................................................................................................. 4
cas d'une molécule diatomique .................................................................................................................... 4
cas d'une molécule polyatomique (eau et gaz carbonique) .................................................................... 4
Exercices …………………………………………………………………………………………………………………………………………………………………….4
III. Cohésion des solides moléculaires. ..................................................................................................................... 5
1 Les solides moléculaires. ................................................................................................................ 5
2 Les interactions de Van der Waals. ............................................................................................ 6
3 La liaison hydrogène ....................................................................................................................... 7
Exercices ……………………………………………………..………………………………………………………………………………………………………….…7
CONCLUSION ................................................................................................................................................................. 7
Cohésion et transformations de la matière
Solide ionique. Interaction électrostatique ; loi de Coulomb.
Solide moléculaire. Interaction de Van der Waals, liaison
hydrogène.
Électronégativité.
Effet du caractère polaire d’un solvant lors d’une dissolution.
Conservation de la matière lors d’une dissolution.
Recueillir et exploiter des informations sur les applications de
la structure de certaines molécules (super absorbants,
tensioactifs, alginates, etc.).
Prévoir si un solvant est polaire.
Écrire l’équation de la réaction associée à la dissolution dans
l’eau d’un solide ionique.
Savoir qu’une solution est électriquement neutre.
Élaborer et réaliser un protocole de préparation d’une solution
ionique de concentration donnée en ions.
Mettre en œuvre un protocole pour extraire une espèce
chimique d’un solvant.

2
I. Cohésion des solides ioniques.
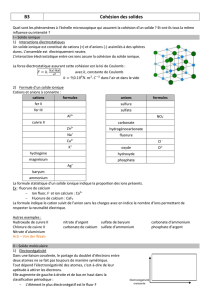
Doc de présentation : « structure du chlorure de sodium.ppt »
Un solide ou ……………………. ionique est constitué d'anions et de cations, assimilés à des sphères dures,
régulièrement espacées dans l'espace.
Un solide ionique est électriquement ……………………………….
Dans un tel cristal, chaque ion s'entoure d'ions de …………………………………………………….. L'interaction électrostatique
………………………………………. existant entre ces ions de charges contraires assure la cohésion du solide ionique.
La formule d'un solide ionique comporte le nombre minimal de cations et d'anions permettant la neutralité
électrique du cristal ionique. Elle commence toujours par la formule du …………………………..
Le nom du solide commence par celui de l'……………………….., suivi de celui du cation.
Tableau des ions les plus courants (voir fiche récapitulative)
Exemple d’écriture :
L'oxyde d'aluminium est constitué d'ions oxyde O2- et d'ions aluminium Al3+, a pour formule statistique Al2O3 .
Le cation est l’ion Al3+, et l’anion l’ion O2-
Le sulfate d’aluminium est constitué d’ions sulfate SO42- et d’ions aluminium Al3+ ; il s’écrira sous forme solide
Al2(SO4)3
Donnez les formules des solides ioniques suivants : fluorure de calcium ……………………………………………..
nitrate de fer (III) ………………………………………………
hydroxyde de cuivre (II) ………………………………………
Exercices sur site prof
Protocole de dissolution et de dilution (voir fiche distribuée en tp)
Rappels titre massique et concentration molaire du solide S dissout (le soluté)
Comprenons bien : on dissout un soluté dans un solvant pour obtenir une solution de ce soluté.
Titre massique en soluté (en g.L-1):
Concentration molaire en soluté (en mol.L-1) :
Docs de présentation : [Dissolution_du_sel.swf ] [Dissolution_du_sel.flv]
Il y a 3 phases dans la dissolution d’un solide ionique dans l’eau :
Le solide ionique (ou cristal ionique) se dissocie car les cations du cristal sont attirés par les atomes d'oxygène des
molécules d'eau et les anions du cristal sont attirés par les atomes d'hydrogène des molécules d'eau : ………………………….
Puis les ions sont entourés de molécules d'eau : …………………………………..
Enfin, à cause de l'agitation thermique, les ions hydratés s'éloignent du cristal : …………………………………..
AN :
a) Quelle masse de fluorure de calcium faut-il dissoudre dans 25,0 mL d’eau pour obtenir une solution de titre on
5,0.10-2 g.L-1 en fluorure de calcium
b) Déterminer la concentration molaire en chlorure de sodium apporté d’une solution préparée par dissolution de
5,85 g de sel dans 200cm3 d’eau :

3
Lien entre la concentration molaire en soluté apporté et la concentration effective des ions
dans la solution :
Exemple du sulfate d’aluminium solide, que l’on suppose intégralement dissout dans l’eau :
Avancement
EI
0
nS
En cours
x
EF
xmax
Donc xmax = …………………..
La dissolution est une réaction chimique car l’état final (des ions) est différent de l’état initial (un solide et de l’eau); donc on aura :
Al2(SO4)3 (s) 2 Al3+ (aq) + 3SO42- (aq)
Concentration molaire du soluté apporté Concentrations molaires effectives des ions
Exercices p174 n° 11 – 15 – 17 - 18
II. Molécules polaires et apolaires.
1 Électronégativité d'un élément chimique. Doc de présentation : [ Electronegativite ds Tab_periodique.ppt ]
Lorsque deux atomes liés par une …………………………………………… sont identiques, la paire d'électrons formant la liaison est
répartie de manière …………………………………………………… entre les deux atomes.
Cependant certains atomes ont plus ou moins tendance à attirer les électrons de la liaison covalente à eux.
Un atome A est plus ……………………………………………… qu'un atome B s'il a tendance à attirer à lui les électrons (le
doublet) de la liaison covalente qui le lie à B.
Electronégativité
Ressource image : électronégativité dans tableau périodique.ppt

4
L'électronégativité des atomes évolue selon leur position dans la classification périodique :
▪ elle augmente de gauche à droite sur une même ligne (…………………………………….),
▪ elle augmente de bas en haut dans une même colonne (………………………………………..).
Les alcalins (col I) ont tendance à ……………………………… des électrons (donc sont ……………………… électronégatifs), alors que
les halogènes (col XVII) ont tendance à ……………………………… des électrons (donc sont ……………… électronégatifs).
Doc de présentation : (téléchargement de 10 min) [molecule-polarity_fr.jar]
2 Polarité d’une molécule
Cas d’une molécule diatomique
Exemple : molécule de chlorure d’hydrogène HCl
Ces molécules sont constituées d’un atome d’hydrogène lié à un atome de chlore par une liaison covalente.
Représentation de Lewis
Caractéristiques géométriques
H Cl
dH-Cl = 127 pm
Le chlore est …………………….. électronégatif que l’hydrogène. Il …………………………. vers lui le doublet de liaison : on dit que
la liaison H – Cl est ……………………………………..
Cette polarisation fait apparaître :
un excédent de charge négative, notée –q , sur l’atome de chlore (q représente la charge partielle)
un excédent de charge positive, notée +q , sur l’atome d’hydrogène.
La molécule de chlorure d’hydrogène a ainsi un caractère ………………………….. : elle constitue un dipôle électrique. Elle
peut être représentée par un dipôle portant les charges –q et +q.
Plus généralement, un dipôle électrique est l’ensemble constitué par 2 charges opposées – q et + q séparées par la
distance d ; il est caractérisé par son ………………………………………………………… :
Ce moment dipolaire est représenté par un vecteur
colinéaire à la liaison et orienté du pôle ……………………………… vers
le pôle ……………………………………….. du dipôle.
Le moment dipolaire s’exprime en ……………………………….. (symbole D)
Exemple : pour la molécule de chlorure d’hydrogène : p(H-Cl) = 1,1 D
Conclusion : Une liaison covalente est polarisée lorsque les deux atomes liés ont des électronégativités
différentes.
Une molécule, entre deux atomes A et B est ………………………………….. si ces deux atomes ont des électronégativités
différentes. Plus la différence d’électronégativité est …………………………….., plus la liaison est polarisée, et plus le moment
dipolaire
est …………………………………... Une molécule diatomique constituée de deux atomes identiques est apolaire.
+q
- q
d

5
Cas d’une molécule polyatomique (possédant plus de deux atomes)
1. Cas de la molécule d’eau H2O
Représentation de Lewis
Caractéristiques géométriques
H O
H
dH-O = 96 pm
molécule coudée 105°
Le moment dipolaire résultant est la somme ……………………………………………. des moments dipolaires des deux liaisons O-H.
La molécule présente un …………………………………………………… { p(H2O) = 1,8 D } : on dit que c’est une molécule ………………….
Mise en évidence de cette propriété : bâton de plexiglas et filet d’eau
2. Cas de la molécule de dioxyde de carbone CO2
Représentation de Lewis
Caractéristiques géométriques
O C O
DC=O = 116 pm
molécule linéaire
Le moment dipolaire résultant est ……… car la molécule est linéaire: la molécule de dioxyde de carbone est ………………...
Conclusion :
Pour une molécule polyatomique, le moment dipolaire est la somme géométrique des moments dipolaires
associés à chaque liaison.
Le moment dipolaire résultant est lié à la géométrie de la molécule.
Exercices : p 157 n° 19 et p 174 n° 9
+q
+q
- 2 q
+2q
-q
-q
 6
6
 7
7
1
/
7
100%