Les tumeurs dérivées de patients : un ancien

Les tumeurs dérivées de patients :
un ancien concept redevenu
populaire dans la recherche
translationnelle en oncologie
Pour citer cet article : Vrignaud P. Les tumeurs dérivées de patients : un ancien concept redevenu populaire dans la recherche
translationnelle en oncologie. Innov Ther Oncol 2016 ; 2 : 43-48. doi : 10.1684/ito.2016.0022
RÉSUMÉ
Les tumeurs dérivées de patient ou patient-derived tumor xenografts (PDX)
sont actuellement considérées comme étant des modèles expérimentaux
prédictifs de la réalité clinique en oncologie. Étant toujours maintenues sur
l’animal, sans passage par des cultures cellulaires in vitro, elles conservent
une morphologie et une hétérogénéité tumorale proches de la tumeur
d’origine du patient. Il en est de même pour leurs caractéristiques
moléculaires, ce qui n’est pas le cas des xénogreffes classiques obtenues à
partir de lignées cellulaires tumorales cultivées in vitro. Même si leur mise en
place est un processus long et complexe, les PDX bien caractérisées sont
de plus en plus utilisées dans la recherche translationnelle en cancérologie.
Elles sont des outils précieux servant à l’identification et à la validation de
cibles thérapeutiques, à l’évaluation des nouveaux agents anticancéreux
et de leurs biomarqueurs associés, ainsi qu’àl’étude des mécanismes de
résistance. Dans le contexte de la médecine de précision, la création de ce
que l’on a appelé « avatars » de la tumeur des patients a récemment été
réalisée pour orienter les choix thérapeutiques offerts à chaque patient.
En revanche, l’évaluation de thérapies impliquant la réponse de l’environne-
ment tumoral est fortement limitée en absence d’un micro-environnement
humanisé. Cela est plus particulièrement critique pour les thérapies impliquant
une réponse immunitaire, ces modèles tumoraux étant xénogreffés sur
des hôtes immunodéprimés. Des stratégies d’humanisation de l’hôte sont
actuellement en cours de développement. Ces nouveaux modèles expéri-
mentaux jouent donc un rôle central dans la recherche translationnelle
anticancéreuse.
lMots clés : modèles animaux ; xénogreffes ; cancer.
ABSTRACT
Patient-derived tumour xenografts (PDX) are currently considered to be
predictive of clinical activity in cancer patients. Having only been maintained
in animals and never in in vitro cell cultures, they retain tumour morphology
and heterogeneity, which is similar to the original patient tumour. The same
holds for their molecular characteristics, which is not the case for classic
xenografts obtained from tumoural cell lines cultivated in vitro. Despite a
complex and time-consuming process to establish, well-characterised PDX
are used increasingly often in translational cancer research. They are precious
tools for identifying and validating new therapeutic targets, screening new
anti-cancer agents and related biomarkers, and investigating resistance
mechanisms. In the context of personalised cancer therapy, what are known
as ‘mouse avatars’of patient tumours have recently been created to guide
the therapeutic choices given to individual patients. Nevertheless, evaluation
Patient-derived tumour
xenografts:
an old concept gaining
renewed interest in
translational cancer
research
Patricia Vrignaud
Gustave-Roussy
114, rue Édouard-Vaillant
94805 Villejuif cedex
France
Remerciements et autres mentions :
L’auteur membre du consortium
CReMEC remercie MEDICEN - région
parisienne et le ministère français
de l’Industrie pour leur soutien dans la
mise en place d’une collection de PDX
colorectales. Nos remerciements vont
également aux patients et à leur famille
grâce à qui ces modèles expérimentaux
peuvent être créés.
Financement : aucun.
Liens d’intérêts : Employée par Sanofiet
détenant des actions de la compagnie.
Tirés à part : P. Vrignaud
Innovations & Thérapeutiques en Oncologie lvol. 2 –n81, janv-fév 2016 43
doi: 10.1684/ito.2016.0022
Passerelle translationnelle PT
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

L’utilisation de tumeurs dérivées de patients ou
patient-derived tumor xenografts (PDX) n’est pas
un concept nouveau [1], mais leur utilisation avant les
années 2000 était très limitée. Pourquoi les tumeurs
dérivées de patients ont-elles autant de succès depuis
quelques années ? Une des explications citées le plus
souvent concerne le très fort taux d’attrition en cancéro-
logie (95 %) pour les nouveaux agents lors des études
cliniques [2]. Ces échecs concernent pour la moitié d’entre
eux des thérapies ciblées sélectionnées sur la base de leur
activité en préclinique, mais qui ont été trouvées inactives
lors des essais cliniques. À la suite de cette constatation, il a
été conclu qu’ilfallait améliorer les modèles précliniquesen
oncologie. Cependant, quel modèle préclinique pourrait à
lui seul couvrir la diversité tumorale et les différents types
de cancer ? Plusieurs générations de modèles murins ont
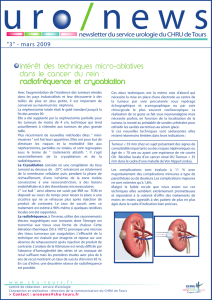
été développées en oncologie (figure 1): des tumeurs
spontanées ou induites par des carcinogènes, des (xéno)
greffes de cellules ou de fragments tumoraux, des modèles
transgéniques obtenus par transgenèse classique, recom-
binaison homologue ou plus récemment grâce au système
CRISPR/cas9 [3]. Le choix d’un modèle tumoral en
cancérologie expérimentale est fonction de l’objectif à
atteindre. Selon qu’il s’agit de la validation d’une cible, de
la preuve du concept que cette cible peut être inhibée par
une petite molécule ou un agent biologique, ou de la
définition des caractéristiques pharmacologiques d’un
candidat au développement clinique, différents modèles
tumoraux seront envisagés [4]. La première génération de
modèles utilisés en oncologie, ceux qui ont permis de
sélectionner les agents cytotoxiques actuellement utilisés
en thérapie anticancéreuse, a été développée à partir de
tumeurs spontanées ou chimio-/viro-induites, obtenues sur
des souris consanguines, puis maintenues sur la même
souche de souris consanguines par passages successifs, en
les greffant par voie sous-cutanée dans la majeure partie
des cas. Ces modèles murins ne permettent cependant pas
d’évaluer des thérapies spécifiques d’une cible humaine,
comme c’est souvent le cas des agents biologiques qui ne
reconnaissent pas la cible murine. La découverte d’une
souris immunodéprimée dont la mutation génétique
confère une lymphopénie T associée à une absence de
pelage, d’où son qualificatif anglais de souris nude (nue), a
ouvert la voie des modèles tumoraux humanisés. Ces
xénogreffes de cellules tumorales humaines ont été
utilisées pour sélectionner la plupart des thérapies ciblées.
Cependant, ces cellules tumorales humaines ont été
cultivées en monocouche dans des boîtes de culture, ce
qui présente un environnement très éloigné de celui d’une
tumeur se développant au sein d’un organe. Elles ont donc
perdu la plupart des caractéristiques de la tumeur d’origine
du patient. Les modèles de tumeurs de patients directe-
ment implantées chez la souris immunodéprimée sans
passage en culture cellulaire sont maintenant largement
utilisés non seulement pour évaluer de nouvelles thérapies
anticancéreuses, mais également pour identifier et valider
des cibles [5].
Les PDX sont mises en place à partir de fragments
de tumeurs de patients obtenues lors de l’exérèse de la
tumeur ou suite à une biopsie tumorale. Les patients
doivent au préalable avoir donné leur consentement à
l’utilisation de leur tumeur à des fins de recherche, incluant
les analyses génétiques qui seront réalisées. Pour éviter des
risques de contaminations accidentelles lors de la prépara-
tion des greffons et de la xénogreffe en animalerie, une
sérologie du patient pour les virus VIH et des hépatites B et
C est fortement recommandée. Différents critères sont à
respecter pour optimiser le taux de prise des PDX, c’est-à-
dire le pourcentage de modèles tumoraux obtenus après la
xénogreffe de tumeurs au sein d’une même indication
thérapeutique. Les premiers critères à prendre en compte
concernentles temps d’ischémie chaude et froide, ainsi que
le milieu de survie dans lequel la tumeur sera conservée
entre la salle d’opération et l’animalerie où aura lieu la
greffe. L’utilisation d’antibiotiques dans le milieu de survie
est recommandée, en particulier pour les tumeurs coliques
qui, du fait de leur localisation d’origine, sont largement
porteuses de germes. Un autre point important à prendre
en considération est la taille et la qualité du greffon
tumoral. Le nombre de cellules tumorales implantées va
conditionner le succès de la prise de la greffe. Il est donc
important de s’assurer que la zone choisie pour le greffon
contienne suffisamment de cellules tumorales et d’éviter
les zones de nécrose. Enfin, le choix de la souche de souris
immunodéprimée qui sera utilisée va, lui aussi, avoir une
importance dans le succès de cette greffe tumorale. Pour
maximiser le taux de prise des PDX, la tendance est
d’utiliser des animaux de plus en plus immunodéprimés. Les
souris severe combined immunodefeciency (SCID) sont des
souris mutantes n’ayant pas de lymphocytes B et T matures.
Il existe plusieurs souches de souris dérivées à partir de la
souris SCID, comme les souris NSG (NOD/SCID-IL2Rg
-/-
) ayant
une délétion du récepteur de l’IL-2 (interleukine 2). Elles
of therapies involving the microenvironment of the tumour is often
limited due to the murine origin of PDX stromal components. This is
particularly critical for therapies involving specific immunotherapeutic
responses, given that these models have been xenografted to the
immunodeficient murine hosts. Humanised mouse models are currently
being developed to overcome these issues. In conclusion, these new
experimental animal models play a key role in translational cancer
research.
lKey words: animal models; xenografts; cancer.
P. Vrignaud
44 Innovations & Thérapeutiques en Oncologie lvol. 2 –n81, janv-fév 2016
Passerelle translationnelle PT
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

n’ont pas de lymphocytes B et T matures, leurs cellules
natural killer (NK) ne sont pas fonctionnelles, et la voie de
signalisation des cytokines est altérée. Cependant, l’utilisa-
tion de ces souches dont l’immunité est fortement
déprimée autorise l’émergence d’une lymphomagenèse
d’origine humaine au détriment de la tumeur du patient
[6].L’utilisation de souris moins immunodéprimées, comme
la souris nude, permet d’éviter ce problème. Cela a été, en
particulier, décrit pour les PDX de tumeurs pulmonaires
non à petites cellules [7]. La localisation de la primo-greffe
sur l’animal devrait avoir également une influence sur
le succès de la greffe et a fait l’objet de nombreuses études.
La greffe sous-cutanée est facile à réaliser, rapide etpermet
de suivre la croissance de la tumeur avec un pied à coulisse
[8]. Cependant, la greffe orthotopique (la tumeur est
greffée dans son tissu d’origine) est souvent favorisée
pour prendre en compte les interactions avec le stroma.
Cette technique peut être plus ou moins difficile à mettre
en œuvre, nécessitant une chirurgie qui dans certains cas
sera faiblement invasive, par exemple pour les tumeurs
mammaires [9]. Mais elle sera plus complexe à réaliser pour
les autres localisations, le suivi de la croissance tumorale
nécessitant le plus souvent l’utilisation de techniques
d’imagerie. Enfin, la greffe sous la capsule rénale
est souvent présentée comme la meilleure option
pour favoriser la prise du greffon tumoral, mais reste
controversée. Des traitements hormonaux dans l’eau de
boisson ou par implant à libération lente sont systémati-
quement rajoutés pour tous les types tumoraux hormono-
dépendants, comme les tumeurs mammaires, ovariennes,
utérines et prostatiques, et ce quelle que soit leur
dépendance hormonale.
« Les PDX ont des limites
à considérer »
Une des limitations majeures de la mise en place de PDX
est leur faible taux de prise dans certaines indications.
Il varie énormément en fonction du type tumoral,
étant inférieur à 10 % pour les tumeurs de la prostate
ou les tumeurs mammaires et supérieur à 50 % pour
les tumeurs colorectales, pancréatiques ou gastriques.
Pour l’améliorer, les tumeurs sont parfois enrichies avec
des cellules stromales lors de la primo-greffe [10]. Au sein
d’une même indication tumorale, le taux de prise peut
varier de façon importante, comme cela a été décrit pour
les tumeurs du poumon non à petites cellules, où le taux
de prise des adénocarcinomes (13 %) était très largement
XénogreffesViro-/Chimio-induits Spontanés
Première génération
Seconde génération
Modèles génétiquement modifiés
Modulation d’expression
de gènes
(RNAi/shRNA)
Transgénèse
classique
Tumeurs
inductibles
Tet-Off/Tet-On
Recombinaison
homologue
KO/KI
PDX
CRISPR/Cas9
CRISPR/Cas9 = CRISPR est l'acronyme anglais pour « courtes répétitions en palindrome regroupées et régulièrement espacées » et Cas9
concerne le nom de la nucléase intégrée dans ce système permettant de « copier-coller » un gène ; KO/KI = la fonction d'un gène
est interrompue (KO) ou activée (KI) ; PDX = tumeurs dérivées de patients (patient-derived tumor xenografts) ; RNAi = interférence
d'un ARN (acide ribonucléique) avec un ARN messager spécifique pour dégrader ou diminuer l'expression de sa protéine ; shRNA =
petit ARN en épingle à cheveux induisant une inhibition transitoire ou stable du gène cible ; Tet-Off/Tet-On = expression réprimée (Off)
ou activée (On) d'un gène inductible par la tétracycline (Tet).
Figure 1. Évolution des modèles tumoraux.
Figure 1. Evolution of tumoural models.
Les tumeurs dérivées de patients : un ancien concept redevenu populaire dans la recherche translationnelle en oncologie
Innovations & Thérapeutiques en Oncologie lvol. 2 –n81, janv-fév 2016 45
Passerelle translationnelle PT
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

inférieur à celui des carcinomes épidermoïdes (60 %) [7].
L’agressivité de la tumeur d’origine de la PDX va
influencer la prise de la xénogreffe, comme démontré
dans les tumeurs du poumon non à petites cellules où les
PDX générées à partir de métastases cérébrales ont un
meilleur taux de prise (74 %) que celles obtenues à partir
des tumeurs primaires (23 %) [11]. Cela est logiquement
relié à la constatation que la prise tumorale d’une PDX est
un facteur de mauvais pronostic pour la survie des
patients et a été démontré pour différentes indications
tumorales [8, 12].
Les avantages et les limitations des PDX sont à prendre en
compte en fonction de l’objectif de l’étude à réaliser
(tableau 1). Les PDX sont régulièrement décrites comme
étant plus proches de la réalité clinique. La première
Tableau 1. Avantages et désavantages des PDX par rapport aux xénogreffes obtenues à partir de cellules tumorales humaines
cultivées in vitro.
Table 1. Advantanges and disadvantages of PDX in comparison with xenografts obtained from human
tumoural cells cultivated in vitro.
PDX Xénogreffes de cellules
tumorales humaines
Avantages Inconvénients Avantages Inconvénients
Mise en place
Complexe (tumeurs
de patients récupérées
en milieu hospitalier)
Aisée (culture
cellulaire)
Taux de prise variable
Lymphomagenèse humaine
(0-10 % selon la souche
de souris utilisée)
Lymphomagenèse
murine (5%)
Lymphomagenèse
murine (5%)
Morphologie
Identique à la
tumeur d’origine
Très différente de la
tumeur d’origine
Stroma murin remplaçant
le stroma humain
Stroma murin
Maintien d’une
hétérogénéité
tumorale
Perte de certains clones
de la tumeur d’origine
Sélection clonale
Caractérisation
moléculaire
Proche de la
tumeur d’origine
Contamination par
le stroma murin
Utilisation de la lignée
cellulaire évitant la
contamination
du stroma murin
Dérive génétique
par rapport à
la tumeur d’origine
Dérive génétique au
sein d’une même
lignée entre les
différents utilisateurs
Utilisation
Corrélation in vitro/in vivo
complexe (cultures 3D)
Corrélation
in vitro/in vivo
Réponse aux
thérapies ciblées
Nécessité de tester
un panel
Réponse aux thérapies
ciblées peu prédictive
Relations PK/PD Métabolisme murin Relations PK/PD Métabolisme murin
Découverte de
biomarqueurs
Voies de signalisation
souvent altérées
Avatar de la tumeur
du patient
Perte des caractéristiques
de la tumeur d’origine
Hôte immunodéprimé Hôte immunodéprimé
3D : en trois dimensions ; PD : pharmacodynamie ; PDX : tumeurs dérivées de patients (patient-derived tumor xenografts);
PK : pharmacocinétique.
P. Vrignaud
46 Innovations & Thérapeutiques en Oncologie lvol. 2 –n81, janv-fév 2016
Passerelle translationnelle PT
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

caractéristique qui les différencie des xénogreffes obte-
nues à partir de cellules tumorales cultivées in vitro,
appelées « xénogreffes classiques », est au niveau de leur
histologie. Ces xénogreffes de tumeurs humaines main-
tenues in vivo conservent une histologie comparable à
celle de la tumeur d’origine du patient [8, 13]. Cette
caractéristique est conservée lors des passages successifs,
alors que le stroma humain présent au sein du greffon lors
de la primo-greffe va être remplacé par un stroma murin
[8, 14].L’hétérogénéité tumorale de la tumeur du patient
est globalement conservée dans les PDX, mais sans assurer
une conservation de 100 % des différents types cellulaires
tumoraux contenus dans la tumeur d’origine du patient. Le
stroma de la tumeur d’origine étant perdu rapidement,
certaines stratégies thérapeutiques nécessitant la réponse
du micro-environnement tumoral seront biaisées et
nécessiteront la mise en place destratégies d’humanisation
de ce stroma [15]. Comme indiqué précédemment, les PDX
sont maintenues uniquement in vivo pour éviter les dérives
génétiques. L’explosion des techniques de séquençage à
haut débit du génome a permis d’approfondir la caracté-
risation moléculaire de ces modèles. C’est une étape
décisive pour une utilisation optimale des PDX dans le
cadre de l’évaluation des thérapies ciblées. Il est cependant
important de prendre en compte une contamination
potentielle du stroma murin dans l’analyse bio-informa-
tique. Cet inconvénient n’avait pas été identifiéavecles
xénogreffes « classiques » grâce à l’utilisation des lignées
cellulaires pour les analyses génétiques. Le statut muta-
tionnel et l’analyse d’expression des gènes des PDX ont été
trouvés très proches de ceux de la tumeur d’origine du
patient [13]. Le profild’expression des gènes et leur
stabilité sont conservés au cours des passages, comme cela a
été montré sur des PDX pancréatiques entre les passages
10 et 39 [16]. Cependant, en règle générale, les PDX ne sont
maintenues que sur un nombre limité de passages, dès qu’il
est possible de les faire repartir à partir de fragments
congelés. Cela permet d’obtenir une meilleure reproducti-
bilité des études, d’éviter de faire des contrôles molécu-
laires au cours du temps et de diminuer grandement le
nombre de souris utilisées pour le maintien des PDX.
Les PDX sont donc morphologiquement et génétiquement
plus proches de la réalité clinique. Sont-elles également
plus prédictives de la réponse aux thérapies ciblées ? Un
autre avantage de ces modèles est de conserver la
fonctionnalité des voies de signalisation cellulaire. Cette
caractéristique est souvent perdue par les modèles
cellulaires tumoraux lors de multiples passages in vitro
oùde nouvellesaltérationsgénétiquespeuventapparaître.
Les PDX sont donc de plus en plus utilisées pour le criblage
de nouvelles molécules dans différentes indications,
comme les PDX pulmonaires, mammaires, prostatiques
et pédiatriques, et bien sûr en fonction des altérations
génétiques d’intérêt [17-20]. En revanche, la réponse
thérapeutique d’une seule PDX à un agent anticancéreux
peut être difficilement extrapolée à la réponse de cet agent
en clinique humaine. Par exemple, sur un panel de PDX
colorectales développées dans le cadre du consortium
CReMEC, la présence d’une mutation de KRAS n’est pas
systématiquement reliée à une absence de réponse au
cétuximab. En revanche, la réponse de l’ensemble des
modèles au cétuximab est significativement corrélée à
l’absence d’une mutation de KRAS [8, 21]. Sur la base de ce
type de résultats, des criblages à haut débit évaluent la
réponse des agents en fonction du génotype tumoral en
utilisant une approche 1 11, c’est-à-dire un animal par
modèle par traitement, ce qui permet à la fois d’évaluer la
réponse thérapeutique d’un grand nombre de modèles
tout en limitant l’utilisation d’un trop grand nombre
d’animaux [22]. La génération de panels de PDX dans
plusieurs indications est une aventure longue et coûteuse,
d’où l’initiative de regrouper les banques existantes,
comme proposé par le consortium EurOPDX [23].Les
PDX sont des outils précieux pour la découverte de
biomarqueurs utilisables ensuite en clinique humaine.
Elles permettent de définir les relations en pharmacociné-
tique (PK) de l’agent anticancéreux et la réponse à cette
thérapie, soit la pharmacodynamie (PD) de cet agent.
Ces relations PK/PD sont importantes pour optimiser le
schéma d’administration de cet agent et orienter le
protocole des études cliniques précoces.
« Les PDX sont précieuses
en recherche translationnelle »
Dans le contexte de la médecine de précision, les PDX
peuvent être également utilisées comme « avatars » de la
tumeur du patient [24]. Cette stratégie consiste à identifier
des biomarqueurs plasmatiques et à caractériser la tumeur
du patient afind’identifier des thérapies sélectionnables
en fonction des altérations génétiques. Ces thérapies
peuvent être ensuite testées sur la PDX générée à partir
de la tumeur du patient, soit en agent seul, soit en
combinaison avec d’autres thérapies anticancéreuses, et
permettre ainsi une orientation de la stratégie thérapeu-
tique pour ce patient [25]. En revanche, cettestratégie a des
limites. Comme nous l’avons indiqué précédemment, le
taux de prise des PDX est très variable et parfois très faible
dans certaines indications tumorales. De plus, la génération
d’une PDX peut être très longue et trop tardive pour
orienter le choix thérapeutique du patient [26].Deplus,
si le patient a reçu pendant l’établissement de son avatar
une thérapie pour laquelle sa tumeur a développé une
résistance, la PDX de la tumeur d’origine ne correspondra
plus à celle qui aura acquis cette résistance. Il faudra donc
générer une nouvelle PDX pour étudier les mécanismes de
résistance et la réponse à d’autres thérapies.
Enfin, l’évaluation de thérapies impliquant la réponse de
l’environnement tumoral est fortement limitée en absence
d’un micro-environnement humanisé. Cela est plus parti-
culièrement critique pour les thérapies impliquant une
réponse immunitaire, la PDX étant greffée dans un hôte
immunodéprimé. Des stratégies d’humanisation de l’hôte
sont en cours de développement [27, 28]. Cela devrait
permettre prochainement de reconstituer, dans des souris
immunodéprimées, le système immunitaire du patient à
Les tumeurs dérivées de patients : un ancien concept redevenu populaire dans la recherche translationnelle en oncologie
Innovations & Thérapeutiques en Oncologie lvol. 2 –n81, janv-fév 2016 47
Passerelle translationnelle PT
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.
 6
6
1
/
6
100%