CANCER COLORECTAL Généralités Formes non

CANCER COLORECTAL
Généralités
Dr David Malka
Département de Médecine Oncologique
Gustave Roussy
Université Paris Saclay
Villejuif

• Côlon = en amont de la jonction recto-sigmoïdienne
• > 15 cm de la marge anale en rectoscopie
• Au dessus de S3
Définition

Quelle partie du colo-rectum est atteinte ?
Sièges les plus fréquents du cancer :
- Côlon (60%)
• Notamment côlon gauche, particulièrement
la charnière recto-sigmoïdienne
- Rectum (40%)
Mais toutes les parties du côlon et du
rectum peuvent être atteintes
3

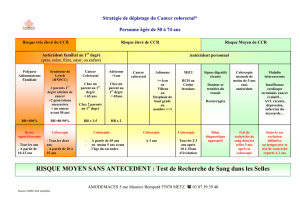
Fréquence des cancers, France, hommes
Nombre de nouveaux cas (2002) Nombre de décès (2004)
-30000 -20000 -10000 0 10000 20000
Prostate
Poumon
Colon et rectum
Bouche, pharynx & larynx
Vessie
Lymphome non hodgkinie
n
Estomac
Œsophage
Foie
Rein
Leucémies
Pancréas
Encéphale
Mélanome
Testicule
Myélome
Thyroïde
Source: IARC 2005 Source INSERM

-40 000 -30 000 -20 000 -10 000 0 10 000
Sein
Colon et
Endomètre
Mélanome
Ovaire
Poumon
Col utérin
Lymphome
Leucémies
Bouche,
Thyroïde
Es tom ac
Rein
Pancréas
Encéphale
Vessie
Myélome
Foie
Oesophage
Hodgkin
Fréquence des cancers, France, femmes
Nombre de nouveaux cas (2002) Nombre de décès (2004)
Source: IARC 2005 Source
INSERM
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
1
/
28
100%