Les pseudohypoparathyroïdies, un spectre de pathologies

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XX - n° 1-2 - janvier-février 2016
12
dossier
dossier
Résistance aux hormones
Les pseudohypoparathyroïdies,
un spectre de pathologies
à reconsidérer d’un œil nouveau
Pseudohypoparathyroidism, a spectrum of pathologies
to look at in a new way
Agnès Linglart1-4, Patrick Hanna1-4, Alessia Usardi1-3
1 Service
d’endocrinologie et
diabétologiepédiatrique,
hôpital Bicêtre Paris-Sud.
2 Centre de référence
des maladies rares du
métabolisme du calcium
et du phosphore et fi lière
santé maladies rares
“OSCAR” (Os-Calcium/
Cartilage-Rein), Paris-Sud.
3 Plateforme d’expertise
maladies rares, hôpital
Bicêtre Paris-Sud.
4 Inserm U1169,
hôpitalBicêtre,
LeKremlin-Bicêtre.
Points forts
Highlights
»
Le terme de pseudohypoparathyroïdie (PHP) regroupe un spectre
de pathologies dont le défaut moléculaire est un élément
de la voie de signalisation du récepteur de la parathormone
(PTH/PTHrP).
»
La classification actuelle des PHP ne reflète ni les bases
moléculaires des pathologies ni l’extrême diversité clinique
des patients.
» L’association de plusieurs résistances à des hormones dont les
récepteurs sont couplés aux protéines G (RCPG) doit faire évoquer
une anomalie de la voie de signalisation RCPG/Gsa/AMPc/PKA.
»
Les ossifi cations ectopiques sous-cutanées sont patho gno-
moniques des mutations de GNAS1.
»
Le diagnostic d’une résistance à la PTH doit faire réaliser une
enquête étiologique moléculaire poussée.
Mots-clés : Pseudohypoparathyroïdie – Empreinte parentale – PTH –
Résistance hormonale – Acrodysostose – GNAS – Méthylation.
T he term of pseudohypoparathyroidism (PHP) indicates a
group of diseases caused by an impairment of the signalling
pathway of the parathyroid hormone receptor (PTH/PTHrP).
The actual PHP classifi cation does not accurately represent neither
the molecular basis nor the clinical diversity of these diseases.
In the presence of several hormonal resistances, involving
receptors coupled with G proteins (GPCRs), one should think
about possible abnormalities of the GPCR/Gsa/cAMP signalling
pathway.
Ectopic ossifi cations are typical features caused by mutations
of the GNAS1 gene.
The discovery of PTH resistance should trigger a molecular
investigation.
Keywords : Pseudohypoparathyroidism – Parental imprinting –
PTH – Hormonal resistance – Acrodysostosis – GNAS –
Methylation.
L
a parathormone (PTH) est une hormone
peptidique dont le rôle essentiel est de maintenir
la calcémie à une concentration située entre 2,20
et 2,65 mmol/l. Les défauts de sécrétion ou d’action
de la PTH ont pour conséquence une hypocalcémie,
une hyperphosphatémie et une augmentation de la
réabsorption tubulaire du phosphate. La PTH agit sur
ses tissus cibles (rein, os) en se liant à son récepteur,
le PTHR1, également dénommé récepteur PTH/
PTHrP. Le PTHR1 appartient à la famille des récepteurs
membranaires à 7 domaines transmembranaires
couplés aux protéines G (RCPG). Il a un deuxième
ligand, le PTHrp (PTH related peptide ), dont la structure
peptidique est proche de celle de la PTH. Il est produit,
entre autres, par les chondrocytes.
Les défauts de signalisation de la PTH sont appelés
“syndromes de résistance à la PTH” ou pseudo-
hypoparathyroïdies (PHP) [1] . En effet, bien que la
PTH endogène soit synthétisée, les patients qui
en souff rent présentent des signes très similaires à
ceux atteints d’hypoparathyroïdie : hypocalcémie,
hyperphosphatémie et augmentation de la
réabsorption tubulaire du phosphate. Cette résistance
à l’action de la PTH est démontrée in vivo par l’absence
de réponse à l’injection de PTH exogène (test à
la PTH) : absence d’élévation de la phosphaturie et
absence d’élévation de l’AMP cyclique (AMPc) urinaire,
produit de l’activation du récepteur de la PTH (2-4).
Les syndromes génétiques de résistance à la PTH sont
donc secondaires à :
0012_MET 12 09/02/2016 14:55:03

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XX - n° 1-2 - janvier-février 2016
13
Les pseudohypoparathyroïdies, un spectre de pathologies à reconsidérer d’un œil nouveau
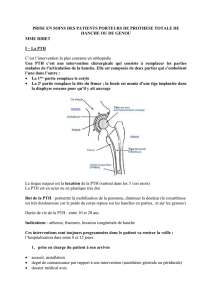
Figure 1. Représentation schématique du locus
GNAS
(qui code pour Gsa) et du gène
STX16
. Les rectangles représentent les exons. Leur localisation supérieure
signifi e une transcription maternelle (Mat) et leur localisation inférieure indique une transcription paternelle (Pat). L’initiation de cette transcription est symbolisée
par une fl èche. Les parenthèses indiquent les limites des délétions identifi ées chez des patients atteints de PHP1B.
GNASSTX16
Cen : centromère ; tél : télomère ; NESP : NeuroEndocrin Secretory Protein ; AS : antisense ; XL : Extralarge Gsa.
✓ une anomalie du récepteur de la PTH : la chondro-
dysplasie de Blomstrand est une maladie létale due
à une mutation homozygote perte de fonction du gène
codant pour PTHR1 (5)
;
✓
une anomalie de la sous-unité α-stimulatrice des
protéines G (Gsa) caractérisant les PHP de type 1 ;
l’injection de PTH exogène ne produit ni élévation de
l’AMPc ni phosphaturie ; les PHP de type 1 représentent
la grande majorité des patients atteints de PHP ;
✓
les PHP de type 2 pour lesquelles l’injection de PTH
exogène élève l’AMPc urinaire mais ne produit pas de
phosphaturie ; l’anomalie se situe donc en aval du
complexe PTHR1/protéine Gsa (6) .
Nous savons aujourd’hui que les patients atteints de
PHP présentent de nombreux signes cliniques en sus
de leur résistance à l’action de la PTH, et qu’il existe de
très nombreux chevauchements – à la fois cliniques et
moléculaires – entre les diff érents types de PHP. C’est la
caractérisation de ces aspects cliniques, de la réponse
biochimique à l’activation de la voie de signalisation
RCPG/Gsa/AMPc/PKA, puis des anomalies moléculaires
qui permet de reconsidérer aujourd’hui ces maladies
et de nous amener dans un futur proche à proposer
une classifi cation moderne (7) .
Les PHP1 ou PHP par défaut
d’expressionde Gsa
Nous n’aborderons pas la chondrodysplasie de
Blomstrand (OMIM #215045), létale, et non relevante
pour le clinicien.
Toutes les PHP1 sont, à ce jour, liées à des défauts
d’expression de Gsa. La protéine Gsa est codée par
GNAS1 , appartenant au locus GNAS soumis à empreinte
parentale (fi gure 1) . L’empreinte est un mécanisme
épigénétique de régulation de la transcription d’un
gène qui aboutit à la transcription d’un seul des
2 allèles parentaux. La modulation de la transcription
est principalement due à la méthylation diff érentielle
de l’ADN de certains promoteurs. L’expression de Gsa
se fait à partir de l’allèle maternel, uniquement dans
certains tissus, comme le tubule rénal proximal (où est
exprimé PTHR1), la thyroïde, l’hypophyse et les gonades.
Dans les autres tissus, comme les leucocytes, le tissu
adipeux ou les ostéoblastes, Gsa est exprimée à partir
des 2 allèles parentaux (8-10) .
La classifi cation actuelle des PHP1 repose principale-
ment sur leur défaut moléculaire.
PHP1A et PHP1C
La PHP1A (OMIM #103580) est une maladie rare de
transmission autosomique dominante avec empreinte
parentale, forcément héritée par la mère. Elle est due
à une mutation hétérozygote maternelle perte de
fonction de la séquence codante de GNAS1 . Tous les
types de mutations ont été identifi és (faux sens, non
sens, délétions, sites d’épissage alternatifs). La muta-
tion peut avoir été héritée, ou être de novo (survenue
sur l’allèle maternel). Les manifestations cliniques
refl ètent le défaut d’expression de Gsa dans les tissus
en fonction de sa transcription mono- ou biallélique.
Les symptômes peuvent être secondaires à un défaut
de signalisation des RCPG (PTHR1, TSHR, FSHR et LHR)
ou à un défaut biologique propre à Gsa (dans le tissu
adipeux, par exemple).
Dans notre expérience, alors que le défaut moléculaire
a été hérité dans près de 50 % des cas, l’âge moyen au
diagnostic est de 6,5 ans au cours de l’investigation
d’une hypocalcémie (symptôme révélateur le plus
0013_MET 13 09/02/2016 14:55:06

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XX - n° 1-2 - janvier-février 2016
14
dossier
dossier
Résistance aux hormones
Figure 2.
A. Ossifi cations sous-cutanées plantaires, une des possibles manifestations cliniques de la PHP1A.
B. Taux de TSH en fonction des formes de PHP (avec diagnostic moléculaire).
C. Brachydactylie (4e orteil) visible cliniquement.
D. Manifestations radiologiques de la résistance du PTHR1 au PTHrP. D1 et D2. Brachyméta-
carpie qui s’aggrave progressivement au cours de la vie. D3. Canal lombaire étroit. D4. Cols
fémoraux courts.
50
40
30
20
10
0
PHP1A
A
C
D1
D4
D2
D3
B
TSH (mUI/l)
PHP1C PHP1B
fréquent), d’une obésité, d’un retard de croissance,
d’une hypothyroïdie ou d’ossifi cations sous-cutanées
(fi gure 2A) .
Le tableau typique de la résistance à la PTH est constitué
d’une hypocalcémie, d'une hyperphosphatémie, d'un
taux élevé de PTH en l’absence de carence en vitamine D
et d’une insuffi sance rénale (attention, la carence en
vitamine D révèle souvent l’hypocalcémie mais sa
supplémentation ne corrige pas le tableau biochimique).
Cette résistance se développe progressivement au cours
de la vie, débutant initialement par une élévation du
phosphate et de la PTH, suivie par une baisse de la
calcémie puis par des symptômes comme crampes
et convulsions (4) . Chez les patients, l’hypocalcémie
résulte du défaut de production de la 1,25-(OH)
2
vitamine D par le tubule proximal, et donc d’un défaut
d’absorption intestinale du calcium, mais probablement
aussi d’un défaut de réponse du squelette à l’élévation
de la PTH. En revanche, dans le tubule distal rénal,
où l’expression de Gsa est biallélique, la réabsorption
du calcium urinaire PTH-dépendante est probablement
longtemps conservée et contribue à la tolérance
prolongée de la résistance à la PTH. La résistance à la
TSH est – presque – toujours présente dans la PHP1A.
Présente dès la naissance mais exceptionnellement
symptomatique, les chiffres de TSH varient entre
4 et 50 mUI/l au diagnostic. Les valeurs de T4 libre
sont généralement dans les valeurs inférieures de
la normale (4, 11) . La résistance à la TSH peut être
détectée par le programme de dépistage néonatal ;
dans ce cas, il s’agit d’une hypothyroïdie congénitale
avec glande en place, sans goitre, à TSH modérément
élevée (12) . La présence d’une résistance à la TSH a
une très grande valeur pour l’orientation vers un
diagnostic de PHP1A (fi gure 2B) . Les mêmes patients
ont également des résistances au TRH, au GHRH et à
la calcitonine, dont les récepteurs sont couplés aux
protéines G (11, 13) . La cryptorchidie bilatérale est
fréquente chez les garçons (selon notre expérience
clinique) ; un retard à l’âge des premières règles a été
décrit chez les fi lles (14,0 ± 1,9 ans) associé à des taux
de FSH élevés (14) .
La très grande majorité des patients PHP1A présente
une chondrodysplasie appelée ostéodystrophie
héréditaire d’Albright (OHA) qui est la manifestation
clinicoradiologique de la résistance du PTHR1 au PTHrP
(fi gures 2C et 2D) . Les patients présentent :
✓
Une brachydactylie aff ectant toujours au moins le
4
e
rayon, mais parfois tous les doigts ou tous les orteils.
✓ Un canal lombaire étroit.
✓ Des cols fémoraux courts.
✓ Parfois des épiphyses en cône.
0014_MET 14 09/02/2016 14:55:08

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XX - n° 1-2 - janvier-février 2016
15
Les pseudohypoparathyroïdies, un spectre de pathologies à reconsidérer d’un œil nouveau
Comme la résistance à la PTH, l’OHA est absente à la
naissance et se développe progressivement, devenant
évidente à l’approche de la puberté.
Le retard de croissance est un symptôme de la PHP1A.
Dès la naissance, la taille moyenne est de –1DS (dévia-
tion standard), le retard de croissance s’accentuant
au cours de la vie, avec une absence complète de
croissance pubertaire (15) . La taille fi nale est autour
de –3DS (notre série personnelle et [16]) . Ce retard de
croissance résulte de l’action combinée de la résis-
tance au PTHrP, d’une résistance au GHRH présente
chez 70 % des patients et d’une résistance aux gona-
dotrophines (14) .
Les ossifications ectopiques sont un signe spéci-
fique des mutations perte de fonction de GNAS1 .
Elles sont faites d’os matures endochondraux for-
més à partir du derme ou de la graisse sous-cutanée
et progressent vers la profondeur (à l’inverse de la
fibrodysplasie ossifiante). L’obésité a toujours été
associée à la PHP1A ; elle est en fait présente dès la
naissance ; il semble qu’ensuite la prise de poids soit
dramatique dès les premières années de vie et difficile
à contrôler après. Plusieurs mécanismes sont impli-
qués : la résistance aux catécholamines (17) , le défaut
de signalisation de Gsa dans le noyau arqué (17) et
la perte de l’effet lipolytique propre de Gsa dans le
tissu adipeux (18) .
Enfi n, le retard mental reste un aspect totalement in ex-
pliqué de la PHP1A, il touche environ 70 % des patients.
Extrêmement variable dans sa sévérité, aucun élément
prédictif n’a été identifi é à ce jour (pas de relation géno-
type-phénotype ; pas de lien avec l’hypothyroïdie ou
l’hypocalcémie) [19] .
Quid de la PHP1C ? (OMIM # 612462) Elle a été décrite
comme un variant clinique de la PHP1A ; l’expression
clinique et biochimique est similaire mais l’activité
biologique de la protéine Gsa, mesurée dans un
système artifi ciel in vitro, est normale. Aujourd’hui,
nous pouvons considérer cette entité comme un
équivalent de la PHP1A regroupant les patients qui ont
une mutation dans l’exon 13 de GNAS1 ; cette mutation
est associée à cette particularité biochimique observée
in vitro (20) .
Le diagnostic de PHP1A n’est pas toujours évident ;
l’ensemble des symptômes n’est pas toujours présent,
en particulier dans la petite enfance. Les éléments
qui concourront le plus à affi rmer le diagnostic sont,
d’une part, l’association de plusieurs résistances à
des hormones dont les récepteurs sont couplés aux
protéines G, et, d’autre part, la présence des ossifi cations
sous-cutanées, quasi pathognomoniques de ces
mutations.
Pseudo-pseudohypoparathyroïdie (PPHP)
ou OHA isolée ou hétéroplasie osseuse
progressive (HOP)
Les patients atteints de PPHP ont d’abord été identifi és
dans les familles de patients PHP1A. Leur présentation
clinique associe OHA, retard de croissance, en particulier
à la naissance (21) , et ossifi cations sous-cutanées, qui
peuvent parfois être au premier plan (la maladie est
alors appelée HOP) [22] (OMIM #603233) . En revanche,
ils n’ont aucune résistance hormonale. La PPHP est due à
une mutation hétéro zygote paternelle perte de fonction
de la séquence codante de GNAS1 . La mutation peut
avoir été héritée, ou être de novo (survenue sur l’allèle
paternel) [4] .
PHP1B
La PHP1B (OMIM #603233) est une maladie rare due à
une perte de la méthylation, sur l’allèle maternel, du
promoteur A/B du locus GNAS, qui a pour conséquence
un défaut d’expression de Gsa uniquement dans les tis-
sus où l’expression de Gsa est exclusivement maternelle,
comme le tubule rénal proximal et la thyroïde. L’âge
moyen au diagnostic est d’environ 13 ans (un diagnostic
à l’âge adulte n’est pas rare), principalement devant
des symptômes d’hypocalcémie.
La résistance à la PTH est le signe clinique principal,
et, comme pour la PHP1A, se développe progressivement
au cours de la vie. Longtemps considérée comme la
seule résistance hormonale, elle s’accompagne en fait
d’une résistance à la TSH modérée (la T4l est toujours
normale), les chiff res de TSH étant généralement juste
à la limite supérieure de la normale (fi gure 2B) . Un cas
d’hypothyroïdie congénitale diagnostiquée par le
programme de dépistage néonatal qui s’est révélé être
une PHP1B a été récemment publié (23) . De même,
ces patients peuvent présenter quelques-uns des signes
décrits ci-dessus, comme l’obésité, la brachydactylie, les
ossifi cations sous-cutanées (24) . Cependant, ces signes
ne sont jamais majeurs ni présents tous ensemble.
À la naissance, ces patients présentent un excès de
croissance qui est encore inexpliqué (21) ; il semble
que cette hypercroissance se prolonge en post-natal
(données personnelles).
Le diagnostic moléculaire de la PHP1B doit être considéré
comme une stratégie à 2 étapes. Premièrement, il faut
démontrer la perte de méthylation du promoteur A/B de
GNAS . C’est l’élément qui affi rme la patho logie et induit
la perte d’expression de Gsa. Selon les laboratoires, la
technique peut varier (pyroséquençage, MS-MLPA).
Chez environ 80 % des patients porteurs d’une PHP1B,
la modifi cation de la méthylation s’étend également
0015_MET 15 09/02/2016 14:55:09

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XX - n° 1-2 - janvier-février 2016
16
dossier
dossier
Résistance aux hormones
à tous les promoteurs du locus GNAS (fi gure 1, p. 13) .
Lorsque le diagnostic est diffi cile ou douteux avec les
techniques de “routine”, il faut avoir recours à une
méthode quantitative.
Deuxièmement, il faut identifi er la cause moléculaire
de la perte d’empreinte. Ainsi, nous savons qu'environ
20 % des PHP1B qui présentent une perte d’empreinte
restreinte au promoteur A/B sont des cas familiaux
de PHP1B, dont la plupart ont une délétion récurrente
de 3kb qui emporte 3 exons du gène STX16 juste en
amont de GNAS (25) . Cette délétion enlève une région
du génome cruciale pour l’établissement et/ou la
maintenance de la méthylation au promoteur A/B de
GNAS . Quelques autres délétions ont ainsi été identifi ées
dans des familles de PHP1B (fi gure 1, p. 13) [26] . Lorsque
la perte d’empreinte touche l’ensemble du locus GNAS
(environ 80 % des PHP1B), la pathologie est sporadique.
Les erreurs cytogénétiques de type disomie uniparentale
paternelle du chromosome 20 expliquent environ 10 %
de ces cas (27) . Pour les autres, aucune étiologie n’est
connue à ce jour. Nous évoquons l’hypothèse de la
dérégulation d’un facteur agissant en trans, puisqu’un
certain nombre de ces patients (environ 10 %) présentent
des défauts de méthylation sur d’autres loci soumis à
empreinte. Ils définissent une nouvelle pathologie
appelée MLID pour Multilocus Imprinting Defect (28) .
Les PHP2
La défi nition biochimique de la PHP2 est l’absence
de réponse phosphaturique à l’injection de PTH
exogène, alors que l’AMPc s’élève normalement.
Historiquement, ce tableau a été observé chez des
patients qui avaient une résistance isolée à la PTH,
sans aucune anomalie osseuse morphologique, et qui
présentaient une carence très profonde en vitamine D.
Récemment, un autre groupe de patients PHP2 a été
identifi é. Ils présentent le même profi l biochimique
de résistance à la PTH, sans carence en vitamine D, avec
des résistances à d’autres hormones dont les récepteurs
sont des RCPG, et avec une atteinte osseuse majeure
appelée acrodysostose (forme extrême de l’OHA).
La PHP2 est une maladie autosomique dominante
due à des mutations hétérozygotes gain de fonction
de PRKAR1A codant pour la sous-unité régulatrice
de la protéine kinase A (ACRDYS1, OMIM #101800)
ou à des mutations hétérozygotes gain de fonc-
tion de la phospho diestérase PDE4D (ACRDYS2,
OMIM #614613) [29] . Le diagnostic d’acrodysostose est
généralement porté dans la petite enfance devant les
anomalies morphologiques osseuses (fi gure 3) .
C’est la chondrodysplasie (acrodysostose voire acro-
scyphodysplasie) par défaut de signalisation du PTHrP
dans les chondrocytes qui est au premier plan (29) . Elle
associe retards sévères de croissance pré- et post-natal
(–3DS en moyenne), hypoplasie de l’étage moyen de la
face et brachydactylie prononcée touchant le plus souvent
tous les rayons (quelques patients avec mutation de
PRKAR1A ou PDE4D ont été décrits avec une brachydactylie
moins marquée, équivalente à celle de la PHP1A).
Les résistances hormonales, et en particulier la résistance
à la PTH et à la TSH, sont présentes uniquement en cas
de mutation de PRKAR1A . Cependant, chez ces patients,
aucun épisode d’hypocalcémie n’a jamais été décrit
dans la littérature, ni observé après plus de 10 ans de
suivi pour certains patients (selon notre expérience cli-
nique) [30, 31] . Les taux de PTH peuvent être supérieurs
à 100 pg/ml, et il convient de ne pas les aggraver par une
carence en vitamine D associée. De même, la résistance à
la TSH est généralement compensée (la T4l est normale).
La calcitonine peut être élevée (entre 50 et 100 pg/ml).
Figure 3. Brachymétacarpie clinique (A) et radiologique (B) chez une patiente de 9 ans atteinte d’acrodysostose avec mutation
de PRKAR1A. Notez la sévérité de l’atteinte osseuse, les épiphyses en cônes fusionnées avant la puberté.
A B
0016_MET 16 09/02/2016 14:55:13
 6
6
 7
7
1
/
7
100%