Sidérose superficielle du système nerveux central – Superficial

202 | La Lettre du Neurologue • Vol. XIV - nos 6-7 - juin-juillet 2010
MISE AU POINT
péjoratif de la maladie, avec un risque de perte
d’auto nomie et d’état grabataire.
Des troubles vésicaux (dysurie essentiellement)
sont également rapportés dans environ un quart
des cas (2), par atteinte de la moelle et des portions
proximales des racines de la queue de cheval (3).
Les troubles cognitifs ne sont pas rares mais affec-
tent une proportion différente de patients suivant
les séries (1 patient sur 4 dans la série décrite par
l’équipe de J.M. Fearnley en 1995 [2], 1 patient
sur 6 dans la série de l’équipe de N. Kumar publiée
en 2006 [4]) et les mécanismes à l’origine sont
multiples.
Les céphalées affecteraient 14 % des patients (1).
Leur origine et les mécanismes physiopathologiques
sont variés. Il s’agit le plus souvent de céphalées
mises sur le compte d’hémorragies méningées, mais
certaines peuvent également ressembler dans leur
présentation à des céphalées migraineuses. D’autres
sont chroniques et peuvent, soit être en rapport
avec l’étiologie de la sidérose (tumeur cérébrale,
malformation artério-veineuse, etc.), soit compli-
quer l’évolution de la maladie via une hydrocéphalie
occasionnant des céphalées d’hypertension intra-
crânienne.
Des lombalgies sont également signalées, ainsi que
des sciatalgies dans environ 10 % des cas (2). Elles
seraient mises sur le compte du dépôt préférentiel
d’hémosidérine sur les racines de la queue de cheval.
Concernant les paires crâniennes, la VIII
e
est la plus
vulnérable en raison de son long trajet. Les autres,
sans être épargnées, sont néanmoins plus rarement
atteintes.
Il a également été suggéré que l’hémosidérose margi-
nale puisse s’accompagner de parkinsonisme (5).
O.C. Cockerel et P. Rudge rapportaient en 1996 le
cas d’un patient atteint de sidérose qui présentait
une dystonie à type de “crampe de l’écrivain” (6).
L
a sidérose superficielle du système nerveux
central (SSSNC), ou hémosidérose marginale, est
due à l’accumulation d’hémosidérine à la surface
du SNC. Elle est attribuée à des saignements sous-
arachnoïdiens répétés. Si le diagnostic peut parfois
être évoqué sur un tableau clinique associant surdité,
ataxie et syndrome pyramidal, il repose essentielle-
ment sur l’imagerie en résonance magnétique.
Il s’agit d’une affection rare, dont les possibilités
thérapeutiques restent décevantes.
Nous n’aborderons pas dans cette mise au point les
sidéroses focales qui soulèvent d’autres considéra-
tions cliniques et étiologiques.
Signes cliniques
Il est classique de décrire une triade comportant
une surdité de perception, un syndrome cérébel-
leux et une atteinte pyramidale. Néanmoins, la
triade au complet n’est présente que chez 39 %
des patients (1).
La surdité de perception est un critère cardinal de la
maladie. Elle est le plus souvent bilatérale, même si
l’atteinte peut être unilatérale au début, ou asymé-
trique. L’évolution naturelle se fait vers la surdité
complète. Ce sont les fréquences aiguës qui sont
les plus affectées.
L’atteinte cérébelleuse est aussi fréquente que l’at-
teinte auditive. Comme l’atteinte affecte surtout le
vermis, il s’agit d’un syndrome cérébelleux statique
prédominant.
Le syndrome pyramidal est en rapport avec les
dépôts d’hémosidérine le long du tronc cérébral,
ainsi qu’au niveau de la moelle épinière, et concerne
53 % des malades (1).
Ces deux derniers syndromes sont responsables de
troubles de la marche et conditionnent le pronostic
* Service de neurologie, hôpital
Central, CHU de Nancy.
** Service de neuroradiologie, hôpi-
tal Central, CHU de Nancy.
Sidérose superficielle
du système nerveux central
Superficial siderosis of the central nervous system
P.A. Baillot*, X. Ducrocq*, H. Vespignani*, A.L. Derelle**

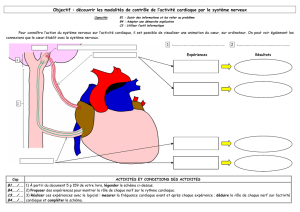
Figure 2. Séquence IRM en pondération
T2* : hyposignal surlignant la région
ponto-mésencéphalique et les régions
paravermiennes supérieures.
Figure 1. Répartition des étiologies de la sidérose
du système nerveux central.
Fréquence (%)
Formes
idiopathiques
Tumeurs
Étiologies
Pathologies
durales
Malformations
vasculaires
Autres
0
10
20
30
40
La Lettre du Neurologue • Vol. XIV - nos 6-7 - juin-juillet 2010 | 203
Points forts
»
La sidérose du système nerveux central est attribuable à des saignements méningés répétés, à l’origine de
dépôts d’hémosidérine ayant des localisations préférentielles. La triade clinique évocatrice du diagnostic associe
surdité de perception, ataxie cérébelleuse et/ou proprioceptive et syndrome pyramidal.
»
Les formes idiopathiques représentent environ 35 % des cas. Les étiologies sont dominées par les pathologies
durales, les tumeurs bénignes du système nerveux central et les malformations vasculaires.
»
Concernant les examens complémentaires, c’est l’imagerie par résonnance magnétique qu’il faut privilégier
et, en particulier, les séquences en T2* qui révèlent des hyposignaux.
»
La chirurgie vise à éradiquer la source du saignement et doit être l’option thérapeutique à privilégier. Les
traitements médicamenteux (chélateurs du fer et corticoïdes principalement) sont d’efficacité très inconstante.
Mots-clés
Hémorragies
méningées
Surdité
Ataxie
Syndrome pyramidal
Des crises d’épilepsie sont signalées, mais elles sont
rares.
Les mécanismes qui en sont à l’origine sont probable-
ment multiples : les séquelles corticales sus-tento-
rielles induites par les dépôts d’hémosidérine, les
hémorragies méningées qui sous-tendent la physio-
pathologie de la maladie ou encore via une ischémie
focale induite par un vasospasme (7).
Étiologies
Elles sont rapportées dans la figure◆1 à partir des
données extraites de l’article de M. Levy et al.
en 2007 (1). Il convient de noter que, dans plus d’un
tiers des cas, il n’est pas retrouvé de cause. Nous
désignons sous le cadre nosologique de pathologies
durales les cavités ectopiques remplies de liquide
céphalo-rachidien (LCR) compliquant, par exemple,
un traumatisme dorsal, ou des lésions de la dure-
mère après une intervention neurochirurgicale.
Examens complémentaires
L’imagerie
N. Kumar de la Mayo Clinic à Rochester a bien décrit
les contributions des différentes techniques d’ima-
gerie dans deux articles récents (8, 9).
L’IRM encéphalique et médullaire permet de poser
le diagnostic avec une excellente sensibilité.
Les dépôts d’hémosidérine apparaissent sous la
forme d’hyposignaux sur les séquences T2 en écho
de gradient, qui sont les séquences de choix pour
porter le diagnostic.
On remarque aussi un hyposignal, mais moins
contrasté sur les séquences T2 pondérées en spin-
écho.
Ces anomalies siègent préférentiellement au niveau
du tronc cérébral, du cervelet, en particulier dans la
portion haute du vermis et la partie antérieure des
hémisphères, de la lame quadrigéminale, le long des
portions initiales de la VIII
e
paire crânienne, mais
aussi autour de la moelle épinière, sans épargner
les structures sus-tentorielles, qui sont toutefois
moins fréquemment concernées, comme le fond
des vallées sylviennes, de l’insula et des faces inféro-
médiales des lobes temporaux, frontaux et occipitaux
(figures◆2◆à◆4).
Les dépôts en rapport avec une hémorragie sous-
arachnoïdienne récente, constitués de méthémo-
globine, peuvent apparaître sous la forme d’un
hypersignal sur les séquences pondérées en T1.
Highlights
» The superficial siderosis of
the central nervous system is
due to repeated meningeal
bleedings, with hemosiderin
deposits which have preferen-
tial locations. The clinical triad
consist of sensorineural hearing
loss, cerebellar and/or propri-
ceptive ataxia and pyramidal
syndrome.
» Idiopathic forms represent
approximately 35% of the
cases. The main etiologies
are dural pathologies, benign
tumors and vascular malfor-
mations.
» Magnetic resonance imaging
is the additional examination to
be privileged. T2* sequences
show hyposignals.
» The surgery is the most effec-
tive treatment. The purpose is
to delete the bleeding’s source.
Iron chelating agents and corti-
coid are of very fickle efficiency.
Keywords
Meningeal bleeding
Deafness
Ataxia
Pyramidal syndrom

Figure 3. Coupe
sagittale en
pondération T1 :
hypersignal qui
circonscrit le
tronc cérébral
et la moelle
cervicale.
Figure 4. Coupe
sagittale en
pondération T2 :
hyposignal surli-
gnant le tronc
cérébral et la
moelle épinière.
Figure 5. Les différentes étapes de la physiopathologie de la maladie.
Extravasation chronique ou intermittente de sang dans les espaces sous-arachnoïdiens
et dissémination dans le LCR
Hémolyse
Hème-oxygénase-1
Lésion du tissu nerveux
Gliose, mort neuronale
Entrée de l’hème dans le tissu exposé
Fer libre HémosidérineConversion hème Ferritine
204 | La Lettre du Neurologue • Vol. XIV - nos 6-7 - juin-juillet 2010
Sidérose superficielle du système nerveux central
MISE AU POINT
L’atrophie du tronc cérébral, du cervelet et de la
moelle est un signe associé fréquent.
Les hypersignaux du parenchyme adjacent peuvent
traduire une réaction gliale qui intervient dans la
physiopathologie de la maladie.
La tomodensitométrie a une faible sensibilité dans
le diagnostic positif. Elle peut révéler une atrophie
aspécifique, en particulier du vermis supérieur et des
portions antérieures des hémisphères cérébelleux.
L’artériographie cérébrale et mé dullaire est peu
efficace quant à la mise en évidence de la source du
saignement. En effet, ce dernier est souvent minime,
intermittent et lent. Ainsi, la réalisation d’une IRM
cérébrale et médullaire paraît indispensable dans le
cadre de la démarche diagnostique, mais l’explora-
tion angiographique est très discutable.
Étude du liquide céphalo-
rachidien
La ponction lombaire constitue le deuxième examen
à privilégier après l’imagerie par résonance magné-
tique. Le LCR est pathologique chez 75 % des
patients (2). Un LCR dépourvu d’anomalie ne doit
donc pas remettre en cause le diagnostic. Les hémor-
ragies sous-arachnoïdiennes répétées peuvent être à
l’origine d’une hyperprotéinorachie en rapport avec
une arachnoïdite. Le LCR est typiquement hémor-
ragique et/ou xanthochromique, et il peut contenir
des érythrophages ou des sidérophages.
Un taux élevé de fer et/ou de ferritine peut être noté,
sans être spécifique de la maladie. En effet, Y. River
et al. rappelaient déjà en 1994 que des taux élevés
peuvent également être en rapport avec des patho-
logies malignes ou inflammatoires du SNC (10).
Ces anomalies ne sont pas permanentes, et il est
licite de renouveler le prélèvement.
On peut également retrouver de façon occasionnelle
un profil mono- ou oligoclonal, dont on ne sait pas
expliquer la physiopathologie.
Physiopathologie
L. Iwanowski et J. Olszewski ont montré en 1960 que
l’on pouvait reproduire une sidérose superficielle en
injectant du sang de façon répétée dans l’espace
sous-arachnoïdien chez des chiens (11).
L’équipe de A.H. Koeppen en 2008 notaient que
5 étapes sont nécessaires pour aboutir à une sidé-
rose du SNC (figure◆5)◆[12].
Pourquoi certaines régions du névraxe
sont-elles plus affectées ?
Plusieurs arguments peuvent être avancés.
➤
Les variations de flux du LCR ne sont pas iden-
tiques en tout point du névraxe. Ainsi, des études
ont montré que les convexités du tronc cérébral et
du cervelet étaient le siège d’un contact continuel-
lement renouvelé du LCR (12).

MISE AU POINT
➤
Des raisons histologiques et histochimiques sont
à évoquer : la glie de Bergmann du cervelet aurait une
grande capacité de synthèse de l’hème-oxygénase-1
ou une susceptibilité excessive à la transcription du
gène de l’hème-oxygénase-1.
➤
L’action de la pesanteur : ce sont les régions
déclives qui sont le plus souvent touchées.
La transformation du fer en ferritine a initialement
un rôle protecteur. En effet, le fer libre peut engen-
drer une peroxydation lipidique à l’origine d’une
dysfonction membranaire et d’une mort cellulaire.
En temps normal, la ferritine est synthétisée sous
la forme d’unités lourdes.
Mais, en cas d’exposition persistante au fer libre,
des sous-unités légères sont préférentiellement
produites. Or, elles sont les premiers constituants
des dépôts d’hémosidérine.
Concernant les sidéroses qui se sont développées à
partir de défects duraux, la source du saignement
pourrait être double d’après N. Kumar et al. (13).
Tout d’abord, les cavités ectopiques du LCR sont
constituées de vaisseaux friables, qui sont potentiel-
lement à l’origine de saignements répétés. D’autre
part, en générant une hypotension du LCR, ces
cavités pourraient entraîner un engorgement des
veines intradurales et épidurales, et provoquer ainsi
une extravasation d’hématies.
Traitements
Les traitements médicamenteux
Aucun de ces traitements, objets uniquement
d’utilisations ponctuelles, n’a fait la preuve de son
efficacité.
◆◆Les◆chélateurs◆du◆fer
La déféroxamine et la triéthylène tétramine sont
d’efficacité inconstante.
◆◆Les◆corticoïdes
La littérature ne rapporte que 2 cas d’amélioration
liée à la prise de corticoïdes (14, 15). Tout d’abord,
un patient chez lequel il a été mis en évidence des
anticorps anti-Ri fortements positifs, dont les symp-
tômes seraient peut-être au moins en partie liés à un
syndrome paranéoplasique possiblement amélioré
par la corticothérapie. Il était noté plusieurs atypies
cliniques chez l’autre patiente, et l’on peut s’inter-
roger sur l’existence d’une pathologie associée à la
sidérose superficielle qui aurait pu également être
améliorée par les corticoïdes.
◆◆Les◆anti-oxydants
La destruction des couches superficielles du cortex
pourrait être en rapport avec la production de radi-
caux libres. Des anti-oxydants tels que la vitamine C,
la vitamine E, la sélégiline et des IMAO-B ont donc
été employés. Mais il n’y a pas assez de cas rapportés
pour juger de leur efficacité.
◆◆Les◆inhibiteurs◆de◆l’hème-oxygénase-1
Il s’agit de certaines protoporphyrines. La principale
difficulté tient au fait qu’elles ne sont pas capables
de traverser la barrière hémato-encéphalique. Elles
ne sont donc pas employées en pratique courante.
Chirurgie
Traiter la source du saignement est probablement
l’approche la plus efficace. Pour J.M. Fearnley et al.,
elle ne permet pas d’amélioration, mais elle vise à
empêcher l’aggravation de la maladie (2).
Certaines séries, avec un nombre restreint de
patients et un recul de quelques mois, signalent
une amélioration clinique après chirurgie (16).
M.O. McCarron et V.H. Patterson ont émis l’hypothèse,
en 2004, qu’en réalisant un shunt du LCR, on pouvait
en diminuer la concentration de sang en le “diluant”,
et ainsi ralentir la progression de la maladie (17). ■
1.◆Levy M, Turtzo C, Llinas RH. Superficial siderosis: a case
report and review of the literature. Nature clinical practice
neurology 2007;3:54-8.
2.◆Fearnley JM, Stevens JM, Rudge P. Superficial siderosis
of the central nervous system. Brain 1995;118:1051-66.
3.◆Straube A, Dudel C, Wekerle G, Klopstock T. Polyradi-
culopathy in the course of superficial siderosis of the CNS.
J Neurol 2001;248:63-4.
4.◆Kumar N, Cohen-Gadol AA, Wright RA, Miller GM,
Piepgras DG, Ahlskog JE. Superficial siderosis. Neurology
2006;66:1144-52.
5.◆Rieder CRM, Perruzo dos Santos Souza M, Maciel de Freitas
R, Fricke D. Superficial siderosis of the central nervous system
associated with parkinsonism. Parkinsonism and Related
Disorders 2004;10:443-5.
6.◆Cockerell OC, Rudge P. Focal dystonia secondary to
superficial siderosis. Movement Disorders 1996;11:452-3.
7.◆Iannaccone S, Golzi V, Sferrazza B, de Rino F, Smirne S,
Ferini-Strambi L. Central nervous system superficial side-
rosis, headache, and epilepsy. Headache 1999;39:666-9.
8.◆Kumar N. Superficial siderosis: associations and thera-
peutic implications. Arch Neurol 2007;64:491-6.
9.◆Kumar N. Neuroimaging in superficial siderosis: an
in-depth look. AJNR Am J Neuroradiol 2010; 31:5-14.
10.◆River Y, Honigman S, Gomori JM, Reches A. Superficial
hemosiderosis of the central nervous system. Movement
Disorders 1994;9:559-62.
11.◆Iwanowski L, Olszewski J. The effects of subarachnoid
injections of iron-containing substances on the central
nervous system. J Neuropathol Exp Neurol 1960;19:
433-48.
12.◆Koeppen AH, Michael SC, Li D et al. The pathology of
superficial siderosis of the central nervous system. Acta
Neuropathol 2008;116: 371-82.
13.◆Kumar N, McKeon A, Rabinstein AA et al. Superficial
siderosis and csf hypovolemia: the defect (dural) in the link.
Neurology 2007; 69:925-6.
14.◆ Angstwurm K, Schielke E, Zimmer C, Kivelitz D, Weber JR.
Superficial siderosis of the central nervous system: response
to steroid therapy. J Neurol 2002;249:1223-5.
15.◆Le Rhun E, Soto Ares G, Pécheux N, Destée A, Defebvre L.
Hémosidérose marginale du névraxe d’évolution favorable
sous corticoïdes. Rev Neurol 2008;164:264-70.
16.◆Lévêque M, Mc Laughlin N, Bojanowski MW. Sidérose
superficielle du système nerveux central : à propos de trois
cas et revue de la littérature. Neurochirurgie 2009;55:
315-21.
17.◆McCarron MO, Patterson VH. Effects of shunting CSF
in superficial siderosis of the CNS. Neurology 2004; 62:
1022-3.
Références bibliographiques
1
/
4
100%