Aucun titre de diapositive

G.Bertoni 1
NV3 – Transport et mobilité des éléments minéraux dans la plante
G. Bertoni

G.Bertoni 2

G.Bertoni 3 3
Le transport et la mobilité des éléments
1. Racine
2. Tige: sève du xylème, sève du phloème
3. Les éléments non mobiles
4. Les éléments mobiles
5. Un système coordonné: exemple de l’azote

G.Bertoni 4 G.Bertoni 4
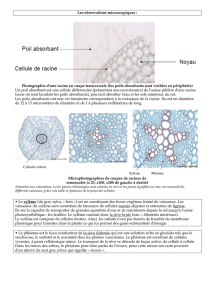
1. le transport dans la racine
Cellule de
l’endoderme
avec cadre
de Caspari
Modèle simplifié de la racine
Cellule de
l’épiderme avec
site
d’absorption
Cellule du
parenchyme
de la stèle
Ca, Fe et Al absorbés par l’extrêmité des racines, dont l’endoderme n’est pas
encore différencié (à relier avec les valeurs données pour l’interception)
Les pompes ioniques entretiennent le gradient de pression osmotique qui
recharge la plante en eau, au printemps et chaque nuit: la poussée racinaire
Sève brute
- 0.03 MPa
Solution du
sol - 0.01 MPa

G.Bertoni 5 G.Bertoni 5
2. La composition des sèves du xylème (sève brute montante) et du phloème (
sève élaborée ( montante et descendante) en meq / L pour les ions et mmoles / L
pour les molécules organiques d’après Mengel et Kirkby (1987)
Xylème Phloème
Saccharose 0 250 - 300
acides aminés 0 35
Acides organiques 15 – 25
ATP 0.5
nitrate 25 - 30 0
phosphates 0.4 7 - 11
potassium 15 - 25 60 - 110
magnésium 3 - 5 9 - 10
chlorures 1 - 1.5 10 - 20
sulfates 3 – 5 < 1
calcium 10 - 15 . 0
pH 6.5 8.0
(Mpa) - 0.03 - 1.5
Microéléments Fe, Cu, Zn, x
Mn, Mo, B x
Hormones ABA, AIA, Gibberellin
cytokinines cytokinines
Mobilité des éléments
↓
Symptômes, Analyses
TDNV2, TDNV3
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
1
/
49
100%