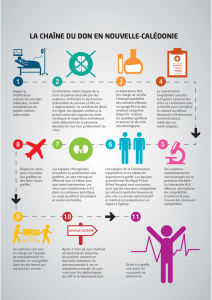
Rôle du laboratoire en cas de suspicion d`incidents

Rôle du Laboratoire en cas de suspicion
Rôle
du
Laboratoire
en
cas
de
suspicion
d’IncidentTransfusionnel
DrOlivierBouix
EtablissementFrançaisduSang
P
y
rénées‐Méditerranée ‐Nîmes
DrChristineLinget
CentreHospitalier
Salon‐de‐Provence
y

Moyen
age
Moyen
age

17
ème
siècle
17
ème
siècle

1913
1913

DéfinitionDéfinition
EffetIndésirableReceveur:
Survenued’uneréactionnocivechezunpatient,liéeoususceptible
d’êtreliéeàl’administrationd’unproduitsanguinlabile(PSL)
Si l t
t
dé l ti bli t i
Si
gna
l
emen
t
e
t
dé
c
l
ara
ti
ono
bli
ga
t
o
i
re
Toutprofessionneldesantéquiconstateunévénementindésirable
ibl d’ê dû à
l’ d i i i d’
PSL dél i d 8 h
suscept
ibl
e
d’ê
tre
dû
à
l’
a
d
m
i
n
i
strat
i
on
d’
un
PSL
aun
dél
a
i
d
e
8
h
eures
pourlesignaleraucorrespondantd’hémovigilancedel’ES
CL
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
1
/
42
100%