Place des médicaments et de l`électricité de ectricité

FORMATION CONTINUE
Le traitement moderne de l'insuffi sance cardiaque comprend
l’association de plusieurs médicaments et, en fonction des in-
dications, l’implantation d’une resynchronisation cardiaque,
associée ou non à un défi brillateur cardiaque. Ces thérapies
sont complémentaires et leurs effets bénéfi ques en terme
d’amélioration des symptômes, diminution de la morbidité et
de la mortalité s’additionnent.
En Suisse, plus de 150’000 personnes sou rent d’insu sance car-
diaque (IC) chronique. Jusqu’à 15% des sujets de plus de 80ans
en sont atteints et il s’agit de la première cause d’hospitalisation
chez les personnes de plus de 65 ans. L’IC est la seule a ection car-
diovasculaire, avec la brillation auriculaire, dont l’incidence
continue d’augmenter dans les pays occidentaux industrialisés.
Deux phénomènes principaux expliquent cette tendance : le vieil-
lissement de la population et l’amélioration générale des traitements
des cardiopathies menant à l’IC, telles que la maladie coronarienne.
La prise en charge de l’IC à fraction d’éjection ventriculaire
gauche (FEVG) diminuée associe un ensemble de mesures non
pharmacologiques (par exemple la réadaptation cardiaque), phar-
macologiques, et une resynchronisation électrique du cœur (éven-
tuellement associée à un dé brillateur). Le but de cet article est de
proposer un tour d’horizon de ces thérapies et de leurs indications.
Défi nition
Selon les dernières directives de la société européenne de cardiolo-
gie (1), la dé nition actuelle de l’IC est la suivante :
un syndrome clinique dans lequel les patients présentent chacune
des trois caractéristiques :
1. des symptômes typiques IC, tels que dyspnée de repos ou à l’ef-
fort, fatigue, oedèmes des membres inférieurs ;
Insuffi sance cardiaque
Place des médicaments et de l’électricité
2. des signes cliniques d’IC, tels que tachycardie, tachypnée, râles
pulmonaires, turgescence jugulaire, oedèmes périphériques, hé-
patomégalie ;
3. des évidences objectives d’une anomalie structurelle ou fonc-
tionnelle cardiaque, telles que cardiomégalie, anomalies à
l’échocardiographie, élévation du peptide natriurétique.
Le diagnostic d’IC en soi n’est pas su sant, et un bilan étiolo-
gique doit être entrepris, car certaines causes peuvent être corri-
gées ou nécessiter un traitement spéci que. Les étiologies les plus
fréquentes sont : la maladie coronarienne (70% des cas d’IC), les
atteintes valvulaires (10%) ou les cardiomyopathies (10%). La prise
en charge comprend :
l la correction des facteurs systémiques aggravants (troubles thy-
roïdiens, diabète, infection),
l les modi cations du style de vie (arrêt du tabac, diminution de
la consommation d’alcool, restriction des apports en sel, perte
de poids si IMC >30 kg/m2),
l l’éviction de certains médicaments potentiellement délétères
(anti-in ammatoires non stéroïdiens, bloquants des canaux cal-
ciques, glitazones),
l la vaccination contre le pneumocoque et la grippe,
l un traitement médicamenteux et, chez des patients sélectionnés,
l’implantation d’un pacemaker de resynchronisation cardiaque
(éventuellement associé à un dé brillateur) dont le but
est d’une part d’améliorer les symptômes et d’autre
part de prolonger la survie.
Traitement pharmacologique
Le traitement pharmacologique de l’IC, autrefois
limité aux diurétiques et à la digoxine a largement
évolué, sur la base de nombreuses études cliniques (1),
avec l’addition des inhibiteurs de l’enzyme de conver-
sion (IEC), des bêta-bloquants, des antagonistes du
récepteur aux minéralocorticoïdes et des bloqueurs
des récepteurs de l’angiotensine II (ARA ou sartans).
Le tableau 1 récapitule ces di érentes molécules et leur
posologie.
Inhibiteurs de l’enzyme de conversion (IEC). En
l’absence de contre-indication ou d’intolérance, un
IEC devrait être introduit chez tous les patients avec
une IC et une FEVG diminuée. Un traitement d’IEC
améliore la fonction cardiaque, diminue les symp-
tômes et le nombre d’hospitalisations pour IC décom-
Dr méd. David Senouf
Genève
TAB. 1
Dosages des médicaments les plus fréquents dans l'insuffi sance
cardiaque
Dose initiale (mg) Dose cible (mg)
IEC* Captopril 6,25 (3 fois par jour) 50–100 (3 fois par jour)
Enalapril 2,5 (2 fois par jour) 10–20 (2 fois par jour)
Lisinopril 2,5 à 5 (1 fois par jour) 20–35 (1 fois par jour)
Ramipril 2,5 (1 fois par jour) 5 (2 fois par jour)
Sartans Candesartan 4 à 8 (1 fois par jour) 32 (1 fois par jour)
Valsartan 40 (2 fois par jour) 160 (2 fois par jour)
ARM** Eplerenone 25 (1 fois par jour) 50 (1 fois par jour)
Spironolactone 25 (1 fois par jour) 25–50 (1 fois par jour)
Bêta-bloquants Bisoprolol 1,25 (1 fois par jour) 10 (1 fois par jour)
Carvedilol 3,125 (2 fois par jour) 25–50 (2 fois par jour)
Metoprolol 12,5 à 25 (1 fois par jour) 200 (1 fois par jour)
Nebivolol 1,25 (1 fois par jour) 10 (1 fois par jour)
* Inhibiteur de l’enzyme de conversion
** Antagonistes du récepteurs aux minéralocorticoïdes
enne.
ulaire
es non
),
fr
atteint
en charge c
la correction des fac
iens, diabète,
catio
mma
si
ignes cliniques d
monaires, turgescence j
omé
. des évidences objectives d’une anomal
tionnelle cardiaque, telles que car
l’échocardiographie, élévation du p
e diagnostic d’IC en soi n’est p
être entrepris, car ce
ter un traitemen
maladie
0%)
aux
e tendan
érale de
de
cardie
me
ectricité
méd. David Senouf
Captopril
Enalapril
2,5
Lisin
2,5 à 5 (1
R
2,5 (1 fois par jo
Ca
8 (1 fois par jo
Valsa
par jo
RM**
Eplerenone
Spironolactone
êta-b
prolol
1,25
3,12
12
iteur de l’enzyme
stes du récepteu
els que
membres
médicaments les plus fréquents da
se initiale (mg)
Dos
ois par jour)
5
jour)
ur)
leurs indication
é européenne de cardiolo-
la suivant
patients présen
e de repos ou à l’ef-
l
l
(a
c
l
l
l
6 02
_ 2012 _ info@gériatrie

FORMATION CONTINUE
pensée et augmente la survie (réduction relative du risque jusqu’à
27% selon les études). Les contre-indications sont un antécédent
d’angioedème, une sténose bilatérale des artères rénales, un potas-
sium sérique >5,0mmol/l, une insu sance rénale avec une créati-
nine sérique >220 μmol/l, une sténose aortique sévère. La fonction
rénale et les électrolytes doivent être surveillés régulièrement. Les
IEC indiqués dans l’IC sont présentés ci-dessous, leur posologie
doit être débutée à faible dose et majorée progressivement, jusqu’à
la dose cible en fonction de la tolérance. En cas de toux sèche, on
les remplace par un sartan.
Bêta-bloquants. Un bêta-bloquant devrait être introduit, autant
que possible, chez tous les patients avec une IC et une FEVG dimi-
nuée, avec les même e ets béné ques que les IEC. Trois études cli-
niques majeures, totalisant plus de 9000 patients ont montré une
réduction de la mortalité (diminution du risque relatif de 34%) et
du nombre d’hospitalisations pour IC décompensée dans
l’année suivant l’introduction du traitement (diminution
du risque relatif entre 26% et 38%). Comme pour les IEC,
les bêta-bloquants doivent être débutés à faible dose, puis
majorés progressivement jusqu’à la dose cible. Chaque
deux à quatre semaines, la dose peut être doublée, en l’ab-
sence d’aggravation clinique. Les contre-indications sont
l’asthme – la bronchite chronique obstructive ne l’est pas
– et un bloc de conduction atrio-ventriculaire de haut
degré.
Antagonistes du récepteur aux minéralocorticoïdes
(ARM). Les directives internationales ont jusqu’à pré-
sent recommandé l’utilisation de la spironolactone
ou de l'éplérénone chez les patients présentant une IC
sévère, de stade New York Heart Association (NYHA)
III-IV et une FEVG ≤35%. Une étude clinique randomi-
sée récente (2) a enrôlé des patients en stade NYHA II,
avec une dysfonction ventriculaire gauche systolique, qui
ont reçu de l’éplérénone versus un placebo. Les auteurs
rapportent une nette diminution du taux de décès et
d’hospitalisations par rapport au placebo. On peut donc
recommander les antagonistes du récepteur aux minéra-
locorticoïdes pour tous les patients symptomatiques (dès
la classe NYHA II) avec une FEVG ≤35%. De nombreux
cliniciens recommandent d’utiliser la spironolactone en
première intention et de la remplacer par l’éplérénone en
cas d’e ets indésirables tels que gynécomastie ou masto-
dynie. Le risque d’hyperkaliémie est faible et identique
pour ces deux molécules. La fonction rénale et les élec-
trolytes doivent être contrôlés 1 et 4 semaines après l’ins-
tauration du traitement, puis à 1, 2, 3 et chaque 6 mois.
Bloqueurs des récepteurs de l’angiotensine II (ARA
ou sartans). Ils sont recommandés en cas d’intolérance
aux IEC. Ils peuvent être introduits en combinaison chez
les patients qui restent symptomatiques malgré un trai-
tement par IEC et bêta-bloqueur. A relever que la triple
inhibition du système rénine-angiotensine-aldostérone
par IEC, ARA et ARM n’est pas recommandée en raison
des risques d’hyperkaliémie.
Digoxine. Chez les patients IC en brillation auriculaire,
elle peut être utilisée pour contrôlée la fréquence car-
diaque, conjointement avec un bêta-bloquant. Chez les
patients en rythme sinusal, elle améliore les symptômes
et diminue le nombre d’hospitalisations, sans e et béné que sur
la mortalité. Les taux sériques devraient être compris entre 0,6
et 1,2 ng/ml (l’amiodarone, le diltiazem, certains antibiotiques
peuvent augmenter la digoxinémie). Il faut prêter attention aux
e ets indésirables potentiels et signes de surdosage (majorés par
l’hypokaliémie), tels que blocs de conduction, arythmies atriales
et ventriculaires, confusion, nausées, troubles de la vision des cou-
leurs (xanthopsie).
L’ivabradine est une molécule agissant sur le noeud sinusal et
permettant une diminution de la fréquence cardiaque, sans autre
e et cardiovasculaire apparent. Dans l’essai clinique randomisé
SHIFT (3), des patients en stade NYHA II-IV l’ont reçue en plus
d’un traitement optimal avec comme résultat principal une dimi-
nution du nombre d’hospitalisations. Cette molécule doit donc
être considérée chez des patients demeurant symptomatiques
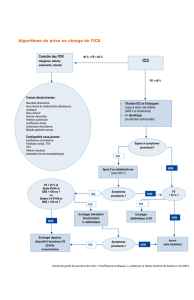
FIG. 1 Algorithme de prise en charge de l'IC*
Rythme sinusal et FC ≥70 bpm ?
diurétiques pour soulager les symptômes/des signes de congestion
IEC (ou ARB non tolérés)
AJOUTER un bêta-bloquant
encore en classe NYHA II-IV ?
AJOUTER un ARM
encore en classe NYHA II-IV ?
FEVG ≤35% ?
AJOUTER l'ivabradine
encore en classe NYHA II-IV et FEVG ≤35% ?
QRS ≥120 ms
encore en classe NYHA II-IV ?
considérer CRT-P/CRT-D considérer défibrillateur
poursuite du traitement
considérer la digoxine et
en phase terminale les
assistances ventriculaires
ou la transplantation
non
oui
oui
oui
oui
oui
oui
oui
non
non
non
non
non
non
AJOUT
ore e
dérée ch
rithme de prise en charge de
ques pour soulager les symptômes/des signes
IEC (ou ARB non tolérés)
TER un bêta-bloq
se NY
e, en l
ations so
ne l’est p
nter la
ables pote
mie)
aires, confusion, n
hopsie).
ine est une mol
diminution
ire apparent. D
atients en stade NYH
ptimal avec comme résultat principa
ions. Cette molécu
emeurant sy
sans e et béné qu
ient être compris entre 0
azem, certains antibiotiques
e). Il faut prêter attention aux
nes de surdosage (majorés par
conduction, arythmies atriales
, troubles de la vision des cou-
ant sur le noeud sinusal et
cardiaque, sans a
yp
molécules. La fo
nt être contrôlés 1 et 4
traitement, puis à 1, 2, 3 et c
es récepteurs de l’angiotensin
ls sont recommandés en cas d’int
EC. Ils peuvent être introduits en combin
patients qui restent sy
ment par IEC et bêta-bloqu
hibition du système rénine-ang
par IEC, ARA et ARM n’est pas reco
des risques d’hyperkaliémie.
Digoxine
. Che
e peut être utili
conjointement a
ythme sinusa
p
u récep
ients sym
e FEVG ≤35%. De nom
d’utiliser la spironolac
a remplacer par l’éplérénone en
ue gynécomastie ou masto-
est faible et identique
rénale et les élec-
s après l’in
mo
NYHA)
e randomi-
ade NYHA
e systoliq
acebo. Le
taux de décè
On peut donc
x minéra-
(dès
info@gériatrie
_ 02 _ 2012 7

malgré le traitement précité, en rythme sinusal à une fréquence
≥70bpm et dont la FEVG est ≤35%.
Diurétiques. Ils améliorent les symptômes de congestion pul-
monaire et les oedèmes périphériques. Ils devraient toujours être
utilisés en association avec un IEC, car ils activent le système
rénine-angiotensine-aldostérone. Leur posologie doit être ajustée
en fonction de la réponse clinique (ne pas hésiter à en diminuer le
dosage, voire les interrompre en l’absence de signes de surcharge).
Un thiazide peut être utile en supplément du diurétique de l’anse
en cas d’oedèmes réfractaires.
Molécules en cours d’investigation. L’aliskiren est un inhibi-
teur direct de la rénine. Jusqu’à présent, il a montré un e et neu-
ro-hormonal positif dans l’insu sance cardiaque (diminution du
NT-proBNP), mais les évidences d’un béné ce clinique manquent
encore pour justi er sa prescription dans cette indication. D’autres
études sont en cours.
Défi brillateurs cardiaques implantables
et resynchronisation cardiaque
Ces appareils ont révolutionné le traitement des patients avec une
IC chronique et font partie du traitement moderne standard de
l’IC. La gure 1 propose un algorithme de prise en charge de l’IC à
dysfonction systolique associant médicaments et thérapies « élec-
triques ».
1. Resynchronisation cardiaque
La resynchronisation cardiaque est basée sur la constatation qu’il
existe fréquemment des anomalies de la conduction électrique
chez les patients insu sants cardiaques (notamment un bloc de
branche gauche). Ceci crée un asynchronisme mécanique à dif-
férents niveaux (inter-atrial, atrio-ventriculaire et inter-ventri-
culaire), et donc une contraction moins e cace. En plaçant une
sonde au niveau du ventricule gauche via le sinus coronaire (ain-
si que dans le ventricule droit et l’oreillette), on peut ainsi exer-
cer une stimulation bi-ventriculaire et corriger cet asynchronisme.
Les indications actuelles à l’implantation d’une resynchroni-
sation cardiaque (CRT-P) sont basées sur plusieurs études ayant
montré un béné ce en terme :
l d’amélioration des symptômes et de la qualité de vie,
l de diminution de la morbidité et du nombre d’hospitalisations
l de diminution de la mortalité.
Un peu plus de dix ans après son introduction clinique, la resyn-
chronisation cardiaque est un des traitements les plus e caces
avec les IEC, les bêta-bloquants et les antagonistes du récepteur
aux minéralocorticoïdes.
Une méta-analyse parue dans le JAMA en 2007 montre une
diminution de 27% du risque relatif d’hospitalisation pour IC
décompensée chez les patients appareillés avec une resynchronisa-
tion. L’étude CARE-HF, publiée en 2005, a permis l’envol de cette
thérapie, puisque les auteurs ont montré une diminution de 36%
du risque de décès (persistant trois ans post-implantation) chez
des patients implantés avec un CRT-P, avec une FEVG <35%, en
classe NYHA III et IV et présentant une largeur de QRS >120 ms.
Les études suivantes (REVERSE, MADIT-CRT, RAFT) se sont
intéressés aux patients moins sévèrement atteints (NYHA II), et
ont mis en évidence une diminution substantielle de la morbidi-
té et de la mortalité, surtout chez les patients avec une durée du
QRS >150 ms.
La stratégie actuelle est donc de proposer une resynchronisa-
tion cardiaque plus tôt dans le cours de la maladie, déjà chez des
patients peu symptomatiques. On peut résumer ainsi les critères
d’implantation :
l patients en classe NYHA III et IV avec FEVG ≤35%, QRS ≥120
ms avec morphologie de bloc de branche gauche (BBG);
l patients en classe NYHA II avec FEVG ≤30%, QRS ≥130 ms avec
morphologie de BBG.
Le choix d’implanter une resynchronisation seule ou associée à un
dé brillateur est toujours débattu dans la littérature, et doit être
discuté avec le patient (et sa famille). Le dé brillateur permet un
gain supplémentaire en terme de réduction de la mort subite.
Même au sein d’une population gériatrique, si les patients ont
une espérance de vie de plus d’une année avec une bonne capa-
cité fonctionnelle, il ne faut pas hésiter à proposer l’implantation
d’une resynchronisation cardiaque (si l’indication est bien posée),
compte tenu du béné ce immédiat en terme de symptôme et de
qualité de vie.
2. Défi brillateurs implantables
Les premiers dé brillateurs ont été implantés de manière presque
expérimentale au 1980 chez des patients à très haut risque de mort
subite, en prévention secondaire, et font maintenant partie de la
prise en charge standard de tout patient avec une FEVG sévère-
ment diminuée. Ils diminuent le risque de mort subite et d’arythmie
dangereuse, mais n’ont pas d’e et sur sur la structure et la fonction
cardiaque. Ils sont indiqués, en prévention de la mort subite, chez
tous les patients avec une FEVG sévèrement diminuée, sous réserve
d’une espérance de vie raisonnable. Resynchronisation cardiaque et
dé brillateur peuvent être associés (ou non) dans le même appareil.
Dr méd. David Senouf
Cardiologue FMH
Rue Charles-Galland 15, 1206 Genève
dr.senouf@bluewin.ch
Dr méd. Philippe Meyer
Service de Cardiologie
Département des spécialités de médecine, Hôpitaux Universitaires Genève
Rue Gabrielle Perret-Gentil 4, 1211 Genève 14
FORMATION CONTINUE
Message à retenir
◆ Le traitement médicamenteux de l’IC associe IEC (sartans en cas
d’intolérance), bêta-bloquants, antagonistes des récepteurs aux
minéralocorticoïdes, leurs posologie doit être majorée progressive-
ment jusqu’à la dose cible.
◆ Les diurétiques améliorent les symptômes de congestion mais
n’offrent pas de bénéfi ce en terme de diminution de mortalité (à la
différence des molécules ci-dessus).
◆ La resynchronisation cardiaque doit être proposée (en complément
du traitement médicamenteux) à tous les patients avec une FEVG
35% et un QRS large, au vu des effets bénéfi ques cliniques immé-
diats et à long terme qu’elle apporte.
◆ La resynchronisation peut être associée à un défi brillateur, permet-
tant une diminution supplémentaire du risque de mort subite, chez
des patients avec une espérance de vie raisonnable.
on
m
danger
cardiaque. I
us les patients avec u
espérance de v
ur peuv
d
onnelle,
esynchronisation
e tenu du béné ce im
é de
2. Défi brillateurs implantables
Les premiers dé brillateurs ont été im
expérimentale au 1980 chez des pat
prévention secondaire
e standard de to
iminuen
pas
iq
derne
e en cha
s et thér
:
n classe NY
mor
en classe NYHA II
ogie de B
mplanter une res
st toujours dé
ient (et sa fam
aire en terme de rédu
d’une population gériatrique, si les
une année avec une
er à proposer
dicatio
me
oser une resynchro
de la maladie, déjà chez d
peut résumer ainsi les critères
V avec FEVG ≤35%, QRS ≥120
branch
EVG ≤30%, QRS ≥130 ms avec
ation seule ou associée à un
littérature, et doit
q
s bêta-bloquan
corticoïdes.
a-analyse parue dans le JA
de 27% du risque relatif d’hos
nsée chez les patients appareillés avec u
L’étude CARE-HF, publiée en 2005, a pe
érapie, puisque les aut
u risque de décès (persistan
es patients implantés avec un CR
classe NYHA III et IV et présentant
Les études suivantes (REVERSE,
intéressés aux
t mis en éviden
e la mortalité, su
s
basées
tômes et de la qualité d
orbidité et du nombre d’
ortalité.
son introduction clinique, la re
s traitements les plus e
antagonistes du
2007
mécanique à di
laire et inter-ventri-
cace. En plaçant une
ia le sinus coronaire (ain-
eillette), o
corriger cet as
tion d’une resy
sieurs études ayant
ons
D
Car
Rue
dr.se
Dr
S
info@gériatrie
_ 02 _ 2012 9
1
/
3
100%