TP génétique n°4 - Sciences de la Vie et de la Terre, Biologie

1
Nom : Prénom : Classe :
TP n°4: des mécanismes de diversification des êtres vivants
Une équipe scientifique internationale estime le nombre d’espèces eucaryotes peuplant la Terre à 8,7 millions
(dont 7,77 espèces animales). La grande majorité de cette richesse spécifique, notamment chez les arthropodes,
n’a pas été décrite ni même découverte. Le brassage génétique, effectué lors de la méiose et la fécondation,
contribue à la diversification du vivant. De même, les mutations sont la source aléatoire de la diversité des allèles,
base de la diversité des espèces et de la variabilité au sein même de ces espèces. Cependant, ces deux phénomènes
biologiques ne suffisent pas à expliquer la grande diversité des organismes présents sur Terre. D’autres
mécanismes, d’origine génétique ou non, permettent cette diversification des êtres vivants.
Problème posé : Quels mécanismes d’origine génétique ou non, permettent de créer une grande diversité
d’espèces, mais aussi d’augmenter la variabilité au sein de celles-ci?
Compétences : (2 séances de TP)
Pratiquer une démarche scientifique.
Communiquer dans un langage scientifique : schéma fonctionnel.
Extraire et exploiter des informations pour comprendre différentes modalités d’une modification du
génome.
Utiliser le logiciel Anagène 2 pour comparer des gènes du développement et identifier les homologies de
séquences.
Raisonner et interpréter un changement évolutif en termes de modification du développement.
Extraire et exploiter des informations pour comprendre des exemples de diversification du vivant sans
modification du génome.
Construire un graphique avec un logiciel type tableur (fiche méthode).
Comprendre la nature provisoire, en devenir, du savoir scientifique.
Etre conscient de sa responsabilité face à l’environnement.
Savoir d’autres mécanismes de diversification des génomes.
Savoir le rôle des gènes dans le développement et les conséquences de variation dans la chronolgie et
l’intensité d’expression de ces gènes.
Savoir une diversification possible des êtres vivants sans modifications des génomes.
Ressources :
- Documents.
- Logiciels : Anagène, type tableur.
Matériel :
- Matériel informatique.
- Matériel d’acquisition et de numérisation d’images.
- Matériel d’observation : microscope…
Activité 1: la polyploïdisation, exemple de la spartine.
1. Quel problème soulève l’histoire évolutive du blé (document 1) concernant l’apparition de l’espèce Triticum
aestivum à partir des deux espèces Triticum turgidum et Tritucum tauschii ?
On parle généralement d’hybridation pour désigner le croisement entre deux variétés différentes d’une même
espèce. Toutefois, le croisement entre deux individus d’espèces différentes est possible. Dans la très grande
majorité des cas, l’hybridation interspécifique conduit à des descendants infertiles en raison d’un mauvais
appariement des chromosomes homologues lors de la méiose. Pourtant, dans certains cas, la stérilité des
hybrides peut être contournée par la polyploïdisation.

2
2. A partir de votre livre p 40 et 41 :
- Combien de chromosomes peut posséder l’espèce Spartina anglica ?
- Expliquer comment la méiose est-elle devenue possible chez l’espèce Spartina anglica
contrairement à Spartina townsendii.
3. Combien de chromosomes peut posséder l’espèce Triticum aestivum ?
4. Montrer, sous forme de schémas légendés, qu’une hybridation suivie d’une polyploïdisation peut engendrer
une diversification des génomes sans mutation (à partir de deux espèces , X avec 2n=4 et Y avec 2n=6).
Activité 2 : Elysia chlorotica.
Les limaces de mer sont des mollusques gastéropodes (ordre Nudibranches) qui ont perdu leur coquille au cours
de l’évolution (document 2). Leurs couleurs fascinent biologistes marins et plongeurs ! Elysia chlorotica vit le long
de la côte atlantique nord-américaine du Canada jusqu’à la Floride. Sa taille adulte minuscule (entre 1 et 3
centimètres) et sa couleur verte pourraient la rendre insignifiante comparativement à ces autres espèces
colorées. Pourtant, cette limace de mer réalise un exploit. Elle peut se nourrir une fois, puis n’a besoin que de
lumière, d’eau et de dioxyde de carbone pour vivre. En effet, elle produit sa propre matière organique
uniquement à partir de matière minérale. Une équipe de chercheurs américains a découvert comment cette limace
de mer est capable d’une telle activité.
Montrer comment les différents documents permettent d’expliquer l’activité exceptionnelle de cette limace
de mer.
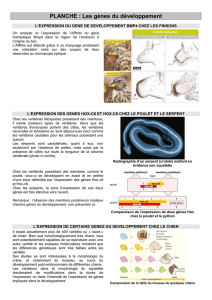
Activité 3 : les gènes du développement.
A. Les serpents, une variation du plan d’organisation des vertébrés. (académie Nantes F. Buron-Mousseau)
Vous avez donc à disposition un squelette de lézard et un squelette de serpent. Lézards et serpents appartiennent
à la lignée des squamates et les lézards forment le groupe de reptiles le plus important et le plus diversifié.
1. Observer et comparer le plan d’organisation de ces deux animaux.
Le python sera donc utilisé comme modèle pour étudier la variation du plan d’organisation au sein des
vertébrés. Les documents sont issus des travaux scientifiques de Martin.J.Cohn et Cheryll Tickle
chercheurs en zoologie à l’Université de Londres et Dundee.
2. A partir des documents A et B (document 3), déterminer (en justifiant) à quel groupe appartient le python.
3. A partir des documents C et D, expliquer la mise en place et le contrôle de l’expansion du nombre de
vertèbres thoraciques.
4. A partir du document E, expliquer la mise en place et le contrôle du développement du membre.
B. Plan d’organisation et morphologie
1. A partir du document A (document 4), expliquer le rôle des gènes homéotiques.
2. Comparer les gènes de développement chez différents animaux avec le logiciel ANAGENE :
Ouvrir thème d’étude puis thèmes personnels
Sélectionner et ouvrir Gènes homéotiques
Sélectionner les fichiers
Faire une comparaison par alignement avec discontinuité
Construire le tableau de comparaison des séquences
3. Conclure
4. Etablir un lien entre les variations dans la chronologie et l’intensité d’expressions de gènes impliqués dans
le développement, et les caractères propres au Chimpanzé et à l’Homme (document B).
Activité 4 : symbiose et diversité des êtres vivants.
1. ECE (ECE 2013 modifié de nodosités et diversification du vivant). Document 5
2. Montrer que, dans chaque cas présenté, le phénotype est modifié par l’association symbiotique (document
6).

3
Document 1 : histoire évolutive du blé.
Hybridation 9000 ans avant JC
Métaphase de mitose Triticum tauschii Métaphase de mitose Triticum turgidum
Blé diploïde sauvage
Triticum monococcum
Blé diploïde sauvage
Triticum tauschii
Blé hexaploïde
Triticum aestivum
Blé tétraploïde
sauvage
Triticum turgidum
Blé tétraploïde dur
cultivé
Triticum turgidum
Blé diploïde sauvage
Triticum speltoïdes

4
Document 2 : limaces de mer.
v
Voici notre cas d’étude : Elysia chlorotica
Document A Cycle de développement : A larve B juvénile après la métamorphose sur l’algue Vaucheria. C juvénile
après 5 jours de la première prise de nourriture D adulte

5
Quatre jours après la ponte, des larves éclosent et mènent une vie planctonique. Elles se nourrissent d’algues
unicellulaires microscopiques. Au bout de 3 semaines, elles se fixent sur des filaments de l’algue Vaucheria et se
métamorphosent. Les juvéniles affichent plutôt un brun translucide, étoilé de points rouges. Puis, elles se
nourrissent des filaments de l’algue dont elles sont friandes. Leur corps change alors de couleur et virant
progressivement au vert intense qu’elles garderont toute leur vie. Parallèlement, un phénomène surprenant se
produit : une fois ce repas terminé, elles peuvent rester plusieurs semaines voire plusieurs mois sans manger de
nouveau. La durée de vie de l’adulte est de 9 à 10 mois.
Document B : localisation de chloroplastes.
Chloroplastes de l’algue Vaucheria vus au microscope électronique
Photographies de chloroplastes au niveau de filaments
de l’algue Vaucheria.
Au niveau d’une cellule épithéliale de l’appareil digestif
du mollusque vue au microscope électronique
Document C : échanges gazeux des limaces avec leur environnement.
Les chercheurs ont quantifié les échanges de dioxygène de la limace adulte avec leur environnement en fonction
de l’intensité lumineuse à laquelle ont été soumis les animaux. Le tableau indique les résultats obtenus :
Intensité lumineuse en % de l’intensité maximale
Intensité des
échanges de O2
(En µmol de
02/mgchl/h)
100
50
25
10
0
+17
+12
+6
+0.5
-7
+ :dégagement de 02 - : absorption de 02
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
1
/
17
100%