PROPHYLAXIEInfos Année 1 No 1/2006

PROPHYLAXIEInfos
Année 1 No1/2006
Informations pratiques sur la prévention en hygiène bucco-dentaire
Action antibactérienne des fluorures
d’amines sur la plaque dentaire
Autres thèmes:
Prophylaxie
Le diabète et les parodontites
EuroPerio5
Traitement à long terme des patients souffrant de parodontite et après pose d’implants
Interview
Stratégies et technologies nouvelles dans les maladies parodontales

02 1/2006 PROPHYLAXIEInfos
Editorial
Thème principal
–Action antibactérienne des fluorures
d’amines sur la plaque dentaire 3
Prof. Dr. Dr. Lutz Stößer, Jena, Allemagne
Prophylaxie
–Le diabète et les parodontites 6
Prof. Dr. Leonardo Trombelli, Ferrara, Italie
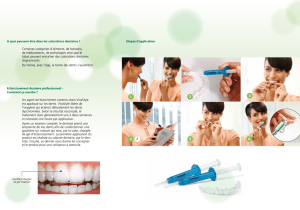
Information sur les produits
–Soins dentaires des patients
présentant des collets dénudés
et des dents sensibles 8
Congrès international
–EOS 2006: Les taches blanches
(White Spots) peuvent-elles être évitees
lors d’un traitement d’orthodontie? 11
– EuroPerio5: Traitement à long terme
des patients souffrant de parodontite et
après pose d’implants 12
– EuroPerio5: Diagnostic et traitement
des infections péri-implantaires 15
Interview
–Stratégies et technologies nouvelles
dans les maladies parodontales 17
• Les tests biologiques en odontologie:
intérêts et limites
Dr. Michel Sixou, Toulouse
• Technologies et stratégies nouvelles
dans les maladies parodontales
Dr. Jean-François Michel, Rennes
Chère Lectrice,
Cher Lecteur,
L’édition que vous tenez en main est le premier
numéro de ce nouveau magazine PROPHYLAXIEInfos.
Il est possible que vous vous demandiez « Pourquoi
un nouveau magazine professionnel? » ou « Que pré-
sente-t-il de particulier? »
PROPHYLAXIEInfos est un magazine professionnel
destiné aux dentistes omnipraticiens mais aussi aux
universitaires. Il est édité par le laboratoire GABA, le
fabricant d’elmex et méridol, et publié deux fois par an
avec des articles d’experts internationaux renommés.
Dans cette édition, le Professeur Lutz Stößer de
l’université de Jena (Allemagne) a rédigé un article sur
le fluorure d’amines et ses propriétés. En outre, nous
nous intéresserons à EuroPerio5 (Madrid) avec des
conférences des Professeurs Mariano Sanz (Madrid/
Espagne), Tord Berglundh (Göteborg/Suède) et
Maurizio Tonetti (Connecticut/U.S.A.). Le Professeur
Leonardo Trombelli de l’université de Ferrara (Italie)
s’intéresse aux exigences particulières de l’hygiène
buccale chez les diabétiques. L’éclectisme internatio-
nal de la sélection des auteurs constitue une particu-
larité dans le domaine des magazines professionnels.
PROPHYLAXIEInfos est également publié en
Allemagne, en Suisse, en Autriche, en Italie et aux
Pays-Bas. L’édition la plus ancienne est le PROPHY-
LAXEdialog en Allemagne qui existe depuis 10 ans et
qui est lu par 36.000 dentistes chaque année.
Par ailleurs, nous traiterons les exigences posées à
une pâte dentifrice pour dents sensibles et collets
dénudés, un domaine où il règne encore trop d’erreurs
et des principes actifs qui ne soutiennent pas le patient
de façon optimale, ainsi que la question de savoir si les
« taches blanches » (White Spots) peuvent être évitées
dans le traitement d’orthodontie. Enfin, nous avons
mené en France deux interviews avec le Docteur
Michel Sixou de l’université de Toulouse, et le Docteur
Jean-Francois Michel de l’université de Rennes, sur les
nouvelles stratégies et technologies dans les maladies
parodontales.
La variété des sujets est vaste. Pour nous, il est
important que nos articles soient transposables non
seulement dans la vie quotidienne du cabinet dentaire
et qu’elles soient pertinentes pour celui-ci, mais qu’el-
les soient également fondées scientifiquement et bien
documentées par des études. Nous pensons que ceci
constitue également un prérequis nécessaire.
Mais il y a encore une autre particularité: Le
PROPHYLAXIEInfos témoigne du souhait d’initier un
dialogue vivant entre les experts universitaires, le den-
tiste omnipraticien et le fabricant. Vous pouvez con-
tribuer à l’évolution de PROPHYLAXIEInfos en nous
faisant parvenir vos desiderata. Nous nous réjouissons
de vos suggestions et nous demanderons aux experts
de les commenter sous forme d’articles selon les prio-
rités de chaque domaine dans les éditions futures.
Nous vous souhaitons bonne lecture de cette pre-
mière édition et nous serions très heureux de vous
compter parmi nos nouveaux lecteurs.
Contenu

PROPHYLAXIEInfos 1/2006 30
Introduction
Dans les années 30 du XX siècle,
Lohmann et
Meyerhof
rapportèrent la haute sensibilité au fluorure
du métabolisme énergétique glycolytique des mam-
mifères. Peu après, l’inhibition par de faibles concen-
trations en fluorure de la production d’acide par les
streptocoques et lactobacilles oraux a été décrite par
Bibby et van Kesteren
(1940). Aujourd’hui, en l’état
actuel des connaissances, c’est l’action locale des
fluorures sur la solubilité de l’émail dentaire, sa reminé-
ralisation et surtout sur le métabolisme bactérien qui
suscite l’intérêt.
La concentration en fluorure
dans la plaque dentaire
La disponibilité en fluorure dans la plaque dentaire
est cruciale pour son effet cariopréventif. Il convient ici
de noter que l’acide fluorhydrique (acide faible) est dis-
socié à 98% à un pH supérieur à 5,0 mais indissocié à
12% déjà à pH 4,0 (sous forme de HF). Conséquence
de sa réactivité, le fluorure est stocké de manière intra
(liaison aux protéines cytoplasmiques) et extracellulaire
(fluorure de calcium stabilisé par des phosphates an-
organiques et des protéines de la matrice). En l’état
actuel des connaissances, deux formes se distinguent
dans la plaque dentaire: environ 5% du fluorure est
«libre» et 95% est «extractible». En cas de faible apport
de fluor, la plaque contient environ 5 à 10 ppm (poids
hydraté) de fluor et en cas de forte concentration
dans l’eau de boisson, cette valeur augmente à 10 ou
20 ppm.
Absorption de fluorure
par la plaque dentaire
La quantité de fluorure dans les bactéries dépend
des concentrations en fluorure à l’extérieur de la cellu-
le; elle peut augmenter dans le milieu intracellulaire de
manière énergie-indépendante contre le gradient de
concentration. Lorsque le pH extracellulaire chute en
raison de la production d’acide par les bactéries, la
quantité de fluorure indissocié (HF) devient relative-
ment haute. En raison de son électroneutralité, il
pénètre dans la cellule et se heurte aux pH neutres,
ce qui provoque sa dissociation en H+et F
-
(fig. 1).
Ainsi, ce n’est pas seulement le fluorure qui entre
dans la cellule, mais aussi un flux de protons engen-
drant une acidification du milieu intracellulaire. Dans la
cellule, une grosse partie du fluorure se trouve sous
une forme libérable par ionisation et une partie bien
plus faible sous une forme liée non dissociable. La sen-
sibilité au fluorure est très différente en fonction des
espèces et des genres microbiens. Indépendamment
de ces différences, aucune modification de la commu-
nauté bactérienne n’a été observée à des concentra-
tions de fluorure de 1 mmol/l (19 ppm) dans la plaque
dentaire.
Effets métaboliques spécifiques
du fluorure
Le fluorure attaque les point suivants dans le méta-
bolisme bactérien:
1. Enolase: cette enzyme est la cible principale de
l’ion fluorure dans la cellule bactérienne; son site actif
contient du magnésium réagissant avec le fluorure, ce
qui interrompt la transformation du 2-phosphoglycé-
rate en phosphoénolpyruvate (PEP). Il s’en suit une
perturbation sévère du métabolisme énergétique.
L’énolase n’est pas seulement sensible au fluorure mais
aussi aux variations de pH intracellulaire. Son pH opti-
mum se situe entre 7,3 et 7,7. La réduction de la pro-
duction d’acide est utilisée comme signe d’une per-
turbation du métabolisme énergétique microbien. Elle
reflète l’effet antibactérien du fluorure et représente
une fonction importante dans la prévention des caries.
Thème principal
Action antibactérienne des fluorures d’amines
sur la plaque dentaire
Professeur Dr. Dr. Lutz Stößer, Université Friedrich-Schiller, Jena, Allemagne
Membrane plasmique
H+ + F- HF
pH 4,0
milieu
extracellulaire
HF H+ + F-
pH 7,0
milieu
intracellulaire
Fig. 1: Transport du fluorure à travers la membrane bactérienne
à pH acide

en suspension dans un liquide, a montré que des con-
centrations 75 à 300 fois plus élevées étaient nécessai-
res pour obtenir un effet similaire sur le bio
film.
Les courbes de Stephan tracées par
Graf
lors de
l’adjonction de solutions contenant du fluorure et du
saccharose confirment la différence de la réaction du
biofilm. Les résultats in vivo parallèles montrent que
l’inhibition de la production d’acide aurait dû survenir
plus tôt et plus intensément (fig. 2).
De manière indépendante, la production d’acide
dans la plaque dentaire semble être inférieure de
0,2 unité de pH environ sous administration perma-
nente de fluorure, ce que
van Loveren
associe à une
participation significative à la prévention des caries.
Le déplacement du minimum de pH de 0,2 unité vers
la neutralité permet une saturation plus précoce du
liquide de la plaque dentaire en apatite et la solubili-
sation de l’apatite amélaire est moins importante ou
totalement supprimée.
Produit Bactéries en Bactéries en
suspension biofilm
CBM* Durée CBM Durée
µM d’action µM d’action
nécessaire min nécessaire min
AmF 20 < 5 1.500 < 5
AmCI 10 < 5 1.500 < 5
CHX 5 < 5 1.500 < 5
44 1/2006 PROPHYLAXIEInfos
Thème principal
2. PEP-phosphotransférase: le transport des
sucres par la membrane bactérienne est touché, car
le système phophoénolpyruvate-phosphotransférase
(PEP-PTF) nécessite de l’ATP pour la translocation du
glucose dans la membrane et son activation.
Le système enzymatique lui-même ne réagit pas
avec le fluorure: la pénétration insuffisante de glucose
dans la cellule est due directement à la carence en ATP.
3. ATPase de transport des protons et «Proton
Motive Force»: chez les bactéries anaérobies, l’ATPase
transmembranaire pompe les protons pour créer un
gradiant de pH entre le milieu intra et extracellulaire
servant au transport des acides aminés et du glucose
dans la cellule. La carence en ATP disponible perturbe
cette fonction cellulaire.
4. Macromolécules/polysaccharides (PS): les bac-
téries orales forment des polysaccharides extra et
intracellulaires pour les utiliser comme réserves en cas
de disette, comme composantes de la matrice ou
comme «colle» pour l’ancrage sur les surfaces solides.
Le fluorure inhibe la synthèse de PS extracellulaire
insoluble dans l’eau chez
S. mutans
, alors que la syn-
thèse de PS hydrosoluble n’est pas influencée. Bien
qu’un déplacement du rapport fructose-glucose du PS
par le fluorure ait été décrite, aucune influence de ce
dernier sur la glucosyltransférase ou la fructosyltrans-
férase n’a été montrée, même jusqu’à une concentra-
tion en fluorure de 200 ppm.
A l’inverse, des effets inhibiteurs du fluorure sur la
synthèse des constituants cellulaires macromoléculai-
res comme l’acide lipoteichoique ou les peptidogly-
canes, cruciaux pour la paroi, ont été décrits.
Pour résumer les effets inhibiteurs du fluorure, on
peut donc dire que l’inhibition de la glycolyse n’est pas
la seule à revêtir une importance significative: les bac-
téries sont en effet simultanément endommagées par
une perturbation du gradiant de pH.
Extrapolation
in vivo
La concentration en fluorure étudiée lors des tests
in vitro
en laboratoire n’est pas directement extrapola-
ble à celle du biofilm de la plaque dentaire. En effet,
les schémas de réaction des bactéries organisées et
structurées dans le biofilm se différencient notable-
ment de ceux des cultures bactériennes planctoniques.
Une comparaison de l’efficacité bactéricide du fluorure
d´amines, du chlorure d’amines et de la chlorhexidine
sur la souche
S. sobrinus 6715
, organisée en biofilm ou
Effets antibactériens du fluorure d’amines (AmF), du chlorure d’amine
(AmCI) et de la chlorhexidine (CHX) sur S. sobrinus 6715 en suspension ou
en biofilm (d’après Shani et al. 2000) - * Concentr. minimale bactéricide
Enzyme II
Glukose + PEP ---> Glukose-6-P + pyruvate
in vitro:
ppm F
Culture bactérienne 002
(Bibby 1941)
in vivo:
Plaque dentaire naturelle 005
(Neff 1987)
Plaque dentaire artificielle 100
(Bodden 1982)
Plaque interproximale 030
(Cornick 1988)
pH Courbes de Stephan mesurées
8dans la cavité buccale
7
6
5
4
320 40 60 min
(d’après Graf 1968)
1000 ppm F
100 ppm F
10 ppm F
0 ppm F
Fig. 2: Inhibition de la plaque dentaire par différentes concentrations
de fluorure (en haut) et évolution de la courbe de Stephan lorsque la
solution de glucose contient également du fluorure

Concernant l’utilisation clinique du fluorure d´ami-
nes, un effet antibactérien est souvent rapporté. Ce
dernier est également mentionné par certaines études
sur l’usage du méridol®, de la chlorhexidine ou du flu-
orure d’amines
(Schulz et al. 1991)
. Après 21 jours sans
hygiène bucco-dentaire, un dépôt de plaque sur 40%
de la surface a été observé sur la face labiale de l’inci-
sive supérieure droite. Cette plaque a pu être réduite
à 13% grâce à un rinçage au fluorure d´amines deux
fois par jour (250 ppm F) (fig. 3). Une telle réduction de
la plaque dentaire n’a pas été obtenue avec le NaF
(250 ppm)
(Perdok et al. 1989)
.
Les fluorures d’amines présentent des propriétés anti-
bactériennes différentes de l’action du fluorure car ils:
■se répartissent particulièrement vite sur toutes les
surfaces dans la cavité buccale en raison de leurs
propriétés tensioactives,
■montrent une clairance plus longue dans la cavité
buccale ou la plaque dentaire,
■présentent une certaine plaquophilie,
■exercent une forte action antiglycolytique et donc
■un puissant effet bactériostatique et bactéricide.
Pour résumer, on peut dire que des preuves étayant
de manière convaincante l’efficacité antibactérienne et
l’effet cariopréventif des fluorures ont été collectées.
L’influence de l’ion fluorure peut être renforcée par des
anions spécifiques, comme cela a été prouvé pour le
fluorure d´amines. Ces effets soutenant l’action du
fluorure sont très importants pour la forte action cario-
préventive (cliniquement prouvée) des préparations
à base de fluorure d´amines.
Adresse de correspondance:
Prof. Dr. Dr. Lutz Stößer
Klinikum der Friedrich-Schiller-Universität Jena
Poliklinik für Präventive Zahnheilkunde
Bachstraße 18 - D-07743 Jena
Tél.: +49 (0) 3641-934800
Fax: +49 (0) 3641-934802
E-Mail: [email protected]
PROPHYLAXIEInfos 1/2006 55
Thème principal
Spécificité de l’action du fluorure
d’amines
Dans les fluorures d’amines, le cation est une
monoamine (Olafluor) ou une diamine (Dectafluor)
polaire possédant en plus une chaîne aliphatique apo-
laire. Ces composants opposés confèrent à ces molé-
cules des propriétés tensioactives. Il en résulte un
mouillage optimal de la surface dentaire par les fluoru-
res d’amines, ce qui conduit à une interaction avec les
tissus durs et une infiltration dans la plaque dentaire
particulièrement fortes.
La composante organique des fluorures d’amines
présente des propriétés antibactériennes intrinsèques
en interagissant avec la membrane bactérienne. Ces
propriétés peuvent être distinguées dans les modèles
de diffusion du fluorure inorganique qui, en raison de
sa taille réduite, est capable de sortir bien plus rapide-
ment d’un «slow releasing device»
(Shani et al. 1998)
.
Avec le fluorure d´amines, la concentration minimale
inhibitrice chez
S. sobrinus
est 100 fois plus faible
qu’avec le NaF
(Shani et al. 1996).
Les bactéries gram-
négatives sont également tuées par le fluorure d´ami-
nes et même
A. actinomycetemcomitans
, un micro-
organisme difficile à influencer, est touché par un
dixième de la concentration présente dans elmex®
(Olafluor)
(Oosterwaal et al. 1989, 1990).
A la suite d’études portant sur l’émail dentaire
traité par la salive, une longue durée d’action compa-
rable à celle de la chlorhexidine a été rapportée pour
le fluorure d´amines
(Decker at al. 2003)
. Les concen-
trations bactériostatiques ou bactéricides, se situent
entre 65 à 260 µg/ml pour une durée d’action de 3
à 46 minutes, comme l’a montrée une étude menée
chez 40 souches
(Kay, Wilson 1988)
. Cette action n’est
pas uniquement due à l’ion F.
Les études
in vitro
sur l’influence du NaF et du flu-
orure d´amines sur l’énolase et l’ATPase transmembra-
naire
(van Loveren)
suggèrent différents mécanismes
métaboliques car l’énolase est inhibée par le fluorure
de sodium alors que la partie amine exerce une action
protectrice et même stimulante sur l’enzyme. Par cont-
re, l’ATPase est nettement plus sensible au fluorure
d´amines qu’au NaF. C’est donc l’addition des effets
inhibiteurs des fluorures d’amines qui enraye la glyco-
lyse bactérienne.
Dans la plaque dentaire, le fluorure d´amines pré-
sente une action particulièrement durable (comparable
à une action à libération prolongée)
(Dolan et al. 1974)
:
90 minutes après un rinçage au NaF, aucune limitation
dans la courbe de Stephan n’est observée après ad-
jonction de glucose dans la plaque, alors qu’après un
traitement par le fluorure d´amines, une réduction de
l’activité est notée
(Schneider, Mühlemann 1974)
.
L’effet
antiglycolytique du fluorure d´amines dure 3 à 6
heures.
%
40
35
30
25
20
15
10
5
0Placebo AmF/SnF2CHX AmF
39
24
3.5
18
2
21
13
24
Jour 21
Jour 0
Fig. 3: Dépôt de plaque sur la dent 12 après 5 jours sans hygiène
bucco-dentaire, puis après 21 jours de rinçage buccal avec une solu-
tion contenant un placebo, du fluorure d´amines/d'étain (250 ppm F),
de la chlorhexidine (0,2 %) ou du fluorure d´amines (250 ppm F)
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
1
/
20
100%