DAVD : évolution de la présentation clinique en fonction

C
A S C L I N I Q U E
La Lettre du Cardiologue - n° 378 - octobre 2004
40
DAVD : évolution de la présentation
clinique en fonction de l’âge
V. Algalarrondo, D. Messika-Zeitoun, M.C. Aumont, V. Beauchais, A. Vahanian*
* Hôpital Bichat, Paris.
OBSERVATION
Monsieur R., 62 ans, est hospitalisé en cardiologie pour bilan de
douleurs thoraciques. Ce patient a comme principal antécédent
une dysplasie arythmogène du ventricule droit (DAVD) suivie
depuis l’âge de 35 ans, découverte à l’occasion d’épisodes de
tachycardie ventriculaire mal tolérés. Un traitement antiaryth-
mique associant un bêtabloquant, un inhibiteur calcique et un
antiarythmique de classe Ia est mis en route et maintenu à l’iden-
tique depuis 1987 devant l’absence de récidive de troubles du
rythme. La fraction d’éjection du ventricule gauche (FEVG) était
normale sur la dernière échographie cardiaque datant de plusieurs
années.
La symptomatologie actuelle est celle de gênes thoraciques
atypiques et d’une fatigabilité d’effort. Monsieur R. n’a pas de
facteur de risque cardiovasculaire, hormis un léger surpoids (IMC
à 25). L’examen clinique retrouve un patient en bon état général,
des bruits du cœur assourdis, sans signe clinique d’insuffisance
cardiaque. L’ECG est aspécifique, en rythme sinusal, régulier,
avec un hémibloc antérieur gauche. La radiographie thoracique
retrouve une cardiomégalie. La coronarographie se révèle nor-
male. Le monitorage rythmique pendant l’hospitalisation n’ob-
jective aucune anomalie.
Un nouveau bilan morphologique est réalisé à l’occasion de cette
hospitalisation. L’échographie cardiaque retrouve une dilatation
importante des cavités droites, un ventricule droit trabéculé, très
hypokinétique, avec maintien d’une contraction uniquement dans
la région apicale, et une insuffisance tricuspide fonctionnelle de
grade 4. La pression pulmonaire systolique n’est pas mesurable
du fait du caractère laminaire de la fuite tricuspide. De manière
plus surprenante, le ventricule gauche est, lui aussi, dilaté et le
siège d’une hypokinésie globale. La fraction d’éjection du ven-
tricule gauche est estimée à 30-35 %. Cette altération est confir-
mée par la scintigraphie. L’IRM cardiaque retrouve la dilatation
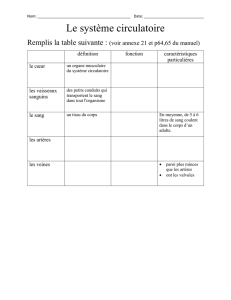
et l’hypokinésie du ventricule droit (figure 1) ainsi qu’un ven-
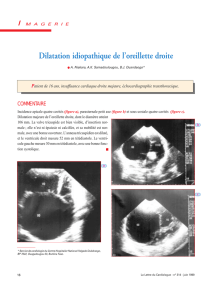
tricule gauche dilaté, siège d’un hypersignal au niveau de sa paroi
latérale témoignant de l’atteinte dysplasique (figure 2).
Figure 1. IRM cardiaque, coupe centrée sur les cavités droites. Le ven -
tricule droit est dilaté, trabéculé. Ses parois sont amincies.
Figure 2. IRM cardiaque coupe parasternale petit axe. En plus de l’at -
teinte ventriculaire droite, on note une dilatation ventriculaire gauche
avec un hypersignal au sein de sa paroi latérale, témoignant de l’infil -
tration adipeuse du ventricule gauche (flèche).

La Lettre du Cardiologue - n° 378 - octobre 2004
41
C
A S C L I N I Q U E
On conclut donc au diagnostic de DAVD vieillie avec atteinte
biventriculaire sévère, développant des symptômes d’insuff i s a n c e
cardiaque. Un traitement médical adapté est associé, et le patient
regagne rapidement son domicile.
DISCUSSION
La DAVD est une myocardiopathie du ventricule droit décou-
verte à la fin des années 1970 (1), caractérisée par un remplace-
ment du tissu musculaire par du tissu fibro-adipeux. Les critères
diagnostiques de la DAVD sont maintenant clairement définis
(2). On recense environ 1 000 cas en France. Le diagnostic de
D AVD chez des patients jeunes, leur suivi et le regroupement des
patients dans des centres spécialisés permettent de mieux appré-
cier l’évolution, encore mal connue, de cette pathologie. Le cas
présenté ci-dessus illustre plusieurs aspects de cette évolution :
–le diagnostic est souvent fait précocement (80 % avant 40 ans)
chez un homme (sex-ratio de 3 pour 1) (3) ;
– les accidents rythmiques (troubles rythmiques graves, mort
subite) se situent entre 20 et 40 ans. L’atteinte précoce du ven-
tricule gauche ainsi qu’une dilatation majeure du VD constituent
les principaux facteurs de risque (4) ;
– la présence de signes d’insuffisance cardiaque (droite et/ou
gauche) s’observe bien plus tard (entre 55 et 70 ans) ;
–si une atteinte histologique du ventricule gauche est retrouvée
dans 3 cas sur 4 (5), la majorité des patients (80 à 90 % des cas)
ont une FEVG globalement conservée (FE moyenne à 60 % ) .
Une atteinte biventriculaire clinique est présente dans 10 à 20 %
des cas, et la FEVG est souvent sévèrement altérée (entre 20 et
30 %) ;
–l’IRM, en complément de l’échographie cardiaque, constitue
un examen particulièrement utile. Elle permet de porter le dia-
gnostic de DAVD devant la présence d’une infiltration graisseuse
de la paroi ventriculaire droite, d’apprécier une éventuelle exten-
sion au ventricule controlatéral et d’évaluer la fonction globale
et segmentaire des deux ventricules (“séquence ciné”) (6).
Les arythmies ventriculaires forment le principal point d’appel
faisant poser le diagnostic. Si ces arythmies manquent à l’his-
toire clinique, la DAVD peut donc se présenter sous la forme
d’une cardiomyopathie dilatée à coronaires saines. Ainsi, 5 %
des patients transplantés à la Mayo Clinic pour insuffisance car-
diaque avaient une histologie cardiaque compatible avec une
DAVD (7).
L’amélioration des thérapeutiques rythmiques de ces patients
amènera probablement à prendre de plus en plus en charge ces
cardiopathies vieillies, contrôlées sur le plan rythmique, mais
présentant une défaillance uni- ou biventriculaire. L’ é v o l u t i o n
vers l’insuffisance ventriculaire droite peut faire envisager une
cardiomyoplastie dynamique du VD (technique consistant à
enrouler le muscle grand dorsal autour du VD dans le but d’amé-
liorer sa fonction contractile et de stopper le processus de remo-
delage) (8), voire une transplantation cardiaque en cas d’atteinte
biventriculaire avec insuffisance cardiaque réfractaire.
B i b l i o g r a p h i e
1.
Fontaine G, Frank R, Vedel J et al. Stimulation studies and epicardial map -
ping in ventricular tachycardia: study of mechanisms and selection for surgery.
In: Reentrant arrhythmias. Lancaster, PA: MTP Publishing, 1977;334-50.
2.
Richardson P, McKenna W, Bristow M et al. Report of the 1995 World Health
Organization/International Society and Federation of Cardiology Task Force on
the Definition and Classification of Cardiomyopathies. Circulation 1996;93:841-2.
3.
Gemayel C, Pelliccia A, Thompson PD. Arrhythmogenic right ventricular car -
diomyopathy. J Am Coll Cardiol 2001;38:1773-81.
4.
Peters S, Peters H, Thierfelder L. Risk stratification of sudden cardiac death
and malignant ventricular arrhythmias in right ventricular dysplasia-cardiomyo -
pathy. Int J Cardiol 1999;71:243-50.
5.
Corrado D, Basso C, Thiene G et al. Spectrum of clinicopathologic manifes -
tations of arrhythmogenic right ventricular cardiomyopathy/dysplasia: a multi -
center study. J Am Coll Cardiol 1997;30:1512-20.
6.
Boxt LM, Rozenshtein A. MR imaging of arrhythmogenic right ventricular dys -
plasia. Magn Reson Imaging Clin N Am 2003;11:163-71.
7.
Nemec J, Edwards BS, Osborn MJ, Edwards WD. Arrhythmogenic right ven -
tricular dysplasia masquerading as dilated cardiomyopathy. Am J Cardiol 1999;
84(2):237-9,A9.
8.
Chachques JC, Argyriadis PG, Fontaine G et al. Right ventricular cardio -
myoplasty: 10-year follow-up. Ann Thorac Surg 2003;75:1464-8.
Les articles publiés dans “La Lettre du Cardiologue”le sont sous la seule responsabilité de leurs auteurs.
Tous droits de reproduction, d'adaptation et de traduction par tous procédés réservés pour tous pays.
EDIMARK S.A.S. © mai 1983
Imprimé en France - Differdange S.A. - 95110 Sannois - Dépôt légal : à parution
Ce numéro est routé avec :
un supplément Correspondances en Risque Cardiovasculaire
“Hypertension artérielle : VALUE et la prise en compte des principaux facteurs de risque cardiovasculaire” (12 pages) ;
un encart 4 pages, intitulé “Sevrage tabagique”, est inséré entre les pages 26 et 27.

AMLOR, p. 42
1
/
3
100%