Transposons: des gènes a

© POUR LA SCIENCE -N° 351 JANVIER 2007
82
D. Anxolabéhère • D. Nouaud • H. Quesneville • S. Ronsseray
P
P
lus de deux mètres d’
ADN
dans chacune
de nos cellules. Près de trois milliards
de nucléotides, soit autant de lettres
A
,
T
,
C
ou
G
qui constituent notre patrimoine
génétique. Un monde certes vaste, mais
que l’on imagine le plus souvent stable,
du moins pour un organisme donné: une
référence sur laquelle la cellule peut compter en toute
occasion pour fabriquer ce dont elle a besoin. Il y a bien
quelques mutations deci-delà, au gré des divisions et
selon l’environnement, mais rien de bien bouleversant.
Erreur, le génome est bien plus « agité » qu’il n’y paraît: des
fragments se détachent, se reproduisent, s’insèrent spon-
tanément en d’autres endroits et multiplient les désordres.
Ces éléments, nommés transposons ou gènes sauteurs,
ont été découverts dans les années 1950 par l’Américaine
Barbara McClintock, récompensée par le prix Nobel en 1983.
Ces transposons, autoréplicatifs (nous verrons comment)
et mobiles, ne sont pas anecdotiques: ils représentent jus-
qu’à 90 pour cent du génome de certaines espèces, tel le blé,
et presque la moitié de notre génome.
Ces transposons sont des gènes, en ce sens qu’ils codent
des protéines, mais celles-ci ne sont destinées qu’au fonction-
nement de l’élément. Lorsqu’ils se déplacent, les transposons
peuvent modifier le fonctionnement du génome de leur hôte,
par exemple en s’insérant dans une séquence codante ou
régulatrice. De plus, les transposons portent eux-mêmes
des séquences régulatrices qui interfèrent parfois avec des
séquences voisines. Ainsi, après l’insertion d’un transpo-
son, des gènes peuvent adopter de nouveaux profils d’ex-
pression temporelle ou spatiale. L’action mutagène des
transposons ne se limite pas là. Ils entraînent également des
réarrangements chromosomiques de grande ampleur.
On convient aujourd’hui que les transposons ont eu
un rôle essentiel dans l’évolution de la structure, de la
taille et du fonctionnement des génomes, mais ils furent ini-
tialement considérés comme des séquences d’
ADN
égoïste,
parasite, ou encore de l’
ADN
poubelle, c’est-à-dire ayant été
mis au rebut au cours de l’évolution. Cette période est révo-
lue et les transposons sont désormais, aux yeux des biolo-
gistes, des « semences de l’évolution », car ils accroissent
les potentiels évolutifs des organismes au travers de
divers mécanismes que nous détaillerons. L’étude des trans-
posons a profondément changé notre vision de nombreux
processus génétiques, telles la mutation, la recombinai-
son, la régulation génique, en un mot l’évolution des
génomes. Dans cet article, après avoir décrit l’anatomie d’un
transposon et ce que l’on sait de leur évolution, nous pré-
senterons quelques exemples, où les désordres occasionnés
seront croissants, illustrant le rôle des transposons dans le
remodelage des génomes tant au travers de l’architecture
des chromosomes que de l’émergence de nouveautés géné-
tiques. Enfin, nous examinerons comment, chez l’être
humain, les transposons participent à diverses maladies
génétiques et à certains cancers. Commençons par voir à
quoi ressemble un transposon et comment il fonctionne.
Parmi tous les organismes, on distingue trois types de
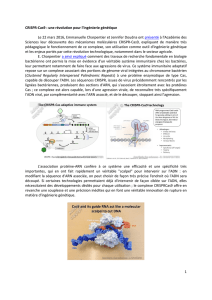
transposons répartis en deux classes (voir la figure 1). Diffé-
rents par leur structure ou leur mécanisme de transposition,
1. Les transposons sont des fragments d’
ADN
d’une cellule qui se
détachent, se multiplient et s’insèrent en d’autres endroits de façon indé-
pendante de l’hôte. Présents chez tous les organismes vivants, on en dis-
tingue deux classes. Les événements moléculaires illustrés ici se déroulent
dans le noyau (à gauche) ou dans le cytoplasme (à droite). Les transpo-
sons de classe
I
(
A
)sont des rétrotransposons: dans le noyau, ils sont
transcrits (
B
)en
ARN
(en violet), lesquels sont traduits, dans le cytoplasme,
en protéines (
C
), par exemple la transcriptase inverse (en bleu) ; cette der-
nière copie l’
ARN
en
ADN
(
D
), qui s’insère (
E
)dans le génome. Les transpo-
sons de classe
II
(
F
)se dispensent de l’intermédiaire
ARN
. Dans les deux
cas, l’insertion du transposon, par exemple dans un gène (en jaune),
peut perturber le fonctionnement de la cellule. Les multiples couleurs de
certains épis de maïs (dont le génome contient 50 pour cent de transpo-
sons) résultent de tels phénomènes.
Des fragments d’
ADN
vivent en toute indépendance dans le génome.
Ce faisant, ils bousculent le fonctionnement
des gènes, souvent pour le pire,
mais parfois pour le meilleur.
Toutes les illustrations sont de Virginie Denis
Transposons: des gènes a
351-ANXOLA.FP.xp 11/12/06 12:42 Page 82

Transposon de classe
II
Copie du transposon
Insertion
de la copie
Gène perturbé
Transposon de classe
I
ARN
ARN polymérase
Ribosome
Transcriptase
inverse
Copie du transposon
Insertion
de la copie
Gène perturbé
NOYAU
CYTOPLASME
A
s anarchistes?
B
E
C
D
F
351-ANXOLA.FP.xp 11/12/06 12:42 Page 83

ils ont en commun d’être relativement petits (de 1 000 à
20000 nucléotides) et de coder les protéines nécessaires à
la mobilité de l’élément et à son insertion en un nouveau
site génomique.
Les éléments de classe
I
sont les rétrotransposons. Ils
se déplacent grâce à une enzyme (codée par le transpo-
son) qui copie l’
ARN
, transcrit de l’
ADN
du transposon, en
un nouvel
ADN
. Ce dernier phénomène est une transcrip-
tion inverse. Les éléments nommés
LINE
(pour Long Inter-
spersed Nuclear Element, soit Long élément nucléaire disséminé)
codent une unique enzyme multifonctionnelle qui, outre
son activité de transcriptase inverse, reconnaît et coupe
l’
ADN
. Les rétrotransposons à
LTR
, dotés de longues répé-
titions terminales (les
LTR
), codent cinq protéines diffé-
rentes, dont trois enzymes: la protéase et la transcriptase
inverse participent à la réplication de l’élément, tandis que
l’intégrase coupe l’
ADN
au site d’insertion. Ces mécanismes
sont similaires à ceux des rétrovirus, tel le
VIH
, quand ils
infectent une cellule.
Les éléments de classe
II
sont les transposons à
ADN
.
Ils se passent de l’intermédiaire
ARN
et codent une enzyme,
une transposase, qui reconnaît les extrémités de l’élément,
l’excise et l’insère ailleurs dans le génome. Ce mécanisme
de couper-coller conduit parfois à une augmentation du
nombre de copies, par exemple quand l’excision se pro-
duit après la réplication et l’insertion dans un nouveau site,
avant le passage de la fourche de réplication.
Chacune de ces classes réunit des éléments plus petits,
les
SINE
(pour Short Interspersed Nuclear Element) et les
MITE
(pour Miniature Inverted-repeat Transposable Element) dont la
taille varie de 100 à 1000 nucléotides. Non autonomes, ils
sont dépourvus de séquence codante et utilisent les protéines
codées par d’autres transposons (voir la figure 3).
Au regard de l’évolution
Le séquençage a révélé que 45 pour cent du génome humain
sont constitués de transposons (pour seulement un à
deux pour cent de gènes codant des protéines cellulaires).
Le plus souvent, seules quelques familles constituent les
transposons d’un génome. Ainsi, plus de 20 pour cent de
notre génome sont des rétrotransposons de type
LINE
, et
principalement des éléments de la famille
LINE
1 (17 pour
cent); plus de 13 pour cent sont des éléments de type
SINE
;
enfin, presque 11 pour cent sont des membres de la
famille Alu (des petits rétrotransposons non autonomes),
qui est aussi la plus représentée en nombre de copies.
Comment ces transposons se sont-ils installés?
La signification évolutive des transposons est débattue.
Les conséquences le plus souvent négatives sur la survie de
leurs hôtes posent le problème de leur maintien au sein
des espèces. En effet, sous la pression de la sélection natu-
relle, les individus avec peu de transposons sont avanta-
gés sur ceux qui en ont beaucoup: on s’attendrait donc à la
disparition progressive des transposons. Or on les trouve
dans presque tous les organismes (animaux, plantes, cham-
pignons, bactéries...), et ce sont les espèces sans transpo-
sons qui apparaissent comme des exceptions énigmatiques;
c’est le cas de la bactérie Bacillus subtilis. Comment se
maintiennent-ils? Selon une première hypothèse, leur pou-
© POUR LA SCIENCE -N° 351 JANVIER 2007
2. Les rétrotransposons, tels ceux de la famille
LINE
1
(en rose)
augmentent la taille des génomes. D’abord, l’élément est transcrit
(a)
en
ARN
(en violet)
. Puis, grâce à une enzyme
(en bleu)
codée par le trans-
poson, cet
ARN
subit une transcription inverse
(b)
, c’est-à-dire qu’il est
recopié en
ADN
. Enfin, ce nouvel
ADN
s’insère dans le génome en un autre
site. La copie peut être tronquée, entière, voire plus grande, quand la
transcription est allée au-delà des limites du transposon.
ADN
Transcription
inverse
ARN
transcrit
Copie entière
Copie tronquée
Enzyme
Transposon
a
a
a
ADN ARN
Enzyme
de
LINE
1
Transpo son
LINE
1
Élément Alu Gène
quelconque
ARN
Nouvelle
copie Pseudogène
Site de recombinaison Transposon
Recombinaison normale
Recombinaison aberrante
Nouvel
ADN
b
3. Les transposons non autonomes, tel l’élément Alu (en
orange), sont mobiles grâce aux protéines codées par d’autres trans-
posons, par exemple
LINE
1 (en rose) : les nouvelles copies d’Alu insé-
rées augmentent la taille du génome (a). Par ailleurs, l’enzyme de
LINE
1
reconnaît n’importe quel
ARN
messager (en bleu foncé) transcrit d’un
gène quelconque (en bleu clair), et peut en faire un pseudogène (un gène
inactif), car l’
ARN
messager n’est pas une copie conforme du gène. Le
pseudogène inséré n’importe où augmente la taille du génome (b).
4. Les recombinaisons inégales. Les transposons, tels ceux de
la famille
LINE
1 (en rose), entraînent des recombinaisons inégales (les
traits discontinus blancs représentent les échanges de matériel géné-
tiques). D’ordinaire, la recombinaison (a)est un échange équilibré de maté-
riel génétique entre deux chromosomes au niveau de sites homologues (en
gris): après la recombinaison, les chromosomes ont la même taille (c).
Cependant, les transposons, sortes de sites homologues, sont répartis aléa-
toirement (b) : le matériel échangé n’est plus équivalent (d).
b
c
d
84
b
ARN
351-ANXOLA.FP.xp 11/12/06 12:42 Page 84

voir mutagène est une source de variabilité génétique qui,
sur le long terme, fait apparaître des mutations avanta-
geuses. Celles-ci compenseraient les effets délétères (mais
non létaux) à court terme. Les transposons seraient alors
des facteurs évolutifs grâce auxquels les espèces s’adaptent
plus rapidement. Cependant, ils pourraient aussi se main-
tenir grâce à leur pouvoir multiplicatif: ils se multiplieraient
plus vite par transposition qu’ils ne sont éliminés par la
sélection, dans une sorte de course-poursuite. Plusieurs
études sur les populations de transposons ont fourni
quelques éclaircissements.
La dynamique
des transposons
On distingue deux modèles de la dynamique des transpo-
sons chez les eucaryotes: l’autorégulation et la sélection. Le
premier modèle s’applique aux transposons qui contrôlent
eux-mêmes leur activité en codant, par exemple, un répres-
seur. La fréquence de transposition d’une copie est alors inver-
sement proportionnelle au nombre de copies dans le génome
de l’individu: plus le nombre de copies est élevé, plus il y a
de répresseur fabriqué et moins il y a de transposition.
Selon le modèle sélectif, la fréquence de transposition
est indépendante du nombre de copies, mais les individus
sont sélectionnés en fonction du nombre de copies d’un
transposon: plus ce nombre est grand, moins l’individu
est viable. Pourquoi? Une hypothèse stipule que les trans-
posons entraîneraient des recombinaisons inégales condui-
sant à des chromosomes déséquilibrés, délétères pour
l’individu (voir la figure 4). Rappelons que la recombinai-
son a lieu au moment de la formation des gamètes: elle se
traduit par l’échange de matériel génétique entre deux chro-
mosomes d’une même paire, qui se « cassent » aux mêmes
endroits (dits homologues) et intervertissent les frag-
ments (de même longueur) obtenus. Or les transposons
joueraient le rôle de « sites homologues »: répartis aléatoi-
rement dans le génome, le matériel génétique échangé
lors de la recombinaison ne serait pas équivalent d’un chro-
mosome à l’autre. Un individu dont le génome est riche
en transposons aurait plus de chances de produire des
gamètes porteurs d’accidents chromosomiques et, en consé-
quence, d’avoir une fertilité diminuée. La réalité est pro-
bablement une combinaison de plusieurs mécanismes, les
deux modèles précédents ne s’excluant pas.
L’invasion des transposons se décompose en deux
phases. La première est l’invasion rapide de l’espèce
avant que des mécanismes de répression (autorégulation
et sélection) ne freinent cette invasion. Suit alors la seconde
phase, celle de dégénérescence: le transposon accumule
des mutations jusqu’à « disparaître » du génome (il est
Les nouveautés génétiques
© POUR LA SCIENCE -Biologie 85
Un transposon de classe
II
(a)
est doté,
à ses extrémités, de motifs nucléo-
tidiques reconnus par le domaine de
fixation à l’
ADN
de la transposase qu’il code
(en violet)
, l’enzyme qui assure la migration
de l’élément. Une fois la transposase arri-
mée au transposon, son domaine endonu-
cléasique
(en bleu)
coupe l’
ADN
. Au cours
de l’évolution, différentes copies d’une même
famille de transposons peuvent perdre leur
mobilité
(b)
: les sites de fixation de l’en-
zyme ne sont alors plus reconnus par la
transposase
(flèches en pointillés)
. Cepen-
dant, certaines copies conservent leur capa-
cité codante, et même si les sites de fixation
ont disparu, l’élément code toujours une
transposase
(c)
. En revanche, d’autres sont
réduits à un unique motif de fixation
(d, e
et
f)
. La transposase peut alors réguler les
gènes
(en jaune)
près desquels les copies
d
,
e
et
f
sont insérées, établissant ainsi
un réseau de régulation génique. Autre
exemple
(g)
: dans un transposon, seule la
partie codant le domaine de fixation à l’
ADN
peut rester fonctionnelle. Quand cet élément
est inséré dans d’autres gènes
(h, i
et
j)
,
les protéines codées acquièrent ce domaine
de fixation à l’
ADN
. Ces « nouveaux » gènes
(k, l
et
m)
peuvent alors constituer une famille
de facteurs de transcription.
Site de fixation Site de fixation
Domaine
de fixation Domaine
d’excision
Transposase
Site de fixation
dégénéré
Séquence codant le domaine
d’excision dégénéré
Nouveaux gènes codant
des protéines dotées d’un domaine
de fixation à l’
ADN
Gènes passés
sous le contrôle
de la transposase
a
i
h
g
f
e
d
c
b
m
l
k
j
351-ANXOLA.FP.xp 11/12/06 12:42 Page 85

© POUR LA SCIENCE -N° 351 JANVIER 2007
86
devenu méconnaissable et ne fonctionne plus). Le salut
du transposon peut venir d’un événement dont les moda-
lités restent mystérieuses: le passage dans une autre espèce,
où son cycle d’invasion recommence. Ainsi, une même
espèce peut subir des invasions successives, voire simul-
tanées, de différentes familles de transposons venus
d’ailleurs. Quelles en sont les conséquences dans le génome?
Les réarrangements génomiques
Plusieurs mécanismes de réarrangements génomiques
ont été identifiés. Le premier concerne les rétrotranspo-
sons, et notamment les éléments de type
LINE
. Leur trans-
cription en
ARN
, la première étape de sa migration, s’arrête
parfois au-delà de l’élément: la séquence génomique aval
est transcrite en continuité avec celle du transposon, fai-
sant la copie plus longue que l’original (voir la figure 2).
Nous avons vu que les copies dispersées d’un trans-
poson pouvaient donner lieu à des recombinaisons inégales
et des chromosomes aberrants. La sélection naturelle par-
ticipe à l’élimination de ces éléments, c’est le modèle sélec-
tif, mais certains événements de recombinaison échappent
à la pression quand le matériel remanié ne perturbe pas
l’intégrité du génome : au final, les chromosomes sont
remaniés de façon durable.
Autre désordre, les éléments de classe
II
créent par-
fois, à cause de leur mode de transposition, des macro-
transposons constitués de deux éléments de la même
famille et de la région génomique qu’ils encadrent. La
transposition utilise l’extrémité droite d’une des copies
et l’extrémité gauche de l’autre comme s’ils étaient les
extrémités d’une même copie. L’ensemble s’excise et s’in-
sère comme un seul transposon, déplaçant une fraction
non négligeable du génome.
Les rétrotransposons à
LTR
auraient un effet plus
notable sur la taille des génomes que les autres types d’élé-
ments. Pour quelles raisons? D’abord, ce sont de grands
éléments; aussi, lorsqu’ils se multiplient, augmentent-
ils plus vite la taille des génomes que les petits transpo-
sons. Cependant, les structures répétées de leurs extrémités
(les
LTR
) jouent un rôle antagoniste. En effet, ces deux
séquences sont la cible de recombinaisons inégales, ce qui
élimine d’un coup la séquence qu’elles encadrent. Ce phé-
nomène peut aussi avoir lieu entre copies et ainsi retirer
des portions génomiques importantes.
Outre ces réductions massives et soudaines, de petites
délétions de quelques dizaines de paires de nucléotides
se produisent continuellement dans le génome. Elles sont
le résultat de cassures, spontanées et aléatoires, de l’
ADN
,
qui sont mal réparées par l’hôte. Lorsqu’elles ont lieu
dans des séquences non essentielles à la survie de l’hôte
ou dans des transposons, ces coupures participent à la dimi-
nution de la taille des génomes. Ce processus d’érosion
joue également un rôle dans l’élimination des transposons.
L’examen du génome révèle que les régions riches en
transposons sont celles où la recombinaison est moins fré-
quente, c’est-à-dire celles où le processus d’élimination
décrit précédemment est moins fréquent, les transposons
pouvant donc s’accumuler. La densité en gènes d’une région
influe aussi sur la densité en transposons. En effet, dans
ces régions à haute densité, les insertions et les éliminations
ont plus de chances de perturber les gènes voisins : la
pression de sélection qui maintient fonctionnels ces gènes
laissera la région pauvre en transposons.
Ces exemples de bouleversements montrent que les
transposons jouent un rôle majeur dans les processus évo-
lutifs en tant que source de nouveauté génétique. Ils ont
aussi des acteurs de la spéciation, c’est-à-dire de l’appa-
rition d’espèces nouvelles à partir d’une population homo-
gène. Trois mécanismes ont été proposés. Le premier est
fondé sur une modification majeure des programmes de
développement des individus. Nous avons vu que les
transposons modifient parfois l’expression des gènes:
de tels changements qui rallongeraient la période de matu-
rité sexuelle de certains individus créeraient un isolement
reproductif, les individus à courte période de maturité
sexuelle s’accouplant ensemble. Selon le deuxième méca-
nisme, les remaniements chromosomiques dus aux trans-
posons empêcheraient l’appariement des chromosomes
homologues chez les hybrides, conduisant là aussi à un
isolement reproductif : seuls les individus au profil
chromosomique identique seraient féconds. Enfin le
dernier mécanisme concerne des familles de transpo-
sons entraînant une dysgénésie des hybrides, par exemple
chez la drosophile. Ces dysgénésies sont des incompati-
bilités de croisements entre des mâles porteurs d’une
famille de transposons et des femelles qui en sont dépour-
vues: la descendance est stérile en raison de multiples
remaniements chromosomiques. Ces croisements déclen-
chent aussi une ségrégation au sein d’une population. Les
effets des transposons que nous avons vus laissent
croire que l’hôte est passif devant cette invasion. Ce
n’est pas toujours le cas.
Le palimpseste génomique
Le manuscrit génomique est réécrit en permanence. La com-
paraison des génomes montre qu’au cours de l’évolution,
les transposons ont notablement contribué à cette réécri-
ture. En effet, ils codent des protéines qui représentent pour
la cellule un répertoire attractif de nouvelles propriétés.
De plus certaines de ces protéines modifient ou détour-
nent la fonction originelle de molécules de l’hôte. Ce der-
nier, en maîtrisant le comportement « anarchique » des
transposons, c’est-à-dire en détournant certaines proprié-
tés de leurs protéines à son profit, bénéficie d’innovations
à bon compte. Voyons comment (voir l’encadré de la page 85).
Plusieurs études ont montré que des transposons de
classe
II
et les transposases qu’ils codent ont été une
source de domaines protéiques pour l’assemblage de nou-
veaux gènes au cours de l’évolution. Au cours de l’évolu-
tion, la séquence codant un domaine de fixation à l’
ADN
d’une transposase peut subir des remaniements et être insé-
rée dans d’autres gènes, on parle de brassage d’exons. Les
protéines codées par ces gènes « dopés » peuvent consti-
tuer, par exemple, une famille de facteurs de transcrip-
tion. Ainsi, le domaine
BED
est un domaine de fixation à
l’
ADN
qui est trouvé à la fois dans plusieurs transposases
et dans plusieurs protéines qui assurent des fonctions cel-
lulaires associées à l’
ADN
.
351-ANXOLA.FP.xp 11/12/06 12:42 Page 86
 6
6
 7
7
 8
8
1
/
8
100%