Commenter ce graphique illustrant les variations respectives du

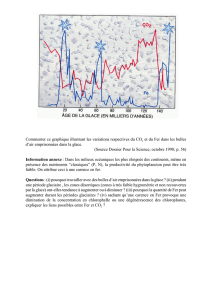
Commenter ce graphique illustrant les variations respectives du CO2 et du Fer dans les bulles
d’air emprisonnées dans la glace. (Source Dossier Pour la Science; octobre 1998; p. 56)
Information annexe : Dans les milieux océaniques les plus éloignés des continents, même en
présence des nutriments “classiques” (P, N), la productivité du phytoplancton peut être très
faible. On attribue ceci à une carence en fer.
Questions 1 : (i) pourquoi travailler avec des bulles d’air emprisonnées dans la glace ? (ii)
pendant une période glaciaire , les zones désertiques (zones à très faible hygrométrie et non
recouvertes par la glace) ont-elles tendance à augmenter ou à diminuer ? (iii) pourquoi la quantité
de Fer peut augmenter durant les périodes glaciaires ? (iv) sachant qu’une carence en Fer
provoque une diminution de la concentration en chlorophylle ou une dégénérescence des
chloroplastes, expliquer les liens possibles entre Fer et CO2 ?
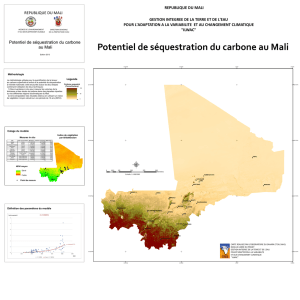
Analyse du document du BRGM (Questions 2)
- Quels sont les différentes possibilités de séquestration de carbone ?
- La séquestration de carbone au niveau du sol existe-t-elle naturellement ?
- Les connaissances scientifiques actuelles sont-elles suffisantes pour envisager une séquestration
efficace du carbone ?
- Quelles sont les limites ? les risques ?
- Quelles sont les principales différences, ou les points communs, entre la séquestration
“océanique” (voir les documents qui suivent) et la séquestration “géologique” ?

Questions 1 : Eléments de correction
(i) l’air piégé dans des micro-poches de glace n’est pas en communication avec l’extérieur et reflète donc la composition de l’air au moment
de son piégeage. Estimation de l’âge en fonction de la teneur en isotopes stables (on connaît la demi-vie ou période).
Donc conditions expérimentales permettent de penser qu’il n’y a pas de contamination. Ce qui est mesuré dans les bulles correspond à ce qu a été
piégé au moment ou la bulle s’est formée. L’air emprisonné est donc représentatif d le’air à une époque donnée.
(ii) le Fer provient essentiellement du domaine terrestre par érosion éolienne et transport par les vents ou les masses d’eaux continentales.
(iii) en période glaciaire, il y a une déshydratation poussée des zones désertiques : l’humidité de l’air est condensée sous forme de glace dans
les hautes latitudes et n’est pas redistribuée à l’échelle planétaire. Il en résulte une avancée ou une extension des zones désertiques. La
conséquence (pas d’obstacle au vent) est une accélération de l’érosion éolienne et donc une augmentation du flux de Fer vers les domaines
océaniques.
(iv) le rôle du Fer chez les végétaux n’est pas forcément très bien compris (voir Hopkins. Physiologie Végétale; De Boeck; page 70-72), mais
on sait qu’il intervient dans la synthèse de la chlorophylle et qu’une carence prolongée induit une dégénérescence des chloroplastes. Dans
les milieux océaniques les plus éloignés des continents, même en présence des nutriments “classiques” (P, N), la productivité du phytoplancton
peut être très faible. On attribue ceci à une carence en fer. En période glaciaire, l’augmentation des apports en Fer a pu relancer la productivité
du phytoplancton. La quantité de carbone fixée a donc considérablement augmenté et, en conséquence, la pression partielle de CO2 a diminuée
dans l’air. Cette diminution de CO2 a entraîné une diminution de l’effet de serre naturel (voir cours sur l’effet de serre) et accentué le
refroidissement de l’atmosphère. Sans intervention d’un autre processus, le système s’auto-entretient, du moins un certain temps. Un
réchauffement climatique a des effets inverses : recul des déserts, diminution de l’érosion éolienne, diminution des apports en Fer en zone
océanique, baisse de la productivité du phytoplancton et augmentation de la pression partielle de CO2.

Remarque 1 (biologie) : les besoins en Fer sont très importants pour les unicellulaires autotrophes. Certains comme le flagellé Ochromonas sont
même capables de phagocyter des bactéries contenant du fer pour assurer une partie de leur approvisionnement en fer. R. Maranger et ses
collaborateurs (1998; Nature, 396: 248-251) ont montré que 35 à 58% des apports en fer du phytoplancton autotrophe en zone équatoriale étaient
assurés par mixotrophie (phagocytose de bactéries). Cette possibilité de passer d’un statut d’autotrophe à un statut de mixotrophe peut représenter
une adaptation aux milieux pauvres en fer.
Remarque 1 (statistique) : la “corrélation” apparente entre les concentrations en fer et en CO2 ne peut être traduite en relation de cause à effet. Il
faut se référer à un processus physiologique (augmentation de la productivité primaire) et physique (diminution CO2 - diminution Effet de Serre -
diminution de la température) pour pouvoir confirmer la relation de cause à effet.
Questions 2 : Eléments de réponse (BRGM) : Quels sont les différentes possibilités de séquestration de carbone ?
* Fixation du CO2 sous forme d’un produit stable (carbonate) = processus naturel
* Biofixation par la biomasse végétale, phytoplancton compris - voir avant (problème de la balance O2 - CO2 de la photosynthèse)
* production de méthane par des bactéries méthanogènes à partir de CO2
* séquestration géologique
- La séquestration de carbone au niveau du sol existe-t-elle naturellement ?
Oui, CO2 emprisonné naturellement dans des couches géologiques (processus pas forcément connus, mais anciens - 15 millions d’années).
Fuite de CO2 parfois dans les nappes aquifères : sources d’eau pétillante !
- Les connaissances scientifiques actuelles sont-elles suffisantes pour envisager une séquestration efficace du carbone ?
Non : récupération, transport et surtout comportement des roches ou des nappes aquifères dans la durée (milliard d’année)
- Quelles sont les limites ? les risques ?
* problèmes financiers, technologiques
* comportement des politiques/industriels : pas de recherche de solutions “propres” (problème identique à celui du rachat de la dette carbone !)

- Quelles sont les principales différences, ou les points communs, entre la séquestration “océanique” (voir les documents qui suivent) et la
séquestration “géologique” ?
Séquestration océanique Séquestration géologique
* Processus biologique, naturel, court (photosynthèse)
* Limites technologiques a priori plus simples (injection de Fer)
* Pas de problème de captage du CO2
* Stockage de courte durée (500 ans ?)
* Pas d’essai véritablement concluant
* Forçage d’un processus naturel long à très long
* Nombreuses limites technologiques
* Problème de captage du CO2 à la source de production
* Stockage long a priori
* Quelques essais déjà fonctionnels

Blain et al. (2007; Nature 26 avril) : a - position du Plateau des
Kerguelen; b - image satellite du bloom phytoplanctonique (trait blanc =
déplacement du navire océanographique); c - concentration en chlorophylle
a dans les stations au centre du bloom; d - mesure de la pCO2 le long du
trajet du bateau (voir a); figure ci-contre - mesure de la Dfe (dissolved
iron; fer soluble) de la surface à 500 m de fond au centre du bloom (rouge,
courbe de droite) et à l’extérieur du bloom (bleu, courbe de gauche), c’est
à dire en dehors du Plateau des Kerguelen (symbolisé par le rectangle sous
la courbe rouge).
Questions 3 : (i) quels liens peuvent être établis entre les figures b et c; b
et d; c et d ? (ii) expliquer la différence de concentration en fer au-dessus
et en dehors du Plateau des Kerguelen; (iii) quel(s) lien(s) avec les
remarques faites à la question (i) ?
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
1
/
12
100%