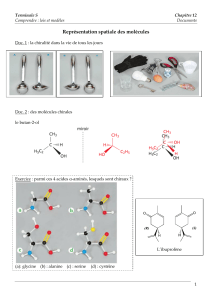
Représentation spatiale des molécules

L6 Représentations des molécules
I- Représentation spatiale des
molécules
1) Représentation de CRAM
Pour représenter dans un plan la géométrie spatiale
des molécules, on utilise les conventions de Donald
James Cram.
2) Stéréoisomérie
Deux molécules de même formule semi-développée peuvent correspondre à des espèces chimiques différentes,
selon la position de leurs atomes dans l’espace : on parle alors de stéréoisomérie. Les espèces chimiques sont
appelées des stéréoisomères.
II- Stéréoisomères de conformation
1) Définition
On appelle conformation d’une molécule la disposition dans l’espace des atomes de cette molécule les uns
par rapport aux autres.
Deux structures sont dites stéréoisomères de conformation si l’on peut passer de l’une à l’autre par rotation
autour d’une ou plusieurs liaisons simples. On passe ainsi d’une conformation à l’autre sans rompre de
liaison.
2) Conformation la plus stable
La conformation qui possède l’énergie potentielle la plus faible correspond à la conformation la plus stable.
III- Stéréoisomères de configuration
Deux stéréoisomères sont dits de configuration si, pour passer de l’un à l’autre, il est nécessaire de rompre
et créer des liaisons.
1) Enantiomères
a) Chiralité
Un objet est dit chiral s’il n’est pas superposable à son image dans un miroir plan. Dans le cas contraire, il est dit
achiral. Un objet présentant un élément de symétrie (plan ou centre) est achiral.
b) Atome de carbone asymétrique
Parmi les atomes de carbone tétraédrique, on distingue l’atome de carbone asymétrique, lié à
quatre atomes ou groupes d’atomes tous différents. On le note C*.
Une molécule possédant un seul carbone asymétrique et chirale.
c) Couple d’énantiomères
Deux molécules chirales et images l’une de l’autre dans un
miroir plan sont dites énantiomères l’une de l’autre.
Chacune constitue alors l’énantiomère de l’autre.
Liaisons dans le plan
Liaisons en avant du plan
Liaisons en arrière du plan
Conventions de Cram

Les chimistes synthétisent souvent des espèces chimiques sous forme d’un mélange équimolaire d’un couple
d’énantiomères. Ce mélange est appelé mélange racémique.
d) Chiralité des acides α-aminés
Tous les acides aminés naturels présentent, sur le même atome de carbone, appelé carbone α, le groupe
caractéristique carboxyle –COOH et le groupe amino –NH2.
A l’exception de la glycine, les acides α-aminés naturels possèdent un atome de carbone asymétrique et sont
donc chiraux.
La plupart des acides α-aminés naturels existent sous la forme de deux énantiomères, appelés D et L, selon
l’agencement des groupes d’atomes autour du C*. Les acides aminés L représentent la quasi-totalité des
acides aminés dans les protéines. En effet, les enzymes dégradent les D.
e) Importance de la chiralité dans la nature
Lors des processus de reconnaissance entre une molécule et des sites
récepteurs, la réponse physiologique peut être différente selon
l’énantiomère impliqué.
Le pouvoir tératogène, toxique ou thérapeutique, ou l’odeur sont ainsi
différents selon l’énantiomère qui interagit avec le site récepteur :
Carvone S sent le cumin et R la menthe fraîche.
L-Dopa : un énantiomère traite la maladie de Parkinson, l’autre est toxique.
2) Diastéréoisomères
On appelle diastéréoisomères des molécules de même formule semi-développée, non superposables et qui
ne sont pas images l’une de l’autre dans un miroir plan.
a) Diastéréoisomérie Z/E
Elle est due à l’impossibilité de rotation
rapide autour des doubles liaisons C=C.
Pour qu’une diastéréoisomérie Z/E
existe, il est nécessaire que la molécule
possède une double liaison et que
chaque atome engagé dans cette double
liaison soit lié à deux groupes d’atomes
différents.
b) Molécules à deux atomes de carbone asymétriques
1
/
2
100%