3.1 Utilisation de l`énergie lumineuse, photosynthèse et production d

ACTIVITÉS ÉLÈVES TS 05/02/17
3.1 Utilisation de l'énergie lumineuse, photosynthèse et production d'ATP
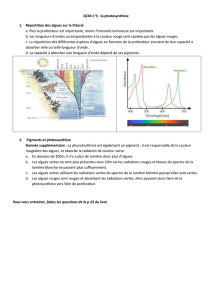
3.1.1 La feuille, organe clé de la photosynthèse
3.1.2 Le chloroplaste organite clé de la photosynthèse
Vous mettrez en évidence les mouvements de cyclose des chloroplastes chez l'élodée et l'influence
d'un poison respiratoire sur ces mouvements. Faire vérifier.
Proposez une explication à ces mouvements (intérêt pour la plante) par un texte court.
L'observation est facilitée dans une zone voisine de la nervure (cellules ayant peu de chloroplastes)
éclairées quelques minutes sous le microscope.
Daniel Devallois 74160 St Julien en genevois 2 Sur 14
http://www.infovisual.info

ACTIVITÉS ÉLÈVES TS 05/02/17
3.1.3 La phase photochimique de la photosynthèse
La cellule chlorophyllienne des végétaux verts effectue la photosynthèse grâce à l'énergie lumineuse.
3.1.3.1 Les rayonnements absorbés par les végétaux chlorophylliens (spectre d'absorption)
Séparez les différents pigments d'une solution de chlorophylle brute puis déterminez le spectre
d'absorption de cette solution brute. Présentez le résultat sous la forme de votre choix. D'après vos
résultats, quelles sont les longueurs d'ondes qui pourraient être efficaces pour la photosynthèse ?
Afin de déterminer les rayonnements absorbés, il est nécessaire:
1- d'extraire les pigments
2- de déterminer les longueurs d'ondes absorbées par ces pigments
1- L' extraction des pigments:
Les pigments concernés étant solubles dans l'alcool, l'extraction se fera dans l'alcool à 90°.
(voir physique chimie pour autres solvants (eau, lipides ...))
épinard ou autre feuilles bien vertes
Liste du matériel disponible:
mortier 1 par groupe
alcool à 90° / autre 10 ml par groupe
épinard / autre QSP classe
bécher + gaze 1 par groupe
pipette fine pour dépôt 1 par groupe
2- La séparation des pigments, chromatographie:
(voir physique chimie pour autres solvants (alcool, mélanges ...))
s'agissant de molécules organiques, la séparation se fera dans des solvants organiques.
Liste du matériel disponible:
papier à chromatographie 1 par groupe
solvant (Ether de pétrole/Acétone/Cyclohexane : 85/10/5% ) /autre QSP classe au fond de la salle
éprouvette/chromatographie 1 par groupe
bouchon et fixation pour le papier 1 par groupe
nécessaire pour obscurité dans l'éprouvette 1 par groupe
Remarques:
limiter la durée pour ne pas monter trop haut (~30 minutes)
faire le dépôt à au moins 2 cm du bord inférieur pour pouvoir faire tremper dans le solvant sans problème
réaliser des dépôts aussi petits que possible (sécher au sèche cheveu pour éviter l'étalement)
réaliser plusieurs dépôts pour concentrer le pigment (4-5)
3- Détermination des longueurs d'ondes absorbées:
L'utilisation d'un spectroscope ou d'un spectrophotomètre permet de déterminer les longueurs d'ondes
absorbées.
Liste du matériel disponible:
spectroscopes (boites bleues PM) autant que possible
Remarque :
Pour les nouveaux spectroscopes, diluer beaucoup (transparent à l’œil).
Daniel Devallois 74160 St Julien en genevois 3 Sur 14

ACTIVITÉS ÉLÈVES TS 05/02/17
3.1.3.2 Pigments, rayonnements et photosynthèse
D'après les documents proposés, quels sont les pigments efficaces pour la photosynthèse ?
Document 1: Pigments foliaires observés par chromatographie
Document 2: Spectre d'absorption des pigments foliaires obtenu par spectrophotométrie
Le spectre d’absorption est obtenu en éclairant
les cellules photosynthétique avec un éclairement
monochromatique (une seule longueur d'onde).
L'absorption est déterminée en mesurant la
quantité de rayonnement absorbée.
Document 3: Spectre d'action des pigments foliaires
Le spectre d'action est obtenu en éclairant les cellules
photosynthétique avec un éclairement monochromatique.
L'efficacité photosynthétique est déterminée en mesurant
soit la quantité de dioxygène produit par unité de temps soit la
quantité de dioxyde de carbone absorbée par unité de temps.
Daniel Devallois 74160 St Julien en genevois 4 Sur 14
Principe du spectrophotomètre
(pour information, pas à commenter)

ACTIVITÉS ÉLÈVES TS 05/02/17
3.1.3.3 Détermination expérimentale de l'intensité photosynthétique
Présentation du matériel :
mise en place des capteurs voir positions ci-dessous
ATTENTION : ne pas mettre dans l'eau le capteur lumière
(voir nom du capteur sur le capteur)
Présentation du logiciel :
à l'ouverture du logiciel, clic sur la fenêtre qui s'ouvre au milieu pour accéder au logiciel
O2 dissous refuser le paramétrage (déjà fait)
CO2 refuser le paramétrage (déjà fait)
Observer les fenêtres de gauche / de droite
fenêtre de gauche à 2 onglets onglet paramétrage onglet données
fenêtre de droite = fenêtre d'affichage des données stockées dans la fenêtre de gauche
manipulation des axes possible
double clic sur le titre d'un axe pour adapter automatiquement l'échelle aux données
clic de part et d'autre de la barre au centre d'un axe pour déplacer le début ou la fin de cet axe
Proposez un protocole permettant de mettre en évidence l'influence de la qualité et de la quantié de
lumière sur la photosynthèse.
Le logiciel Latis-bio
Pour éviter d'avoir à manipuler le logiciel pendant les mesures, prévoir un temps plutôt trop long que
trop court.
Daniel Devallois 74160 St Julien en genevois 5 Sur 14
Fenêtre graphique
Liste des courbes
paramétrage
de l'acquisition
Axe gauche du graphique
Déclenchement
des mesures
Indication du temps

ACTIVITÉS ÉLÈVES TS 05/02/17
3.1.3.4 L'origine du dioxygène dégagé
D'après les documents ci dessous (Nathan spécialité) quelles sont les conditions nécessaires
au dégagement de dioxygène lors de la photosynthèse ? (type 2b).
Document 1: influence d'un accepteur d'électrons (oxalate de potassium ferrique) sur la photosynthèse.
Document 2: Origine des atomes d'oxygène des molécules de dioxygène produites
Une suspension d'algues éclairée est placée dans une eau marquée par de l'oxygène 18 (isotope radioactif
de l'oxygène = *O dans les réactions ci dessous). Le résultat de cette réaction est schématisé ci dessous:
6 CO2 + 12 H2*O C6H12O6 + 6 *O2+ 6 H2O
La même expérience est réalisée avec du CO2 marqué. Le résultat est le suivant:
6 C*O2 + 12 H2O C6H12*O6 + 6 O2+ 6 H2*O
Document 3: les conditions d'oxydation de l'eau (doc 31 à gauche, doc 32 à droite)
Daniel Devallois 74160 St Julien en genevois 6 Sur 14
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
1
/
14
100%