Vaccination thérapeutique en oncologie

Vaccination thérapeutique en oncologie :
Dr Denis Migliorini, service oncologie, HUG Genève
Les buts de cette présentation sont d’explorer l’interaction qu’il existe entre le système
immunitaire et le cancer, de revoir chaque composant de la réponse immunitaire impliquée
dans la détection et la destruction tumorale, mais aussi les mécanismes qui permettent un
échappement tumoral à une telle réponse par le biais notamment de voies de signalisations
qui bloquent l’activation des lymphocytes T.
Le postulat selon lequel le système immunitaire pourrait jouer un rôle est parti d’un ensemble
d’observations à savoir qu’il existe :
- Une corrélation entre l’importance de l’infiltrat immun intratumoral et la survie globale
- Une corrélation entre l’augmentation de l’incidence des tumeurs et
l’immunosuppression
- des régressions tumorales spontanées (mélanome).
L’Immunologie tumorale comprend tout un ensemble de concepts de base, les cellules
immunitaires impliquées ont toutes des rôles différents.
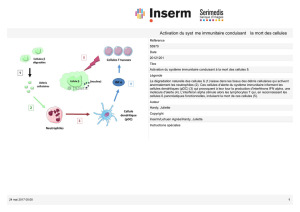
Tout part de la détection d’Antigènes(Ag), mutés ou non, dits associés aux tumeurs par des
cellules présentatrices d’antigènes telles que les cellules dendritiques, une fois détectés par
des récepteurs universaux (Toll like récepteurs), ces cellules ont la capacité de phagocyter la
cellules tumorale, la digérer et processer des antigènes qu’elle présentera à sa surface par
le biais de complexes majeurs d’histocompatibilité (MHC). Ce faisant ces cellules
dendritiques entament un processus de maturation qui les mèneront jusqu’au premiers relais
ganglionnaires où elles présenteront les Ag anormaux aux cellules T. Ceci va induire
l’activation des T cells qui vont se diviser de façon exponentielle et délivrer dans la
circulation des clones de cellules T spécifiques d’un Ag donné. Ces cellules vont de même
acquérir la capacité de retourner sur le site tumoral par le biais de chemokines activatrices
(CXCR4, α1β4 Integrins).
Alors Pourquoi ces mécanismes ne fonctionnent-il pas en réalité ? l’explication sur le plan
théorique a été donnée sur la base de modèles murins par Shreiber qui décrit l’échappement
de la tumeur au système immunitaire comme la théorie des 3Es (Elimination, Equilibre,
Editing).
En effet suite à la reconnaissance du pathogène, l’organisme parvient à Eliminer un
contingent tumoral, survient après une phase d’Equilibre puis Echappement et ce suite à
deux types de réactions :
- Au niveau tumoral : sous expression des complexes MHC et donc de la présentation
antigénique, expression de cytokines (TGFβ, IL10, VEGF) qui recrutent des cellules

immunosuppressives (Tregs, MDSCs), exploitation de ces fameux immunes checkpoints
nécessaires à l’activation des cellules T (CTLA4, PD1).
- Au niveau du microenvironnement Tumoral : sécrétion de molécules émanant de
cellules immunosuppressives (de façon autocrine).
La compréhension de tous ces mécanismes et de cette balance fragile entre activation et
inhibition du système immunitaire a permis de faire de grandes avancées dans le domaine
de l’immuno-oncologie qui a commencé par la toxine de Cooley en 1891 qui reporte des
régressions tumorales suite à l’inoculation de germes chez des patients atteints de sarcome
tels que le streptocoque pyogene et serratia marcescens. Une fois mixés leur propriété, par
le biais de cytokines inflammatoires et activation des DC, était d’éliciter une réponse
tumorale croisée contre la tumeur. Plus récemment l’arrivée des anticorps anti CTLA4 et
PD1 qui lèvent l’inhibition sur les cellules T ont fait beaucoup de bruit au vu de leur résultats
cliniques qui ont révolutionné la prise en charge des mélanomes métastatiques.
Il existe différentes stratégies d’immunothérapie :
- Immunothérapie active : Vaccination (Peptidique, anti-lysat/RNA/DNA tumoral, virus
oncogene vaccin exploitant les propriétés des DCs )
Un exemple : la vaccination peptidique dirigée contre les Gliomes de Haut Grade à
Genève
- Immunothérapie adoptive (T cells clonotypiques, CARs chimeric antigen receptors)
- L’utilisation des facteurs influençant le microenvironnement tumoral
- Et éventuellement les combinaisons entre les thérapies cytotoxiques et les
immunothérapies
En Conclusion, l’avenir sera très certainement caractérisé par une personnalisation des
thérapeutiques anticancéreuses, une combinaison des différentes stratégies et sur le plan
pratique la collaboration entre pharmacie, biologistes et médecins avec l’augmentation des
moyens à mettre à disposition pour chaque patient (thérapies couteuses++).
1
/
2
100%