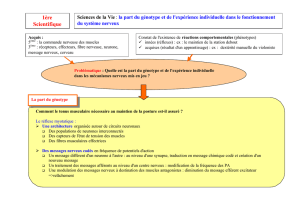
détermination du génotype rhd fœtal

Applications au Diagnostic
Prénatal Non Invasif
14 octobre 2015
La PCR Digitale
Dr Juliette Nectoux
Service de Génétique
GHU Paris Centre
Hôpital Cochin
ATELIER SFBC 2015

DIAGNOSTIC PRÉNATAL INVASIF
Amniocentèse
(15 SA)
Biopsie de
Trophoblaste
(11 SA)
CONTEXTE
•Antécédents familiaux de maladie génétique
•Dépistage combiné trisomie 21 à risque
•Signe(s) d’appel échographique(s)
INCONVÉNIENTS
•Terme
•Fausses-couche
•Prématurité, Hémorragie, Infection…
0,5 à 1% de risque de perte fœtale
ATELIER SFBC 2015

SOURCES DE MATÉRIEL FŒTAL
•Cellules Fœtales dans la Circulation Maternelle
•Acides Nucléiques Fœtaux dans la Circulation Maternelle
-ARN fœtal libre
-ADN fœtal libre
ADN FŒTAL LIBRE
•Origine trophoblastique
•Détectable dès 5 SA
•[ADNfl] augmente au cours de la grossesse
•Disparait de la circulation maternelle 30 min après
l’accouchement
Lo et al, Lancet, 1997
DIAGNOSTIC PRÉNATAL NON INVASIF
ATELIER SFBC 2015

DÉFIS TECHNIQUES
DÉTECTION DE L’ADNF
Faible quantité absolue d’ADN plasmatique
Faible proportion d’ADNf
ATELIER SFBC 2015

DÉFIS TECHNIQUES
DÉTECTION DE L’ADNF
Faible quantité absolue d’ADN plasmatique
Faible proportion d’ADNf
DÉLAI DE PRISE EN CHARGE DES PRÉLÈVEMENTS
Influence sur la proportion d’ADNf
ATELIER SFBC 2015
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
1
/
34
100%