activité1

Notions abordées dans les questions : Principe actif / excipient / Formulation / Espèces naturelles et
synthétiques
PARTIE I : ETUDE DOCUMENTAIRE
HISTORIQUE
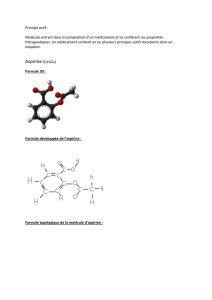
A l’origine de la synthèse de l’aspirine, molécule qui n’existe pas dans la nature, il y a l’acide salicylique,
molécule extraite de plantes telles que le saule, la reine-des-prés (spirée) qui agit comme antipyrétique et
analgésique. L’acide salicylique est synthétisé industriellement dès 1874, c’est-à-dire avec les débuts de la
chimie organique, mais en raison d’effets secondaires, on cherche à le transformer pour obtenir un
médicament moins agressif pour l’organisme.
C’est le chimiste allemand Félix Hoffmann, qui travaille pour l’entreprise de chimie Bayer, qui met au point
la synthèse de l’aspirine ou acide acétylsalicylique ; son collègue pharmacologue Arthur Eichengrün avait,
quant à lui, remarqué en premier les propriétés antalgiques de l’aspirine. Aspirine® est le nom choisi par la
firme Bayer et Cie.
1. Rechercher la signification des mots en italique.
2. L'aspirine est-elle une substance chimique naturelle ou synthétique? Justifier.
3. Chercher l'explication du nom commercial d’Aspirine® donné à la molécule d’acide
acétylsalicylique.
FORMULATION
L’acide acétylsalicylique, à température ordinaire, se présente sous forme d’une poudre blanche, pas du tout
agréable à absorber, même avec beaucoup de sucre !
Cette poudre a subi, depuis sa création, toute sorte de transformation, pour la rendre plus comestible et
digeste. Elle a été, comme une star qu’elle est, maquillée, parée, coiffée, remplie de bulles… pour nous la
rendre plus agréable et plus efficace. Cette étude se fait par des pharmaciens spécialistes de la galénique* et
de la pharmacocinétique qui s’appuie sur les propriétés de la molécule et du milieu dans lequel elle va se
trouver.
Il en résulte de nombreuses formulations qui en toutes en commun le principe actif acide acétylsalicylique ou
de son dérivé, l’ion acétylsalicylate ; les différences sont dues à la variété des excipients utilisés.
Il existe huit principales formes galéniques, mises au point par des chimistes et des pharmaciens, pour
répondre à des besoins thérapeutiques spécifiques et /ou de confort pour le malade.
En voici quelques-unes:
ASPIRINE DU RHONE 500
Composition
Acide acétylsalicylique 500 mg
Excipient : amidon, gel de silice.
Mode d'administration
Doit être utilisé de préférence avant ou au
cours d'un repas même léger. Absorber les
comprimés après les avoir fait désagréger
dans un verre d'eau
ASPEGIC 500
Composition
Acétylsalicylate de DL lysine : 900 mg
(quantité correspondante en acide
acétylsalicylique: 500 mg)
Excipient : glycine, arôme mandarine,
glycyrrhizinate d'ammonium pour un
sachet.
Mode d'administration
Boire immédiatement après dissolution
complète dans un grand verre d'eau, lait,
soda ou jus de fruit.
ASPIRINE UPSA 325, gélule
Composition
Acide acétylsalicylique : 325 mg
Excipient : Lactose monohydraté,
béhénate de glycérol.
Mode d'administration
Les gélules sont à avaler avec un verre
d'eau.
4. Rechercher la signification des mots en italique.
5. Citer quelques types d'excipients contenus dans des formulations d'aspirine.
6. A quoi correspond la notation « 500 » ou « 325 » qui suit le nom de la formulation?
TP N°1 : ETUDE DE DIFFERENTES FORMULATIONS DE L'ASPIRINE

EFFETS SECONDAIRES
Des effets gastro-intestinaux indésirables
L'aspirine® (ou acide acétylsalicylique) est active après son passage dans le sang du patient, et donc après
avoir traversé les parois lipidiques de l'estomac ou de l'intestin. Mais cette traversée n’est pas toujours sans
danger pour le patient.
L’aspirine® se dissout dans les graisses présentes dans la muqueuse de l’estomac qui est un milieu acide ;
elle se « fixe » donc sur la paroi stomacale et exerce une action corrosive sur la muqueuse gastrique. De
nombreuses recherches ont été entreprises afin d’améliorer la tolérance de ce médicament. Elles ont abouti à
la mise au point de différentes formes pharmaceutiques. En 1941, l’allemand Harold Scruton utilisa de
l’amidon comme excipient afin de faciliter la solubilité globale du médicament dans l’eau et ainsi favoriser
son absorption dans le corps humain. Cependant, les particules d’aspirine® ainsi obtenues, des « paquets »
de molécules, très peu solubles dans l’eau, étaient encore trop grosses et la gastrotoxicité du médicament n’a
pas été diminuée. De nouvelles formes pharmaceutiques ont été mises au point afin de réduire la taille des
particules d'aspirine, le temps de contact entre les particules d’aspirine et la muqueuse gastrique, voire de
modifier le lieu d’absorption du médicament.
7. A quoi semble être principalement dus les effets indésirables de l'aspirine sur l'estomac?
8. Sur quels paramètres travaillent les pharmacologues pour diminuer cet effet?
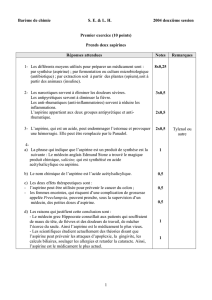
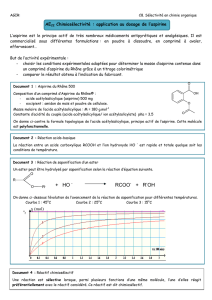
L'ACIDE ACÉTYLSALICYLIQUE ET SON DÉRIVÉ
La molécule d’aspirine ou acide acétylsalicylique est peu soluble dans l’eau et se trouve dans les solutions
dont le pH est inférieur à 3,5.
Pour faciliter sa prise et diminuer ses effets secondaires, on peut la prescrire sous forme d’ions
acétylsalicylate (associés à un cation comme l’ion sodium) car ceux-ci sont très solubles dans l’eau. La
solution qui les contient a un pH supérieur à 3,5.
On note AH l’acide acétylsalicylique et A- l’ion acétylsalicylate.
9. Parmi les 3 formulations dont vous avez la composition, quelle est celle qui contient la forme
ionique de l'aspirine ? Que note-t-on dans le mode d'administration par rapport aux autres
formulations proposées?
__ __
0 3,5 14
10. Compléter cet axe gradué en pH en faisant apparaître le domaine où on trouve l’espèce AH et celui
où on trouve l’espèce A- (ces domaines s’appellent domaines de prédominance).
Quelle que soit la forme absorbée, AH ou A-, celle-ci va dans l’estomac dont le pH se situe entre 1 et 2. Une
partie de l'aspirine peut également être absorbée au niveau de l'intestin dont le pH se situe entre 7 et 8
11. Sous quelle forme trouve-t-on l’aspirine dans l’estomac ?
12. Sous quelle forme trouve-t-on l’aspirine dans l’intestin ?

PARTIE II : ETUDES EXPERIMENTALES
Objectifs : Pratiquer une démarche expérimentale pour montrer qu'une espèce active interagit avec le
milieu dans lequel elle se trouve (nature du solvant, pH).
Savoir qu'une solution peut contenir des molécules ou des ions
Notions abordées expérimentalement et dans les questions : Solution : solvant, soluté, dissolution d’une
espèce moléculaire ou ionique
A – ETUDE D'UN EXCIPIENT
1. Mise en évidence
a) Etude préliminaire : influence de la nature du solvant
Objectif : on se propose ici de vérifier l'influence de la nature du solvant sur la solubilité d'une espèce
chimique
• Introduire 500mg d'aspirine pure (ou acide acétylsalicylique) dans un bêcher contenant 50mL d'eau,
Agiter à l'aide d'un agitateur en verre. Observer. Ce bécher sera conservé tout au long de la
première partie du TP.
• Recommencer l'expérience avec 50mL d'éthanol puis avec 50mL d'huile d'olive.
Question 1 : Comparer la solubilité de la molécule l'acide acétylsalicylique dans chacun des solvants et
compléter la première colonne du tableau suivant avec des expressions comme faible, très faible, élevée, très
élevée...
Espèce chimique
Acide acétylsalicylique
Formule brute
C9H8O4
Solubilité dans l'eau
Solubilité dans l'éthanol
Solubilité dans l'huile
b) Mise en évidence d'un excipient
Objectif : on se propose ici de mettre en évidence la présence d'autres espèces chimiques que le principe
actif dans un médicament
• Broyer soigneusement un comprimé d'Aspirine du Rhône 500 dans un mortier puis introduire la
poudre dans un bécher contenant 10mL d'éthanol. Filtrer. Rincer le mortier à l'éthanol au-dessus du
filtre.
On observe un dépôt solide sur le filtre.
Question 2 : D'après le tableau précédent, pourquoi peut-on affirmer que ce solide n'est pas de l'acide
acétylsalicylique? Un comprimé d'aspirine commercial est-il pur?
• Verser quelques gouttes d'eau iodée sur le solide contenu dans le filtre.
Question 3 : Quelle est l'espèce chimique identifiée dans l'excipient?
2. Mise en évidence du rôle d'un excipient
Objectif : on se propose ici d'illustrer le rôle d'un excipient comme l'amidon dans une formulation classique
d'un comprimé d'aspirine
• Broyer soigneusement un comprimé d'Aspirine du Rhône 500 dans un mortier puis introduire la
poudre dans un bêcher contenant 50mL d'eau. Ce bécher sera conservé tout au long du TP et sera

noté bêcher A.
Question 4 : Quelle différence y-a-t-il entre la solution préparée avec de l'aspirine pure et celle préparée
avec ce comprimé pharmaceutique? A quoi sert l'excipient?
Question 5 : En utilisant les données documentaires dont vous disposez, dire si cette formulation est
totalement satisfaisante pour l'estomac.
B – ETUDE DE QUELQUES FORMULATIONS
1. Aspirine dite « soluble » ou « Aspégic »
Objectif : « Il est préférable, pour éviter des problèmes d’irritation gastrique, d’absorber l’aspirine sous sa
forme ionique A- plutôt que sous forme moléculaire AH. » Nous allons tenter d'illustrer cette affirmation
dans cette partie.
• Dissoudre un sachet de 500 mg d'Aspégic® dans un bêcher contenant 50 mL d'eau (bêcher B).
Utiliser un agitateur en verre si besoin.
Question 1 : Comparer le résultat avec celui obtenu pour le comprimé d'aspirine du rhône 500 (bêcher A)
noter vos observations et donner un premier avantage de la formulation sous forme d'Aspegic.
• Mesurer le pH des solutions obtenues avec l'Aspegic® et l'Aspirine du Rhône®.
Pour étudier ce qui se passe lorsque le médicament arrive dans l'estomac, on souhaite reproduire au
laboratoire les conditions chimiques régnant dans le milieu stomacal qui est un milieu acide.
Question 2 : Proposez une expérience qui permettrait de simuler cette condition.
• Faire valider la proposition d'expérience par le professeur
Question 3 : Qu’observez-vous ? Expliquer vos observations à l’aide des données et en utilisant les mots
« soluble » « forme moléculaire »et « forme ionique ».
Question 4 : Observer la texture des précipités obtenus dans les deux béchers et expliquer pourquoi
l'Aspégic® est une bonne alternative à l'aspirine du Rhône® pour les estomacs fragiles.
2. Aspirine retard : Aspirine pH8
Cette formulation se présente sous forme de comprimé, gastro-résistant. Le pH de l’intestin est supérieur à 7.
• Casser un comprimé à l’aide d’un mortier. Introduire un morceau de l’enrobage, dans 3 tubes à essai
contenant, respectivement, une solution d’acide chlorhydrique (à 0,1 mol.L-1), de l'eau, une solution
d’hydroxyde de sodium (à 0,1 mol.L-1),. Mesurer le pH de chaque solution.
Question 1 : Qu’observez-vous ? Pourquoi parle-t-on de comprimé gastro-résistant?
Question 2 : A quel niveau du corps humain est alors libéré le principe actif? Sous quelle forme se trouve t-
il ? Justifier.
Question 3 : Cette formulation convient-elle bien pour soulager un mal de tête soudain ?
3. Aspirine effervescente tamponnée ; une autre forme d’aspirine soluble
• Dissoudre un morceau de comprimé dans un tube à essai contenant de l'eau.
Question 1 : Qu’observez-vous ? Que vaut le pH de la solution ?
• Ajouter alors un peu de solution d’acide chlorhydrique ; mesurez le pH.
• Ajouter à nouveau de la solution acide.
Question 2 : Comment évolue le pH au fur et à mesure des ajouts d’acide ? Que simule-t-on ?
Question 3 : Que pensez-vous de cette formulation ?
Question 4 : Quel est, à votre avis, le gaz qui provoque l’effervescence ? Comment peut-on le mettre en
évidence expérimentalement ?
1
/
4
100%